Alkadieenejä tai dieenejä on kolme tyyppiä:
1-kertynyt: Kaksoissidokset sijaitsevat samalla hiilellä ja esiintyvät peräkkäin:
─C ═ Ç ═ C -
│ │
2- Eristetty: Kaksoissidokset ovat eri hiileillä ja erotettu vähintään kahdella peräkkäisellä yksittäisellä sidoksella:
│
─C ═ C C - C ═ C -
│ │ │ │ │
3- Konjugaatit: Kaksoissidokset esiintyvät vuorotellen, erotettuna yhdellä yksittäisellä sidoksella:
─C ═ C C ═ C -
│ │ │ │
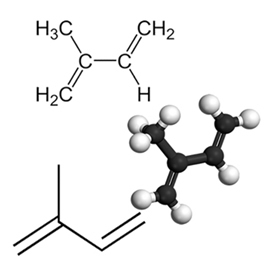
Esimerkki tärkeästä konjugoidusta dieenistä on isopreeni, joka on orgaanisten yhdisteiden luokan terpeeniryhmän emäksinen yksikkö. erittäin tärkeää, joitain esimerkkejä isopreenien muodostamista tuotteista ovat kumi, beetakaroteeni (vastuussa porkkanat), A-vitamiinia ja hedelmien kuorissa, siemenissä, kukissa, lehdissä, juurissa, vihanneksissa ja puussa esiintyviä öljyjä, kuten limoneeni ja myrseeni.
Kohteeseen kertyneet ja eristetyt dieenit, lisäysreaktioita tapahtuu aivan kuten alkeenien tapauksessa, mitä voit ymmärtää lukemalla tekstin Lisäysreaktiot. Ainoa ero on se, että dieenit käyvät läpi tämän tyyppisen kaksoisreaktion, koska niillä on kaksi kaksoissidosta, kun taas alkeeneilla on vain yksi kaksoissidos.
Kuitenkin konjugoituja dieenejä, additioreaktiolla on erityispiirre, koska nämä yhdisteet voivat käydä resonanssissa, joten lisäys voi tapahtua kahdella tavalla:
1- Lisäys 1.2:
Tätä pidetään normaalina lisäyksenä, koska lisäys tapahtuu kahdella hiiliatomilla, jotka muodostavat saman kaksoissidoksen, eli hiileille 1 ja 2:
Älä lopeta nyt... Mainonnan jälkeen on enemmän;)
H2Ç ═ CH─ CH ═ CH2 + HBr → H2C CH─ CH ═ CH2
│ │
HBr
Katso, että tämän tyyppinen reaktio seuraa Markovnikovin sääntö, vety sitoutuu enemmän hydrattuun hiileen (johon on kiinnittynyt enemmän vetyatomeja).
Lisäys 1,2 prosessoidaan matalissa lämpötiloissa (-60 ° C).
2- Lisäys 1.4:
Tässä tapauksessa reaktio etenee korkeissa lämpötiloissa. On tärkeää korostaa, että sekä lisäyksen 1,2 että 1,4: n tulo muodostuu aina, mutta lämpötila osoittaa, mitä muodostuu suurempana määränä.
Seuraava on esimerkki tyypin 1.4 lisäyksestä:
H2Ç ═ CH─ CH ═ CH2 + HBr → H2C CH ═ CH─CH2
│ │
HBr
Huomaa, että tapahtuu seuraava, jokaisen kaksoishiilen pi-sidoksessa yksi jaetuista elektroneista ovat yhteisiä substituentin kanssa ja muut muodostavat uuden kaksoissidoksen muiden hiilien välillä:
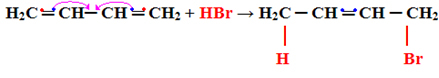
Kirjailija: Jennifer Fogaça
Valmistunut kemian alalta
Haluatko viitata tähän tekstiin koulussa tai akateemisessa työssä? Katso:
FOGAÇA, Jennifer Rocha Vargas. "Additioreaktiot Dienesissä"; Brasilian koulu. Saatavilla: https://brasilescola.uol.com.br/quimica/reacoes-adicao-dienos.htm. Pääsy 28. kesäkuuta 2021.