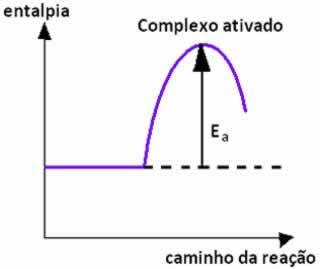
Katalyytin toiminnan tarkoituksena on periaatteessa nopeuttaa tietyn reaktion kehittymistä. Tämä on mahdollista, koska katalyytti muuttaa mekanismia, jolla reaktio etenee, mikä johtaa "vaihtoehtoiseen polkuun", joka vaatii vähemmän aktivointienergiaa, jotta reaktio alkaa ja saavuttaa aktivoidun kompleksin.
Katalyysejä on useita, joista yksi on heterogeeninen katalyysi, joka voidaan määritellä se, joka tapahtuu, kun järjestelmässä on useampia kuin yksi faasi, toisin sanoen reagoivat aineet ja tuotteet ovat fysikaalisessa tilassa, joka eroaa katalyytin fyysisestä tilasta.
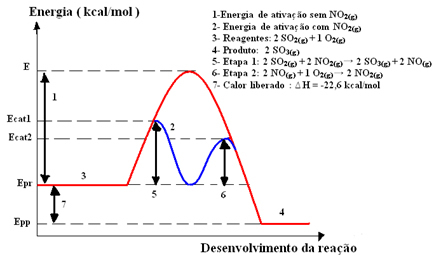
Esimerkkinä voimme mainita rikkihapon muodostumisen välivaiheen (H2VAIN4 (aq)). Tämä vaihe koostuu rikkitrioksidin (SO3 g)) rikkidioksidin (SO2 g)):
2 SO2 g) + O2 g) → 2 käyttöjärjestelmää3 g)
Kun tämä reaktio etenee niin hitaasti, katalysaattoria käytetään sen nopeuttamiseen. Katalyytti, jota voidaan käyttää tässä tapauksessa, on divanadiumpentoksidi (V2O5 (S)), joka on kiinteä. Koska reagoivat aineet ja reaktiotuote ovat kaasumaisia, meillä on heterogeeninen järjestelmä.
Mutta miten divanadiumpentoksidi voi nopeuttaa reaktiota?
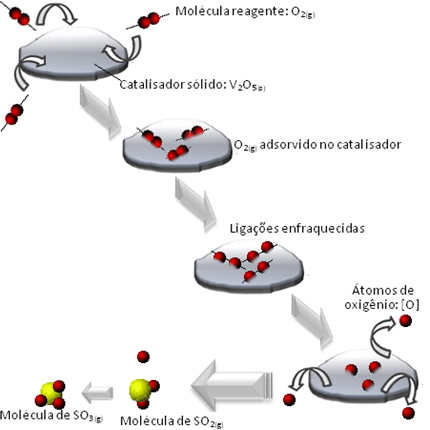
Tapahtuu, että happireagenssin molekyylit adsorboituvat, toisin sanoen pidätetään divanadiumpentoksidin pinnalla. Tämä aiheuttaa tämän kaasun molekyylien sidosten heikkenemisen ajan myötä, mikä helpottaa kompleksin muodostumista aktivoituu ja siten vähentää reaktion aktivointienergiaa lisäämällä sen kehitysnopeutta eli sen nopeus.
Älä lopeta nyt... Mainonnan jälkeen on enemmän;)
Katso kuinka tämä tapahtuu alla olevasta kaaviosta:
Muita esimerkkejä heterogeenisesta katalyysistä on esitetty alla. Huomaa, että molemmissa tapauksissa reagoivat aineet ja tuotteet ovat kaasumaisessa, vesipitoisessa tai nestemäisessä tilassa, kun taas katalyytit ovat kiinteässä tilassa:
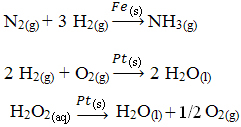
Esimerkki heterogeenisestä katalyysistä, joka tapahtuu jokapäiväisessä elämässämme, on muuntimien katalyysi auton katalyyttinen, paremmin tunnettu katalyytit. Nämä pilaantumisenestolaitteet on päällystetty aineilla, jotka toimivat katalysaattoreina yleensä palladium- ja rodiumseos (bensiinimoottoreille) ja palladium ja molybdeeni (bensiinimoottoreille). alkoholi).
Tämän katalyytin sisällä tapahtuu kemiallisia reaktioita, joissa epätäydellisestä palamisesta syntyvät kaasut, jotka ovat ihmisille haitallisempia, muutetaan myrkyttömiksi kaasuiksi. Reagenssit ja tuotteet ovat kaikki kaasuja, kun taas katalyytit ovat kiinteitä aineita.
Jos haluat lisätietoja tämän laitteen käyttöjärjestelmästä, lue teksti: "Katalysaattori”.
Kirjailija: Jennifer Fogaça
Valmistunut kemian alalta
Haluatko viitata tähän tekstiin koulussa tai akateemisessa työssä? Katso:
FOGAÇA, Jennifer Rocha Vargas. "Heterogeeninen katalyysi"; Brasilian koulu. Saatavilla: https://brasilescola.uol.com.br/quimica/catalise-heterogenea.htm. Pääsy 27. kesäkuuta 2021.