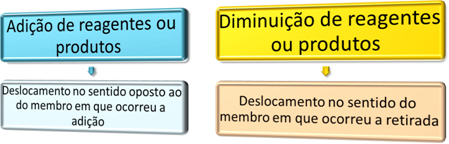
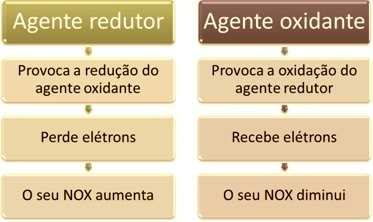
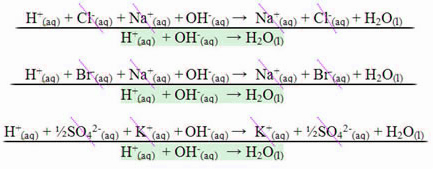Yksi pääpiirteistä, jotka erottavat hapetus-pelkistysreaktion (tai redox) on hapettimen ja pelkistysaineen läsnäolo, joka voidaan määritellä seuraavasti:
Katso esimerkiksi alla olevaa kemiallista reaktiota, jossa alumiini (Al) syöpyy kloorivetyhapon (HCl) vesiliuoksessa. Alumiiniatomit siirtävät elektroneja H-kationeihin+(tässä) ja tuottaa Al-kationin3+(tässä):
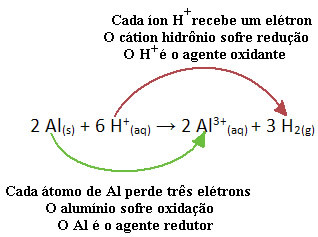
Huomaa, että koska Al siirsi elektroneja, tämä tarkoittaa sitä hän aiheutti vähennyksen H-kationeista+(tässä); siksi hänet kutsutaan pelkistävä aine. Jo kationi H+(tässä) poisti elektronit alumiinista, aiheuttaen hapettumista kyseisen metallin; siksi hän toimii a hapettava aine.
Jokapäiväisessä elämässä on monia esimerkkejä hapettavien ja pelkistävien aineiden toiminnasta. Katsokaa joitain niistä ja muista kuitenkin, että kaikissa tapauksissa pelkistys tapahtuu samanaikaisesti hapettumisen kanssa; siksi, jos on pelkistävää ainetta, on myös hapettava aine.
- Esimerkkejä pelkistävistä aineista:
- Valokuvauselokuvissa: valokuvauselokuvat sisältävät valolle herkkiä hopeasuoloja. Pisteissä, joissa esiintyy valon esiintymistä, Ag-ionit vähenevät +, mikä johtaa negatiivisissa tapauksissa havaittuun kontrastiin.

- C-vitamiini: C-vitamiini (L-askorbiinihappo) on voimakas pelkistävä aine vesiliuoksessa. Sillä on poikkeuksellinen mahdollisuus hapettaa, ja siksi sitä käytetään laajalti, erityisesti elintarvikkeissa antioksidantti, toisin sanoen, se lisätään muihin elintarvikkeisiin ja suojaa niitä mahdollisilta hapettumisilta, koska ne ovat omia uhrata. Esimerkkinä voidaan mainita hedelmät, kuten omenat ja päärynät, jotka tummuvat kosketuksissa ilmassa olevan hapen kanssa, koska ne hapettavat. Mutta kun lisäät pienen määrän appelsiini- tai sitruunamehua (jotka sisältävät C-vitamiinia) hedelmiin leikattu, tämä estää tämän reaktion esiintymisen, koska C-vitamiini toimii pelkistävänä aineena ja hapettuu ennen hedelmää.

- Vetykaasu: vetykaasu (H2) käytetään rakettien työntövoimana ja sitä pidetään yhtenä tärkeimmistä energiavaihtoehdoista, koska sen palaminen vapauttaa suuren määrän energiaa eikä pilaavia aineita. Tässä reaktiossa vety toimii pelkistävänä aineena, hapen hapettamana.
- Esimerkkejä hapettimista:
- Etikan tuotannossa: kun viini altistuu ilmalle, se muuttuu etikaksi, jonka pääkomponentti on etikkahappo. Tämä johtuu siitä, että viinissä oleva etyylialkoholi tai etanoli hapettuu kosketuksessa ilmakehän hapen kanssa, mikä johtaa etikkahappoon. Täten happi on hapettava aine. Jopa termin "hapetus" alkuperä liittyy reaktioon hapen kanssa.

Älä lopeta nyt... Mainonnan jälkeen on enemmän;)
- Ruosteessa: kuten edellisessä esimerkissä todettiin, happi toimii hapettimena alkoholille; ja se tekee tämän myös kosketuksessa erilaisten metallien, kuten raudan kanssa, aiheuttaen ruostumisprosessin. Ilmassa olevan hapen lisäksi muita hapettimia on tässä tapauksessa vesi tai hapan liuos.
- Valkaisuaineissa: valkaisuaineiden valkaisuvaikutus johtuu kahden seuraavan pelkistimen läsnäolosta: o hypokloriittianioni (yleensä natriumsuolan - NaOCl muodossa), läsnä esimerkiksi valkaisuaineessa; ja vetyperoksidi (H2O2), jota markkinoidaan vetyperoksidina. Näillä kahdella yhdisteellä on erittäin vahva taipumus hapettaa ja aiheuttaa muiden kemiallisten lajien pelkistymistä. Siksi ne ovat vastuussa hapettavista aineista, jotka antavat tuotteille tumman värin. Esimerkiksi selluloosassa ligniini hajoaa ja muuttuu kevyemmäksi ja muokattavammaksi. Tahranpoiston ja kankaan valkaisun tapauksessa nämä hapettimet aiheuttavat orgaanisten molekyylien, kuten rasvojen ja väriaineiden, hapettumisen.

- Alkometreissä: yksinkertainen kertakäyttöinen alkometri koostuu kirkkaasta putkesta, joka sisältää rikkihapolla kostutettua kalium- ja piidioksidikromaattisuolan vesiliuosta; sekoitettu oranssiin väriin. Tämä suola, joka on kosketuksissa rattijuopumuksen kuljettajan hengityksessä olevan alkoholihöyryn kanssa, reagoi muuttamalla värin vihreäksi. Tämä tarkoittaa, että etanoli (alkoholi) hapetaan etanaaliksi.

Kirjailija: Jennifer Fogaça
Valmistunut kemian alalta
Haluatko viitata tähän tekstiin koulussa tai akateemisessa työssä? Katso:
FOGAÇA, Jennifer Rocha Vargas. "Pelkistimen ja hapettavan aineen käsite ja esimerkkejä"; Brasilian koulu. Saatavilla: https://brasilescola.uol.com.br/quimica/conceito-exemplos-agente-redutor-agente-oxidante.htm. Pääsy 28. kesäkuuta 2021.
Kemia

Ilmakehän korroosionkestävä teräs, kromi, nikkeli, valmistettu valuraudasta masuunissa, kestävyys korkean lämpötilan hapetus, Ruostumaton teräs, hapettumista ja korroosiota kestävä rautaseosten ryhmä, osien valmistus ajoneuvolle
Kemia

Alkometrin toiminta, alkoholipitoisuus, alkometri, etyylialkoholiin liittyvät reaktiot, alkoholityypit alkometrit, kaliumdikromaatti, polttokenno, katalyytti, elektronien vapautuminen, etikkahappo, vety, conce
Kemia

Valoherkät linssit, hapetus-pelkistysreaktiot, elektronien menetys tai voitto, fotosynteettiset linssit aurinkolasissa, valokromaattisen lasin koostumus, tetraedriset happiatomit, hopeakloridin kiteinen rakenne, ultraviolettivalo, hopeametalli