THEosmoos ja lahusti läbipääs, vähem kontsentreeritud lahusest kontsentreerituma lahuseni, läbi a poolläbilaskev membraankuni lahuse membraanile avaldatav rõhk takistab lahusti läbipääsu. See protsess on mõeldud tasakaalustada lahuse kontsentratsioon.
Loe ka: Lahustatud aine ja lahusti
osmootne rõhk
THE osmootne rõhk ja suurema kontsentratsiooniga lahusele avaldatav rõhk nii et osmoosi ei toimuks, st et lahusti ei läbiks poolläbilaskvat membraani.
Osmootset rõhku kasutatakse vee magestamine, sundides protsessi pöördosmoos, põhjustades lahusti ülemineku kontsentreeritumast lahusest vähem kontsentreeritud lahusesse. Me nimetame seda protsessi pöördosmoos. Vaadake järgmist pilti, milles võrreldakse kahte protsessi:
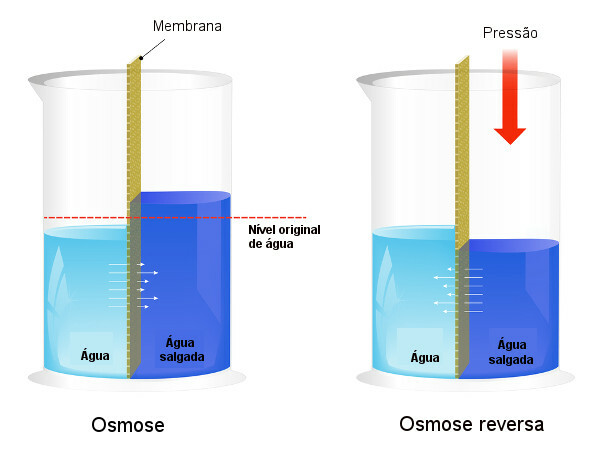
Pange tähele, et osmoosi korral kulgeb lahusti kõige kontsentreerituma lahuse suunas ja pöördosmoosi korral on läbiviik rakendatud rõhu tõttu vastupidises suunas. Teema kohta lisateabe saamiseks lugege meie teksti: osmootne rõhk.
rohkem teada: Pöördosmoos merevee magestamisel
Ärge lõpetage kohe... Peale reklaami on veel;)
osmootse rõhu võrrand
Osmootne rõhk, mida tähistab täht pi (π) lahuse, saab arvutada järgmise võrrandi abil:
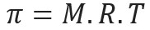
M = kontsentratsioon mol / l
R = täiuslike gaaside universaalne konstant
T = absoluutne temperatuur K-des
nagu teisedki kolligatiivsed omadused, osmootne rõhk sõltub lahuse kontsentratsioonsee tähendab, et mida suurem on lahuse kontsentratsioon, seda suurem on osmoosi mõju lahustele ja seetõttu ka suurem osmootne rõhk.
Näited
Osmoos ilmneb meie igapäevaelus erinevatel aegadel. Võime tuua näite liha soolamise protsess sinu juurde kaitse. Sina mikroorganismid mis põhjustaks liha degradeerumist kaotada vettseest väljapoole, mis sisaldab soola kontsentratsiooni, muutes toidu kauemaks.
Soola tõttu juhtub ka seda, et salati lehed närbuvad vee kaotamise eest nende seestpoolt rakke (selline vähem kontsentreeritud) karastatud lahendus väliskeskkonnas.
Osmoos on oluline ka siis, kui me räägime veri inimlik. Me ütleme, et Punased rakud ja veri on üks isotooniline keskkondsee tähendab, et neil on sama osmootne rõhk, mis võimaldab rakust vee sisenemist ja väljumist hõlpsalt.
Kui veri muutub vähem kontsentreerituks kui punaste vereliblede sees (hüpotooniline keskkond), toimub vee läbimine raku sees kergemini, muutes selle paisuda kuni lõhkemiseni. Kui vere kontsentratsioon ületab punaliblede (hüpertoonilise keskkonna) kontsentratsiooni, siis vererakud närtsivad, kuna nad kaotavad vett.

Liha säilitamise sama põhimõtte kohaselt puuviljade säilitaminekommikompottides, kes säilitavad toitu tänu kõrge suhkru kontsentratsioon lahuses.
Järgnevad on muud näited osmoosi tekkimise kohta:
- mahla tõusmisel taime juhtivates anumates;
- kell hemodialüüs;
- toitainete selektiivses liikumises inimkeha rakkudes.
Et mõista, kuidas osmoos loomarakus, taimerakus ja muudes bioloogilistes küsimustes toimub, lugege järgmist: Osmoos: mis see on ja kuidas see toimub looma- ja taimerakus.
Autor Victor Ferreira
Keemiaõpetaja
Kas soovite sellele tekstile viidata koolis või akadeemilises töös? Vaata:
FERREIRA, Victor Ricardo. "Osmoos"; Brasiilia kool. Saadaval: https://brasilescola.uol.com.br/quimica/osmose.htm. Juurdepääs 28. juunil 2021.



