O sulamis- ja keemistemperatuur on vastavalt temperatuurid, mille juures materjalid muutuvad tahkest vedelaks ja vedelaks. gaasi jaoks või maksimaalne temperatuur, mille juures vedelik võib antud füüsikalises olekus püsida surve.
Perioodilisustabeli keemiliste elementide sulamis- ja keemistemperatuurid varieeruvad vastavalt nende aatomnumbrile, mis tähendab siis, et need on perioodilised omadused.
Perioodilises tabelis järgitakse keemiliste elementide sulamis- ja keemistemperatuuride kasvu järjekorda järgmise nooleskeemiga:
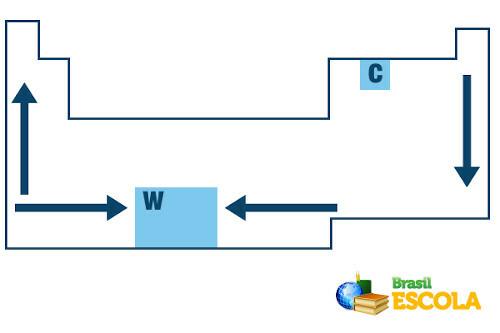
Sulamis- ja keemistemperatuuri kasv perioodilises tabelis
Pange tähele, et kui arvestada tabeli vasakul küljel samasse perekonda kuuluvaid elemente, siis sulamis- ja keemistemperatuurid vähenevad, kui elemendi aatomnumber suureneb, see tähendab altpoolt üles. Seda võib näha allpool toodud perekonna 1 elementide sulamis- ja keemistemperatuuri juures 1 atm juures:

1. perekonna elementide sulamis- ja keemistemperatuurid
Perioodilise tabeli paremal küljel toimub vastupidine, samasse perekonda kuuluvate elementide sulamis- ja keemistemperatuuri kasvusuund suureneb ülevalt alla. Seetõttu asuvad madalaima sulamis- ja keemistemperatuuriga elemendid tabeli ülaosas. Ainus erand on süsinik, mille sulamistemperatuur on 3550 ° C ja keemistemperatuur 4287 ° C.
Ärge lõpetage kohe... Peale reklaami on veel;)
Vastasel juhul on enamasti madala sulamis- ja keemistemperatuuriga gaasid või vedelikud toatemperatuuril merepinnal. Nagu ka väärisgaasid, lämmastik, hapnik, fluor ja kloor, mis asuvad tabeli paremas ülanurgas.
Nüüd, kui tegemist on samasse perioodi kuuluvate elementidega (tabeli sama rida), näeme, et sulamis- ja keemistemperatuurid tõusevad külgedelt tabeli keskosani. Vaadake teise perioodi elementide näidet:
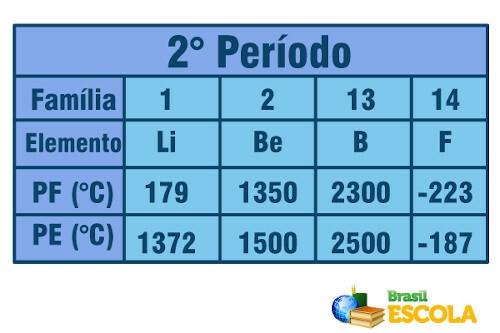
Perioodilisustabeli teise perioodi elementide sulamistemperatuur ja keemistemperatuur
Volfram (W) on element, mis asub perioodilise tabeli keskel ja mille sulamistemperatuur on metallide seas kõrgeim, olles võrdne 3422ºC. Sellepärast kasutatakse seda hõõglampide hõõgniitides, kuna see talub kõrgeid temperatuure sulamata.
Autor Jennifer Fogaça
Lõpetanud keemia
Kas soovite sellele tekstile viidata koolis või akadeemilises töös? Vaata:
FOGAÇA, Jennifer Rocha Vargas. "Sulamis- ja keemistemperatuur - perioodilised omadused"; Brasiilia kool. Saadaval: https://brasilescola.uol.com.br/quimica/ponto-fusao-ebulicaopropriedades-periodicas.htm. Juurdepääs 27. juunil 2021.