THE auto-oksi-redutseerimine või ebaproportsionaalne reaktsioon on redoksreaktsiooni tüüp, milles toimub sama keemiline element oksüdeerumine ja vähendamine. Vaatame kahte sellist tüüpi reaktsiooni näidet ja kuidas neid redoksmeetodi abil tasakaalustada:
1. näide:
JUURES2- + H+ → EI3- + NO + H2O
- Kõigi reaktsioonis osalevate aatomite ja ioonide oksüdatsiooninumbrite (NOX) arvutamise abil on võimalik kontrollida, kes oksüdeerisid ja kes reageerisid:
+3 -2 +1 +5 -2 +2 -2 +1 -2
JUURES2- + H+ → EI3- + NO + H2O
- Pange tähele, et lämmastik oli liik, mis nii reageeris kui ka oksüdeerus:
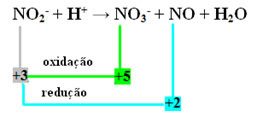
- Selle reaktsiooni tasakaalustamiseks redoksiga peame seostama NOX toodete, mitte reagentidega:
JUURES3- = ∆Nox = 5 - 3 = 2
NO = ∆Nox = 3 - 2 = 1
- ∆NOX koefitsientide ümberpööramisel on meil:
JUURES3- = ONOKS = 2 → 2 on NO koefitsient
EI = ONOKSI = 1→ 1 on NO koefitsient3-
JUURES2- + H+ → 1 JUURES3- + 2 NO + H2O
- Seega teame juba, et tootes on 3 N, seega NO koefitsient2- saab olema 3:
3 EI2- + H+ → 1 EI3- + 2 NO + H2O
- H koefitsientide määramiseks + ja H-st2O, pidage meeles, et vastuvõetud elektronide arv võrdub sama annetatud elektronide arvuga; seega võrdub reaktiivi laeng toote laenguga. Sel viisil saame koostada järgmise skeemi:
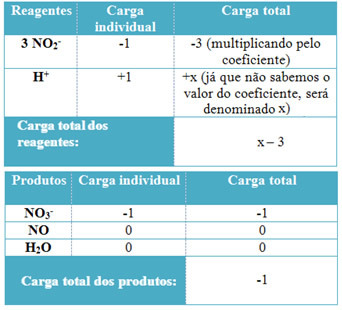
Selle teabe põhjal on meil reagentide kogulaeng võrdne x - 3 ja toode on võrdne -1. Nagu öeldud, peavad nende kahe tasud olema võrdsed. Kuna meil on toodete kogukoormus juba olemas, saame teha lihtsa arvutuse, et teada saada, milline on x väärtus:
x -3 = -1
x = -1 +3
x = 2
Seega on koefitsient H+ on 2 ja sellest tulenevalt ka H2See saab olema 1:
3 EI2- + 2 H+ → 1 EI3- + 2 NO + 1 H2O
2. näide:
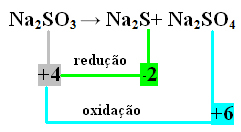
Sel juhul läbis reduktsiooni ja oksüdeerumise üheaegselt just S. Seega, nagu varem tehtud, saame seostada NOX-i toodetega ja pöörata nende väärtused, määrates neile koefitsiendid:
Kell2 S = ∆Nox = 4 - (-2) = 6 → 6 on Na koefitsient2 AINULT4
Kell2 AINULT4= ∆Nox = 6 - 4 = 2 → 2 on Na koefitsient2 s
Kell2 AINULT3→ 2 Kell2 Y + 6 Kell2 AINULT4
Kuna 2. jäsemes on 8 väävlit, on Na koefitsient2 AINULT3 saab 8:
8 sisse2 AINULT3→ 2 tolli2 S + 6 tolli2 AINULT4
Autor Jennifer Fogaça
Lõpetanud keemia
Allikas: Brasiilia kool - https://brasilescola.uol.com.br/quimica/reacoes-auto-oxirreducao.htm
