kahekordne sool on ühele klassifikatsioonile antud nimi, mis anorgaanilised soolad saavad vastu võtta. Muud liigitused on: lihtsad, maarja, hüdroksüülitud, hüdrogeenitud ja hüdreeritud. Anorgaanilisel soolal peab olema topeltsoola iseloomustus üks järgmistest kombinatsioonidest:
Katioon (Y) ja mis tahes kaks aniooni (X ja W) ning neid tähistab järgmine valem:
YXW
Anioon (X) ja mis tahes kaks katiooni (Y ja Z) ning neid tähistab järgmine valem:
YZX
Märge: Need soolad tekivad siis, kui a neutraliseerimisreaktsioon toimub kahe vahel alused erinev ja üks hapevõi kahe erineva happe ja aluse vahel.
Topeltsoola nimetamise reegel
Kui nimetada a kahekordne sool, on kõigepealt vaja teada selle põhiseadust, sest iga topeltsoola tüübi jaoks on olemas konkreetne nomenklatuuri reegel, nagu allpool näha:
a) Nomenklatuuri reegel kahe katiooniga kahekordse soola jaoks
Kui üks kahekordne sool on kaks katiooni, peame kasutama järgmist reeglit:

Nomenklatuuri reegel, mida kasutatakse kahe katiooniga topeltsoolade puhul
Järgnevalt on toodud kaks nime-reegli rakendamise näidet:
1. näide: Rida4s
See sool koosneb:
Anioon: sulfiid (S-2);
Rohkem elektropositiivset katiooni: liitium (Li+1);
Vähem elektropositiivset katiooni: ammoonium (NH4+1).
Seega on selle nimi liitium (topelt) ammoonium sulfiid.
2. näide: RbCaBO3
See sool koosneb:
Anioon: boraat (BO3-3);
Rohkem elektropositiivset katiooni: rubiidium (Rb+1);
Vähem elektropositiivset katiooni: kaltsium (Ca+2).
Seega on selle nimi rubiidiumi ja kaltsiumi boraat (topelt).
b) Nomenklatuuri reegel kahe aniooniga kahekordse soola jaoks
Kui üks kahekordne sool on kaks aniooni, peame kasutama järgmist reeglit:
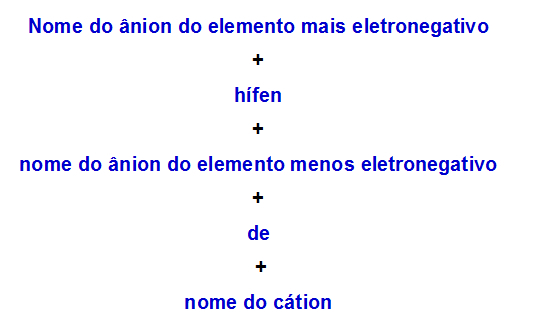
Nomenklatuuri reegel, mida kasutatakse kahe aniooniga topeltsoolade puhul
Siin on kaks näidet selle reegli rakendamiseks:
1. näide: MgFI
See sool koosneb:
Katioon: magneesium (Mg+2);
Enamik elektronegatiivseid anioone: fluoriid (F-1);
Vähem elektronegatiivset aniooni: jodiid (I-1).
Seetõttu on selle nimi magneesiumfluoriid-jodiid.
2. näide: ZnNO2br
See sool koosneb:
Katioon: tsink (Zn+2);
Rohkem elektronegatiivseid anioone: nitrit (NO2-1);
Vähem elektronegatiivset aniooni: bromiid (Br-1).
Seega on selle nimi tsinknitritbromiid.
Topeltsoola valemi kokkupanek selle nomenklatuurist
a) Kahe katiooniga kahekordse soola jaoks
Valemi konstrueerimine a kahekordne sool see sõltub selle nime teadmisest, mis on standardiseeritud nagu kogu soola puhul, see tähendab kõigepealt katiooni ja seejärel aniooni. Kuna topeltsoolal võib olla kaks katiooni, järgivad nende järjestus ja paigutus valemis antud nime.
1. näide: baarium-nikkel-pürofosfaat II
See sool sisaldab fosfaati (P2O7), baarium (Ba+2) ja nikkel II (Ni+2), selles järjestuses kirjutatud katioonid. Nii et selle valem on BaNiP2O7.
2. näide: vask II fosfaat ja kuld I
See sool sisaldab fosfaati (PO4-3), vask II (Cu+2) ja kuld I (Au+1), selles järjestuses kirjutatud katioonid. Seetõttu on selle valemiks CuAuPO4.
b) Kahe aniooniga topeltsoola jaoks
Juhul kui kahekordne sool kahe aniooniga järgime anioonide valemisse paigutamisel ka järjekorda, nagu need esinevad eesnimes.
1. näide: niklisulfaat-jodiid III
Sellel soolal on sulfaatioonid (SO4-2) ja jodiidi (I-1), ja selles nikkel III katioon (Ni+3). Nii et selle valem on NiSO4Mina
2. näide: plii tsüaniidfosfaat IV
Sellel soolal on fosfaatioonid (PO4-3) ja tsüaniid (CN-1), mis on kirjutatud selles järjestuses, ja pliikatioon IV (Pb+4). Nii et selle valem on PbPO4CN.
Minu poolt. Diogo Lopes Dias
Allikas: Brasiilia kool - https://brasilescola.uol.com.br/o-que-e/quimica/o-que-e-um-sal-duplo.htm
