keemiline element fosfor (P) kuulub perioodilise tabeli kolmandasse perioodi ja lämmastiku (VA) perekonda. Sel põhjusel moodustavad selle aatomid tavaliselt kolm keemilised sidemed jõudmiseks okteti teooria (stabiilsus). Siiski on mõningaid olukordi, kus fosfori aatom loob rohkem kui kolm sidet, see on võimalik ainult läbi hübridisatsiooni nähtus.
Et mõista fosfori hübridiseerimine, peame kõigepealt mõistma, miks selle elemendi aatom seob kolm sidet. Selleks peame lihtsalt jälgima teie elektroonilist levitamist:

Elektrooniline fosfori levitamine
Me võime täheldada, et valentsikihis on fosfori aatomil täielik 3s alamtase (koos kaks elektroni) ja mittetäielik 3p alamtase (kõigil kolmel alataseme orbitaalil on a elektron). Allpool on elektronide jaotumine alataseme orbitaalides Fosfori valentsikiht:
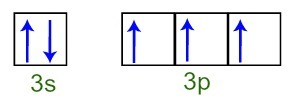
Fosfori aatomi valentskesta elektronide kujutamine
Kuna kõik 3p alataseme orbitaalid on puudulikud, on fosfori aatom võimeline looma kolm keemilist sidet, saavutades seeläbi stabiilsuse.
Kui nüüd vaadata ainet PCl
5näiteks oleme kindlad, et selles molekulis läbis fosfor hübridiseerimise, kuna see tegi viis ühendust. Kuna VIIA perekonda kuuluv kloor vajab stabiilseks sidet ja molekulil on sellest viis aatomit element, peavad kõik neist looma sideme, mis muudab fosfori aatomi omakorda ka viieks Ühendused. See on võimalik ainult läbi fosfori hübridiseerimine (mittetäielike aatomorbitaalide liitumine).Väliskeskkonnast energiat saades ergastuvad fosfori aatomi elektronid. Varsti pärast seda liigub üks kahest 3s alamtasandisse kuuluvast elektronist d alatasemel olevale tühjale orbitaalile, millel seni pole ühtegi elektroni. Vaadake allolevat skeemi:
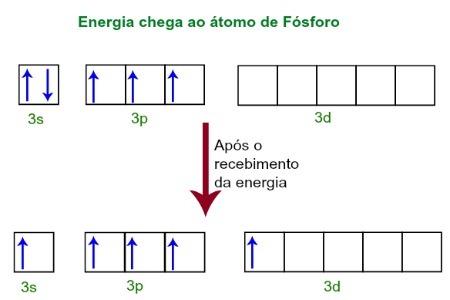
Energia vastuvõtmisel ergastuvad fosfori elektronid ja üks hõivab orbitaali d alatasemest.
Sel hetkel on fosfori valentsikihis orbitaal, kolm p orbitaali ja mittetäielik orbitaal.Lõppkokkuvõttes need viis orbitaali hübridiseeruvad, see tähendab, et nad ühinevad, mille tulemuseks on viis mittetäielikku aatomi orbitaali, mis on nüüd võimelised moodustama viis keemilist sidet.

Fosfori mittetäielike aatomorbitaalide hübriidimine
Kui orbitaal, kolm p orbitaali ja d orbitaali ühendati, on fosfori hübridisatsioon seda tüüpi sp3d.
Minu poolt. Diogo Lopes Dias
Allikas: Brasiilia kool - https://brasilescola.uol.com.br/quimica/hibridizacao-fosforo.htm