O titaan on keemiline element sümboliga Ti ja aatomnumbriga, st prootonite arv on võrdne 22-ga. See metall asub perioodilisuse tabeli 4. ja 4. rühmas.
Elemendi aatommass on 47,867 u ja kuna selle aatomi elektronides on 22 elektroni, on selle elektronide jaotus 1 s2 2s2 2p6 3s2 3p6 4s2 3d2.
Titaanil on paljude rakenduste jaoks soovitavad omadused, kuna see on sama tugev kui teras ja palju kergem.
Kuna see on plastiline, tulekindel ja korrosioonikindel metall, on sellel mehaaniline vastupidavus, termiline stabiilsus ja madal reaktsioonivõime, lisatakse see metallisulamitele nii, et neil oleks kõrge esitus. Selle biosobivus ja mittetoksilisus muudavad selle kasulikuks ka luuproteeside valmistamisel.
Titaani peamised omadused on järgmised:
- Sulamistemperatuur: 1668 °C
- Keemistemperatuur: 3287 °C
- Tihedus: 4,5 g/cm3
- Värvus: hõbehall
- Füüsikaline olek 20 °C juures: tahke
- Isotoobid: Ti46, sina47, sina48, sina49 ja sina50
Selle keemilise elemendi avastas 1791. aastal inglane William Gregor ja selle nimi tulenes kreeka keelest. titaanid, omistas hiljem Martin Heinrich Klaproth.
Titaan on planeedi arvukuse poolest üheksas element ja seda leidub maakoores maakides nagu rutiil (TiO2) ja ilmeniit (FeTiO3). Seetõttu on kaevandamine selle metalli saamise peamine meetod.
Milleks titaani kasutatakse?
Kuna titaan on toatemperatuuril keemiliselt mittereaktiivne, kergesti vormitav, kõrge mehaanilise ja korrosioonikindlusega, kasutatakse titaani strateegilise metallina.
Lennundus- ja kosmosetööstus on titaani peamised kasutajad osade, näiteks turbiini- ja kerekomponentide tootmiseks. Muud rakendused on hambaproteeside, kirurgiliste implantaatide ja ehete tootmine.
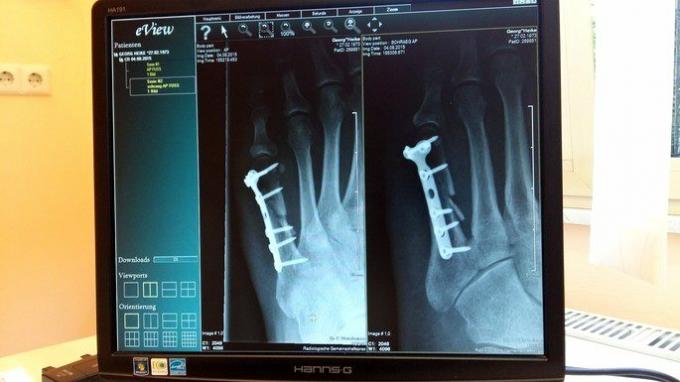
Meditsiinis on titaan väga kasulik oma kokkusobivuse tõttu inimese kudedega, kerguse ja tugevuse tõttu. Seda kasutatakse kehaosade implantaatide tootmiseks, nagu kinnituskruvid, põlveliigese proteesid, õlavarreluu proteesid, puusaproteesid jne.
Titaandioksiid (TiO2) on selle elemendi üks peamisi ühendeid, mida kasutatakse pleegitusainena. Üldiselt kasutavad kvaliteetsed valged tindid seda värvi ja läike visuaalse välimuse parandamiseks. Pigmenti kasutavad ka teised tooted, näiteks hambapastad ja päikesekaitsekreemid. Seda kasutatakse ka toiduvärvina, mida lisatakse piimatoodetele, maiustustele ja jookidele.
Arhitektuuris võime näha titaani kasutamist kõverate struktuuride katmiseks Guggenheimi muuseumis Bilbaos, Põhja-Hispaanias.

Igapäevaelus leiame arvukalt tooteid, mille koostises on titaan, näiteks jalgrattaraamid, prillid ja tennisereketid.
Keemiatööstuses kasutatakse titaani reaktsioonide katalüsaatorina. Nii on võimalik kontrollida reaktsioonikiirust ja vähendada toote moodustumise aega, ilma et see mõjutaks ainete koostist.
Autotööstus on uurinud titaani kasutamist autode valmistamisel, et vähendada nende massi ja seega vähendada kütusekulu ja suurendada nende kiirendust.
Hankige sisuga rohkem teadmisi:
- Keemilised elemendid
- Perioodilisustabel
- Mis on metallid?
Bibliograafilised viited
ATKINS, P.W.; JONES, L. Keemia põhimõtted: tänapäeva elu ja keskkonna kahtluse alla seadmine. 3.ed. Porto Alegre: Bookman, 2006.
FELTRE, R. Keemia alused: kd. vallaline. 4. väljaanne Sao Paulo: Moderna, 2005.
Lee, J. D. Mitte nii ülevaatlik anorgaaniline keemia. Tõlge 5. väljaandest. Inglise. Kirjastaja Edgard Blucher Ltd. 1999.