O aktiinium, sümbol Ac ja aatomnumber 89, on element, mis kuulub plokki f Perioodilisustabel, nn sisemised üleminekuelemendid. Keemiliselt sarnaneb see lantaaniga (nii näiteks on selle laeng ühendites +3), kuid raskesti kättesaadav ja väheste rakendustega. Selle elemendi ligikaudu 30 isotoobist on ainult kaks looduslikku, aktiinium-227 ja aktiinium-228.
Aktiiniumi saab kõige paremini kätte tuumade pommitamise teel raadio (Ra) termiliste neutronitega – tehnika, mis võimaldab seda saavutada milligrammivahemikus. Selle rakendused on endiselt piiratud, kuid on teada, et see saab kasutada energiaallikana kosmoselaevade ja kaugetes piirkondades töötavate seadmete jaoks on aktiinium-225 potentsiaalne kandidaat teatud tüüpi vähi raviks.
Loe ka:Tseesium-137 — radioaktiivne isotoop, mis põhjustas kiirgusõnnetuse Goiânias
Kokkuvõte aktiiniumi kohta
See on perioodilise tabeli f-plokki kuuluv metall.
Metallilisel kujul on see hõbevalge värvusega, mõnikord kuldse säraga.
Lahuses, arvestades selle sarnasust lantaaniga, on selle NOx é +3.
Sellel on umbes 30 isotoopi, millest ainult kaks leidub looduses: mass 227 ja 228.
Seda esineb proovides uraan, kuid see saadakse raadioisotoopide pommitamisel termiliste neutronitega.
Seda on raske hankida ja sellel on vähe rakendusi.
Siiski paistab silma aktiinium-225 isotoobi roll võitluses teatud tüüpi vähiga.
aktiiniumi omadused
Sümbol: ac
aatomnumber: 89
aatommass: 227 c.u.
elektronegatiivsus: 1,1
Ühinemispunkt: 1050 °C
Keemispunktst°: 3198 °C
TihedusKaal: 10,07 g.cm-3 (arvutatud)
elektrooniline konfiguratsioon: [Rn] 7 s2 6d1
keemiline seeria: aktiniidid, f-plokk, sisemised üleminekuelemendid
aktiiniumi omadused
aktiinium, aatomnumber 89 ja sümbol Ac, see on metallist kuuluv aktiniidide rühma, mis asub perioodilise tabeli f-plokis. Metallilisel kujul on see hõbevalge värvusega, mõnikord kuldse tooniga.
Keemiliselt aktiinium meenutab väga lantaani, võib öelda, et kvalitatiivselt nende kahe vahel erinevusi pole. Seetõttu on aktiiniumi laeng lahuses ja ühendite moodustumisel +3 (Ac3+). Õhuga kokkupuutel oksüdeerub see kiiresti ja moodustab vahelduvvoolukihi.2O3, mis takistab selle jätkamist oksüdatsioon.
Tuntud aktiiniumi ühendeid on vähe, nende hulgas halogeniidid, oksühalogeniidid, oksiidid ja sulfiidid. Oodata on ka teisi, nagu karbonaadi puhul, kuid neid pole veel tuvastatud.
Teada on umbes 30 aktiiniumi isotoopi, mis on ainult kaks loomulikku: 227acc 228B.C. Esimene, tuntuim, pärineb radioaktiivse lagunemise seeriast 235U ja on aega pool elu 21,77 aastat. Aktiinium-228, mille poolestusaeg on 6,15 tundi, on toorium-232 radioaktiivse lagunemise seeria saadus.
Loe ka:Radioaktiivne lagunemine - nähtus, mille käigus aatom muutub uueks tuumaks
Kust võib aktiiniumi leida?
Aktiinium (täpsemalt kujul 227B.C) sõltub otseselt uraan-235 kogusest, jaotunud hästi kogu maakoores. Keskmine uraanisisaldus maakoores on 2,7 ppm (osa miljoni kohta ehk mg/kg), kusjuures 0,72% massist vastab 235U. See võimaldab arvutada loodusliku arvukuse 227Ac (põhineb uraani ja isotoobi enda poolestusajal), mis oleks 5,7 x 10-10 ppm.
Aktiiniumi saamine
Kuigi seda leidub uraanimaakides, oli sellest looduslikust allikast saadud maksimaalne aktiiniumi kogus ligikaudu 7 μg (mikrogrammi, 10-6 grammi).
Parim viis selle hankimiseks oli 1940. aastate lõpus, kui teadlased suutsid hankida 227B.C kiiritamise kaudu 226Ra termiliste neutronitega.

Selle tehnikaga saadi Ac milligrammides koguses.
aktiiniumirakendused
Energia viiest osakesest alfa mis tekivad radioaktiivse lagunemise seeria käigus 227Ac lubas seda kasutada a soojusallikas radioisotoopide termoelektrilistes generaatorites. Energiat toodetakse kosmoselaevade või muude seadmete jaoks, mis pidid kaugetes kohtades pikka aega töötama.
juba 225Ac, mille poolestusaeg on 10 päeva, on alfa-kiirgust kiirgav radioisotoop, millel on huvitavad omadused vähirakkude kiireks hävitamiseks. Märkimisväärne energia eraldub lagunemisel 225ac, mis genereerib neli alfaosakest, saab kasutada kirurgias vähkkasvajate ründamiseks eesnääre, rinna- ja luuüdi. Veel üks huvitav punkt on see, et aktiinium-225 lagunemisseeria lõpeb kell 209Bi, stabiilne ja mittetoksiline isotoop.
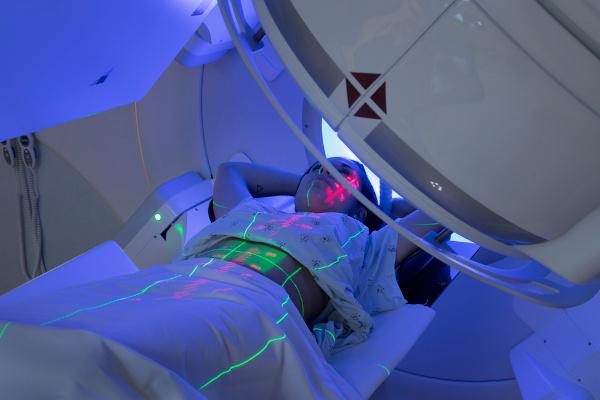
Kasutamise väljakutsed 225Ac on teiste mittemoodustamisel radioisotoobid, nagu potentsiaalselt ohtlikud 221Fr ja võimaldades aktiini isotoobil kasvaja sihtmärgil kauem toimida.
aktiiniumi ajalugu
1899. aastal Pierre'i laborites ja Marie Curie, André-Louis Debierne teatas, et leidis uue radioaktiivse elemendi, mis oleks keemiliselt lähedal titaan. Kuus kuud hiljem, aastal 1900, jõudis Debierne nii kaugele, et väitis, et titaani fraktsioon ei ole enam eriti aktiivne ja et uus element, mida ta uuris, meenutab nüüd keemiliselt tooriumi.
Debierne väitis uue elemendi avastamist, ristides ta aktiiniumiks (kreeka keelest aktis, mis tähendab "kiirt"). Tol ajal André-Louis Debierne'i avastust ei kritiseeritud, kuid tänapäeval teadaoleva põhjal on ilmne, et 1899. aasta katsed ei olnud ei tootnud aktiiniumi, samas kui 1900. aastate katsed tekitasid radionukliidide segu, mis sisaldas võib-olla ka väiksema ulatusega aktiiniumi.
kuigi, 1902. aastal teatas Friedrich Oskar Giesel uuest "eralduvast" ainest (radioaktiivne aine) pigisegu lisandite hulgas (üks pigisegu maagi variantidest, uraanoksiid). Giesel suutis õigesti kindlaks teha selle uue aine mitmed keemilised omadused, sealhulgas oluline asjaolu, et see oli keemiliselt sarnane haruldaste muldmetallide tseeriumi rühmaga.
1903. aastal õnnestus teadlasel proov kontsentreerida nii, et lisandina oli ainult lantaan, tooriumi ei olnud võimalik tuvastada. Järgmisel aastal ristis Giesel uue elemendi emaniumiks, kuna see oli selgelt silmitsi uuega raadio element.
Debierne ründas jõuliselt Gieseli väiteid, kinnitades, et tegemist on sama ainega, mille ta oli avastanud ja millele pani nimeks aktiinium, kuigi ta ise teatas, et see on keemiliselt sarnane titaani ja tooriumiga.
Hiljem domineeris Debierne, mistõttu paljud ajaloolased pidasid teda elemendi 89 tõeliseks avastajaks, kuid võib-olla Curie paari mõju ja asjaolu, et Rutherford on teile krediiti andnud. Teised aga eelistavad jagada krediidi Debierne'i ja Gieseli vahel.
THE Aktiiniumi avastamine oli ühtlasi ka Curie'de töö jätk, kuid sellel pole kunagi olnud sama mõju kui äsja avastatud raadiumil (Ra). Erinevalt raadiumist ei olnud aktiiniumil sel ajal rakendust, lisaks oli see looduses äärmiselt haruldane ja raskesti kättesaadav.
Autor Stefano Araújo Novais
Keemia õpetaja

