O tsirkoonium, sümbol Zr, aatomnumber 40, on keemiline element, mis kuulub rühma 5 Perioodilisustabel. See paistab silma oma suure korrosioonikindluse ja hea termilise stabiilsuse poolest.
element on keemiliselt väga sarnane hafnium, ja seetõttu on igas looduslikus tsirkooniumiproovis väike hafniumisisaldus. Seda leidub maapõues ohtralt, selle sisaldus on palju suurem kui laialt kasutatavatel elementidel nagu vask, tsink ja plii.
Tsirkooniumil on laialdane rakendus tuumatööstuses, kuna selle madal neutronite neeldumine muudab selle suurepäraseks kattekihiks uraandioksiidi rikka kütuse jaoks. Lisaks, kuna seda peetakse mittetoksiliseks ja väga bioloogiliselt ühilduvaks, kasutatakse tsirkooniumi kirurgilistes proteesides ja implantaatides.
Loe ka: Uraan on energiatootmisel väga oluline element
Kokkuvõte tsirkooniumi kohta
Tsirkoonium on a metallist kuuluvad perioodilise tabeli 5. rühma.
Looduses esineb see alati väikese hafniumisisaldusega, kuna need elemendid on keemiliselt väga sarnased.
Peamised tsirkooniumimaagid on tsirkoniit ja baddeleyite.
Tsirkooniumi ja hafniumi eraldamine on väga keeruline.
Tsirkooniumil on hea korrosiooni- ja kõrge temperatuurikindlus.
Seda saab kasutada hambaimplantaatides ja muudes proteesides, kuna see on mittetoksiline ja sellel on kõrge biosobivus.
Suure osa tsirkooniumist kasutab tuumatööstus.
Selle elemendi avastas 1789. aastal saksa teadlane Martin Klaproth.
Tsirkooniumi omadused
Sümbol: Zr.
aatomnumber: 40.
aatommass: 91,224 c.m.u.
elektronegatiivsus: 1,33.
Ühinemispunktst°: 1855 °C.
Keemispunktst°: 4409 °C.
Tihedus: 6,52 g.cm-3 (temperatuuril 20 °C).
elektrooniline konfiguratsioon: [Kr] 5s2 4d2.
Keemia sari: rühm 4, siirdemetallid.
Ära nüüd lõpeta... Pärast kuulutust on rohkem ;)
Tsirkooniumi omadused
Tsirkoonium oma metallilisel kujul on a hallikas metall ja millel on hea korrosioonikindlus, peamiselt ZrO kihi tõttu2 mis moodustub selle ümber, kaitstes sisemist metallmassi. Peeneks jaotatud tsirkoonium on aga väga pürofooriline, st võib kokkupuutel õhuga spontaanselt süttida, eriti kõrgetel temperatuuridel.
Keemiliselt on tsirkoonium väga lähedane hafniumile, eriti seetõttu, et elemendid esinevad looduses koos. Seetõttu, nagu hafnium, tsirkoonium ei kannata keemiliste rünnakute all happed lahjendatud (välja arvatud HF), kui neid ei kuumutata. Aluselised lahused ei ole tsirkooniumi puhul kuigi tõhusad isegi kõrgematel temperatuuridel.
Kõrgema temperatuuriga süsteemides on tsirkooniumil võime reageerida enamikuga mittemetallid. Reageerimisel on näha, et kõige stabiilsemad on tsirkooniumiühendid oksüdatsiooninumbriga +4, nagu ka ZrO puhul2 või ZrCl4. Madalamad oksüdatsiooniastmed, näiteks +3, on vähem stabiilsed, mis erineb sellest titaan, grupi 4 kergeim element, millel on selle koormuse juures hea stabiilsus.
Kust leida tsirkooniumi?

Perioodilise tabeli d-ploki elementide hulgas on tsirkoonium sageduselt neljas, tagapool raud, titaanist ja mangaan. Need on olemas rohkem 30 maagid, mis mul onjam tsirkooniumi oma koostises. Tuntumad ja olulisemad on tsirkoniit (tuntud ka kui tsirkoon), ZrSiO4 ja baddeleiit (või baddeleiit), ZrO2. Baddeleyite leidub isegi Brasiilias.
Suurimate tsirkooniumivarudega riigid on Austraalia, Lõuna-Aafrika ja Mosambiik. Suurimad tootjad on aga Hiina, Prantsusmaa, India, Venemaa, Saksamaa ja USA.
Huvitaval kombel tsirkoonium Mõnes leidub seda ohtralt tähed. Element tuvastati isegi Päike ja meteoriitides. Apollo missioonide käigus saadud Kuu proovid osutusid suureks ZrO sisalduseks2 nendes kivimites võrreldes maapealsete kivimitega.
Vaata ka: Kuld — väärismetall, mis paistab silma hea elektrijuhtivuse poolest
Tsirkooniumi saamine
tsirkoonium esineb looduslikult koos hafniumiga, mille teise elemendi sisaldus on alati vahemikus 1 kuni 3 massiprotsenti. Vaatamata nende madalale sisaldusele on nende kahe eraldamine väga keeruline.
Tavaliselt kasutatakse tsirkooniumi ekstraheerimiseks Krolli protsessi. Selles protsessis ZrO2 maakides sisalduv muundatakse kõrgel temperatuuril ZrCl-ks4. Sel viisil saab tsirkooniumi saada, kasutades redutseerijana magneesiumi. Järgmised reaktsioonid näitavad protsessi.
ZrO2 → ZrCl4 (kasutades CCl4 temperatuuril 770 K)
ZrCl4 → Zr (kasutades Mg-d Ar atmosfääris temperatuuril 1420 K)
Suur keemiline sarnasus Zr ja Hf vahel tähendab aga seda, et hafnium jääb lõppsüsteemi püsiva lisandina. Seega on vaja metallurgiliste tehnikate kasutamine Zr ja Hf eraldamiseks. Tööstus arendab juba hüdrometallurgilisi (st vesilahusena esinevaid) ja pürometallurgilisi (ilma veeta) teid.
Hüdrometallurgiline tehnika on K-soolade fraktsionaalne kristallimine2ZrF6 ja K2HfF6, mille lahustuvus vees ei ole sama. Teine lahendusmeetod on lahustiga ekstraheerimine, mille käigus Zr- ja Hf-ühendid lahustatakse. vees ja seejärel ekstraheeritakse selektiivselt orgaaniliste lahustitega, nagu metüülisobutüülketoon ja austusavaldus. Arvestades eraldamise keerukust, turustatakse kaubanduslikku tsirkooniumi tavaliselt 1–3 massiprotsenti Hf-i sisaldusega.
tsirkooniumirakendused
Metallist tsirkoonium on aastal tööle võetud liigad, peamiselt terasest, et muuta need mehaanilise ja korrosioonikindluse osas paremaks. Seda võimaldab ka metalli stabiilsus kõrgel temperatuuril kasutatakse kosmoselaevadel, mis saavad Maa atmosfääri taassisenemisel tekkinud äärmuslike tingimuste tõttu palju kahju.
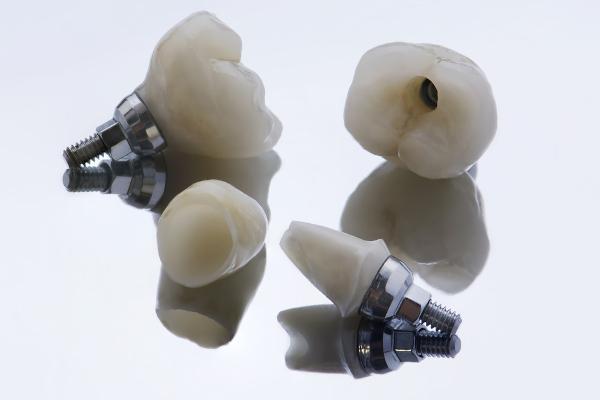
Kuna tsirkooniumi peetakse mittetoksiliseks ja väga korrosioonikindlaks elemendiks, siis lisaks heale biosobivusele Uuritakse ka kasutamist kirurgilistes rakendustes, nagu hambaproteeside ja implantaatide puhul.
Tsirkooniumdioksiid, ZrO2, on väga kõrge sulamistemperatuuriga, vahemikus 2500 °C. Seega kasutatakse seda kõrge kuumakindlusega konteinerite valmistamine, lisaks väga vastupidavale keraamikale. Sel põhjusel on seda keraamikat isegi lõikemasinates kasutatud. ZrO2 Seda saab kasutada ka kosmeetikas, higistamisvastastes ainetes, toiduainete pakendites ja isegi võltsitud vääriskivides.
Väärib märkimist, et suurt osa tsirkooniumist kasutab tuumatööstus. Seal on näiteks Z liigaircaloy®tsirkooniumi ja tina metallisulam, mis on välja töötatud eranditult tuumaeesmärkidel.
Tuumatööstuses on tsirkoonium kasutatakse pakendis, mis sisaldabêm uraanoksiid, kütust Elektrijaamad. Kuna see on väga veekindel ja vähese kinnipüüdmisega neutronid, osutub see selleks otstarbeks heaks materjaliks. Tasub meeles pidada, et ajal kasutatakse neutroneid lõhustumine, ja seetõttu on oluline, et tsirkoonium neid ei haaraks. Mittepüüdmine põhjustab ka seda, et tsirkoonium ei ilmu radioaktiivsus. Sellepärast ei saa tsirkooniumil sel juhul olla jälgi hafniumist, metallist, millel on suurepärane neutronite püüdmise võime.
Vaadake seda meie podcastist:Kuidas tuumaelektrijaamad töötavad?
tsirkooniumi ajalugu
Nimetus tsirkoonium tuleneb tõenäoliselt sellest sargon, sõna süüria keelest, mida kasutatakse vääriskivide värvide kirjeldamiseks, mida tänapäeval tuntakse tsirkooniumoksiidina. Kuigi mineraalid olid juba teada, ei teatud, et need sisaldasid uut elementi enne Martin Heirinch Klaprothil õnnestus 1789. aastal see element Berliinis tuvastada. Saksa teadlane otsustas elemendile nime anda tsirkhorn.
Aasta 1789 oli Klaprothi jaoks väga oluline, kuna samal aastal avastas teadlane elemendi uraani.
Lahendas harjutusi tsirkooniumil
küsimus 1
(FGV SP/2014 – kohandatud) Uus ja paljutõotav ülijuhtivate materjalide klass põhineb vanaadiumtsirkooniumdiboriidi ühendil. See ühend sünteesitakse tsirkooniumi (IV) soolast.
(Ajakiri Otsi Fapesp, juuni 2013. kohandatud)
Prootonite ja elektronide arv Zr-ioonis4+ on võrdne vastavalt:
A) 36; 40
B) 40; 40
C) 40; 44
D) 40; 36
E) 36; 36
Vasta
D täht
Nagu tsirkooniumil on aatomnumber võrdne 40, võime järeldada, et selle arv prootonid on samuti 40, sest aatomnumber on arvuliselt võrdne prootonite arvuga.
Esitades laengu, mis on võrdne +4, teame, et sellisel kujul on tsirkooniumil neli elektronid välja arvatud juhul, kui see on neutraalsel kujul.
Neutraalses seisundis võrdub prootonite arv elektronide arvuga, see tähendab, et algselt on tsirkooniumil 40 prootonit ja 40 elektroni. Kaotades neli elektroni, jääb tsirkooniumi alles vaid 36.
küsimus 2
(Uerj 2013 —kohandatud) Tsirkooniumdioksiid meenutab teemanti, süsiniku allotroopset vormi, mida saab asendada odavate ehetega.
Märkige alternatiiv, mis sisaldab tsirkooniumdioksiidi keemilist valemit, samuti selle aine aatomitevahelise sideme tüüp.
A) ZrO4, kovalentne.
B) ZrO2, iooniline.
C) ZrO2, kovalentne.
D) ZrO4, iooniline.
E) ZrO2, metallist.
Vasta
Täht B
Tsirkooniumdioksiid, nagu nimigi ütleb, peab sisaldama ainult kahte aatomit hapnikku. Seega on eeldatav valem ZrO2. Lisaks omandab tsirkoonium tavaliselt oksüdatsiooniastme, mis on võrdne +4.
Aatomitevahelise sideme tüüp on iooniline, kahel põhjusel:
tsirkoonium on metall ja hapnik on mittemetall;
erinevus elektronegatiivsus mõlema vahel on suurem kui 1,7 (3,5 – 1,3 = 2,2).
Autor Stefano Araújo Novais
Keemia õpetaja

