Puhverlahus see on homogeenne segu, mis ei muuda pH-d ega pOH-d, kui sellele segule lisada väikeses koguses tugevat hapet või tugevat alust. Kuid segu ei muuda pH-d ega pOH-d ainult siis, kui sellel on üks kahest alltoodud koostisest:
Pistik hape (pH alla 7):
Selles on nõrk hapet segatud a soola lahustuv, millel on sama anioon, nagu vesiniktsüaniidhape (HCN) ja kaaliumtsüaniid (KCN), millel on sama tsüaniidanioon (CN).
Põhipuhver (pH suurem kui 7):
Alus nõrgalt segatud soolaga, millel on sama katioon, nagu tsinkhüdroksiid [Zn(OH)2] ja tsinkkloriid (ZnCl2), millel on sama tsinkkatioon (Zn+2).
Selleks, et mõista puhverlahuse mõju tugeva happe või aluse vastuvõtmisele, on oluline meeles pidada, millal happeid ja aluseid peetakse tugevateks:
→ Aluste pingerida tugevuse järgi
tugev: alused keemiliste elementidega IA (leelismetallid) ja IIA (leelismuldmetallid) perekondadest, välja arvatud magneesium;
nõrk: alused, milles on element magneesium ja mõni muu, kui see ei kuulu IA ja IIA perekondadesse.
→ Klassifikatsioon hape tugevuseks
a) Hüdraatide jaoks (hapnikuvabad happed):
tugev: ainult HCl, HBr ja HI;
modereerib: ainult HF;
nõrk: mis tahes muu hüdroksiid.
b) Hapnikhapete (hapnikuga happed):
tugev: kui hapnikuaatomite arvu lahutamine vesinikuaatomite arvust on võrdne või suurem kui 2;
modereerib: kui hapnikude arvu lahutamine vesinikuaatomite arvust on võrdne 1-ga;
nõrk: kui hapnikude arvu lahutamine vesinikuaatomite arvust on 0 või väiksem.
Puhvrile tugeva aluse lisamise mõju
Selgitamiseks kasutame puhverlahus moodustub tsinkhüdroksiidist [Zn(OH)2] ja tsinkkloriidi lahustuv sool (ZnCl2), mis saab väikese koguse tugevat naatriumhüdroksiidi (NaOH) alust. Vaadake selle puhverlahuse saldosid:
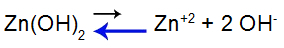
Aluse dissotsiatsiooni tasakaaluvõrrand
Tasakaal nihkub vasakule, kuna alus on nõrk.
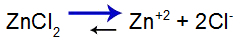
Soola dissotsiatsiooni tasakaaluvõrrand
Ära nüüd lõpeta... Peale reklaami on veel midagi ;)
Tasakaal nihkub paremale, sest sool on lahustuv.
Tugeval alusel on järgmine tasakaal:
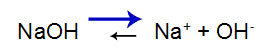
Aluse dissotsiatsiooni tasakaaluvõrrand
Tasakaal nihkub paremale, kuna alus on tugev.
Lisatud tugev alus vabastab hüdroksiidi aniooni (OH) vette-), millel on kõrge afiinsus tsingi katioonide (Zn+2) teises tasakaalus olevast soolast. Hüdroksiidi ja tsingi seos moodustab tsinkhüdroksiidi:
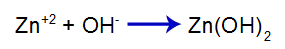
baasi moodustamise võrrand
Nii et OH- aluse sisaldus vähendab tsingi kogust teises tasakaalus ja suurendab aluse kogust [Zn(OH)2], põhjustades selle edasise dissotsieerumise ja Zn-katioonide vabastamise+2 esimeses tasakaalus. Kuna me ei muuda hüdroksiidi kogust söötmes, siis pH ei muutu.
Tugeva happe puhvrile lisamise mõju
Selgituseks kasutame tsinkhüdroksiidist moodustatud puhvrit [Zn(OH)2] ja tsinkkloriidi lahustuva soola (ZnCl2), mis saab väikese koguse vesinikjodiidhapet (HI), mis on tugev. Vaadake korgis olevaid saldosid:
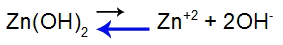
Aluse dissotsiatsiooni tasakaaluvõrrand
Tasakaal nihkus vasakule, kuna alus on nõrk.
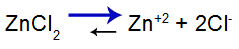
soola tasakaalu võrrand
Tasakaal nihkus paremale, kuna sool on lahustuv.
Tugeval happel on järgmine tasakaal:
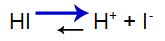
Happetasakaalu võrrand
Tasakaal nihkus paremale, kuna hape on tugev.
Lisatud hape tekitab vees hüdrooniumi katiooni (H+), millel on kõrge afiinsus hüdroksiidioonide (OH-) aluselt. Hüdrooniumi ja hüdroksiidi vaheline seos moodustab veemolekuli:
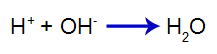
vee moodustumise võrrand
Nii et H+ hape vähendab hüdroksiidide hulka esimeses tasakaalus, suurendades aluse dissotsiatsiooni. Kuna me ei muuda hüdroksiidi kogust söötmes, siis pH ei muutu.
Mina. Diogo Lopes Dias
Kas soovite sellele tekstile viidata koolis või akadeemilises töös? Vaata:
PÄEVAD, Diogo Lopes. "Mis on puhverlahus?"; Brasiilia kool. Saadaval: https://brasilescola.uol.com.br/o-que-e/quimica/o-que-e-uma-solucao-tampao.htm. Sissepääs 27. juulil 2021.


