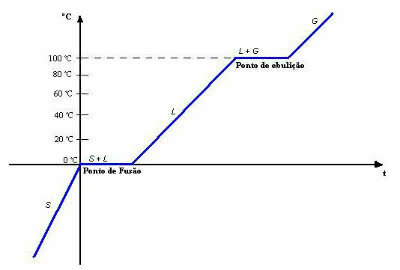
Sina aluselised oksiidid need on need, mis veega reageerides tekitavad aluseid. Kui nad reageerivad happega, moodustavad nad soola ja vett.
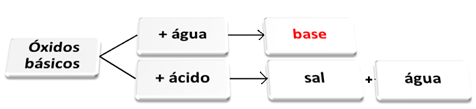
Aluselised oksiidid, mis reageerivad vee ja happega.
Näiteks on meil naatriumoksiid (Na2O), mis on aluseline oksiid. Vaata allpool, et veega reageerides moodustab see naatriumhüdroksiidi aluse:
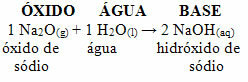
Kui see sama oksiid reageerib happega, näiteks väävelhappega (H2AINULT4), tekib sool (naatriumsulfaat) ja vesi.
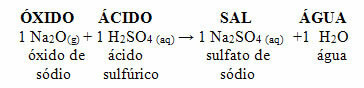
Kui aluseline oksiid reageerib happelise oksiidiga, tekib ka sool, kuid ilma veeta.
Nagu näidatud näites, on ka teised aluselised oksiidid ioonühendid, mis tekivad nendes peamiselt metallid, elemendid, mis on väga elektropositiivsed ja mille "laeng" on tavaliselt +1 või +2.
Näited:
Kell2O = Na1+
K2O = K1+
CaO = Ca2+
MgO = Mg2+
Nendel ühenditel on kõrge sulamis- ja keemistemperatuur ning kõik sisaldavad hapnikuaniooni (O2-).
Ära nüüd lõpeta... Peale reklaami on veel midagi ;)
Mõnede põhioksiidide rakendused:
• Koer: Kaltsiumoksiid
Seda ühendit tuntakse üldiselt kui
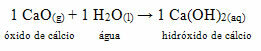

Valge värvimine.
• K2O: kaaliumoksiid
Kaaliumoksiidi leidub tavaliselt puidus ja sigaretituhas. Veega reageerides moodustab see kaaliumhüdroksiidi (KOH) baasi, mida kasutatakse seepide valmistamisel. Ka varem kasutati kohtades, kus KOH puudus, taimset tuhka, mis sisaldas K2O, et reageerida rasvadega ja toota nn "hall seep".
Autor Jennifer Fogaça
Lõpetanud keemia eriala
Kas soovite sellele tekstile viidata koolis või akadeemilises töös? Vaata:
FOGAÇA, Jennifer Rocha Vargas. "Aluselised oksiidid"; Brasiilia kool. Saadaval: https://brasilescola.uol.com.br/quimica/oxidos-basicos.htm. Sissepääs 27. juulil 2021.