Orgaanilisi ühendeid saab esitada mitmel viisil, näiteks lamestruktuurivalemi, lihtsustatud või lühendatud struktuurivalemi või kriipsvalemiga. Lihtsaim esitus on aga molekulaarvalemi kaudu.

Seega vaatame, kuidas määrata orgaaniliste ühendite molekulaarvalem teiste ülalnimetatud valemite põhjal.
1. Lameda struktuurivalemi kaudu:see valem näitab aatomite paigutust või paigutust molekulis. Näiteks allpool on ühe bensiinis sisalduva süsivesiniku lame struktuurvalem.

Pange tähele, et selles valemis on näidatud kõik aatomid ja kõik nendevahelised sidemed. Nüüd selle ühendi molekulaarvalemi määramiseks lugege lihtsalt iga elemendi aatomite arv ja asetage indeks kõnealuse elemendi alumisse parempoolsesse serva.
Oluline aspekt, mida tuleb esile tõsta, on see orgaaniliste ühendite molekulaarvalemit alustame alati elemendist süsinik, kuna see on nende ainete peamine koostisosa. Vaata näidet:
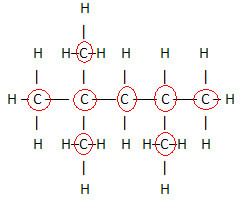
Kuna süsinikku on 8, alustame molekulaarvalemi kirjutamist järgmiselt: Ç8
Selle valemi täitmiseks loendame vesinike koguse:
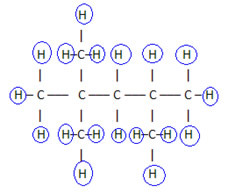
seega teie molekulaarne valem é Ç8H18.
2. Lihtsustatud või lühendatud struktuurvalemi kaudu: seda tüüpi valemis on vesinike kogus lühendatud. Näiteks vaadake sama valemit bensiinis leiduva molekuli jaoks, nüüd kondenseeritud kujul:
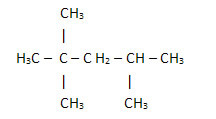
Nii on vesinike kogust veelgi lihtsam lugeda, piisab, kui liita indeksid (3 +3+ 3 +2 +1 +3 +3 = 18).
Kuid nüüd vaatame linoolhappe kondenseeritud struktuurivalemit, mida leidub köögiviljades nagu puuvill, sojaoad, päevalilled jne. ja mida kasutatakse värvides ja lakkides:
H3C─CH2CH2CH2CH2CH═CH─CH2CH═CH─CH2CH2CH2CH2CH2CH2CH2─COOH
Arvestades süsiniku, vesiniku ja hapniku kogust, saame järgmise molekulaarne valem linoolhape: Ç18H32O2.
3. Löögi valemi kaudu: see valem lihtsustab veelgi orgaaniliste ühendite esitamist, kuna jätab välja rühmad C, CH, CH2 ja CH3.
Näiteks on linoolmolekul, vaadake, kuidas see välja näeb:

Loendame kõigepealt süsiniku kogust, pidades meeles, et selles valemis on iga süsinikuvaheline side tähistatud kriipsuga. Seega vastavad tipud ja ka kaks pöördepunkti süsinikuaatomitele.
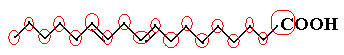
Nii et meil on: Ç18
Nüüd, et lugeda vesinike hulka, peame meeles pidama, et süsiniku ja vesiniku vahelised sidemed on eeldatud, kuna süsinik moodustab teadaolevalt neli sidet; seega on puuduvate sidemete hulk selle elemendiga seotud vesiniku hulk.
Vaadake allolevaid selgitusi:
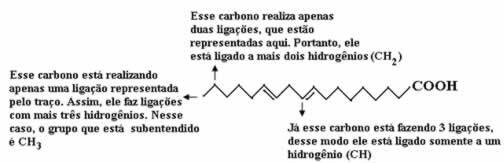
Seega on vesinike kogus: 32.

Hapniku kogust on üsna lihtne lugeda, kuna neid on ainult kaks. Alates molekulaarne valem é: Ç18H32O2.
Autor Jennifer Fogaça
Lõpetanud keemia eriala
Allikas: Brasiilia kool - https://brasilescola.uol.com.br/quimica/formulas-moleculares-compostos-organicos.htm

