Oksüdatsioon on nimetus, mis antakse elektronide kadumise protsessile aatomi, rühma või ioonliigi poolt a keemiline reaktsioon. Seda tuvastatakse suurenemise põhjal NOX liigi või aatomi (oksüdatsiooniarv) reagendi ja produkti võrdlemisel.
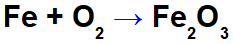
Raua oksüdatsiooni võrrand.
Näiteks ülaltoodud võrrandis võime näidata iga osaleja NOX-i:
Reaktiiv raud (Fe): sisaldab NOX 0, kuna see on a lihtne aine;
Hapnik reagendis (O): sisaldab NOX 0, kuna see on lihtne aine;
Tootes sisalduv hapnik: selles on NOX-2, kuna see ei ole seotud leelismetalliga, leelismuld või vesiniku moodustamine peroksiidid või superoksiidid;
Raud tootes: selles on NOX +3, kuna raua NOX korrutis 2-ga (aatomite arv) + hapniku NOX korrutis 3-ga peab andma tulemuseks 0, kuna tegemist on liitainega:
x.2 + 3.(-2) = 0
2x - 6 = 0
2x = +6
x = + 6
2
x = +3
Võrreldes reaktiivi raua NOX-i (0) tootega (+3), täheldasime tõusu, see tähendab, et see läbis protsessi oksüdatsioon. Väärib märkimist, et esinemine oksüdatsioon sellega kaasneb alati redutseerumisnähtus (mis tähendab elektronide võimendust), mida identifitseerib NOx vähenemine, nagu näiteks hapniku puhul.
Loe ka:Oksüdatsiooniarvu (NOX) määramine
Näited olukordadest, kus oksüdatsioon toimub:
1. Põlemine

Materjali põlemine viitab samuti oksüdatsioonile.
Põlemine on iga keemiline reaktsioon, mis toimub a juuresolekul kütust mis tahes ja oksüdeeriv gaas hapnik (O2), mille tulemuseks on soojuse ja valguse tootmine. Igas põlemisreaktsioonis toimub oksüdatsioon.
2. Mõned orgaanilised reaktsioonid
Igas orgaanilises reaktsioonis, mis toimub allpool loetletud vahendite juuresolekul, toimub protsess oksüdatsioon:
Kaaliumdikromaat (K2Kr2O7) või kaaliumpermanganaat (KMnO4);
Tugeva happe või tugeva aluse olemasolu;
Osoongaas (O3) metallilise tsingi (Zn) ja vee (H2O).
3. Patareid või patareid

Patareid on seadmed, milles oksüdeerumine toimub alati.
Virnad või patareid on elektrokeemilised seadmed, mis salvestavad keemilisi aineid. Üks neist ainetest oksüdeerub ja teine redutseerub, mille tulemusena tekib elektrivool.
4. Elektrolüüs
Elektrolüüs on keemiline protsess, mille käigus soola sisaldav vesilahus on allutatud elektrivoolule, mis soodustab nendes materjalides sisalduvate anioonide oksüdeerumist. Igas elektrolüüsis on oksüdatsioon.
Mina. Diogo Lopes Dias
Allikas: Brasiilia kool - https://brasilescola.uol.com.br/o-que-e/quimica/o-que-e-oxidacao.htm

