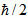Võib juhtuda, et on sama elemendi happeid ja sellel elemendil on sama oksüdatsiooninumber (NOX), kuid erinevus on hüdratsiooniastmetes.
Näiteks allpool on meil kolm hapet, mis on moodustatud elemendi fosforist (P):
H3TOLM4 H4P2O7 HPO3
Pange tähele, et kõigis kolmes happes on fosfori oksüdatsiooniarv +5; erinevus seisneb hüdratsiooniastmes.
Sellest lähtuvalt eristatakse neid happeid nomenklatuuris eesliidete kaudu orto, püro ja meta.
Kõige rohkem hüdreeritud hapet nimetatakse orto. Toodud näites esimene (H3TOLM4) kutsutakse hape ortofosfor, sest see on neist kolmest kõige hüdreeritum. Orto eesliide on kulutatav, nii et enamasti nimetatakse seda hapet lihtsalt fosforhappe.
Eesliiteid püro ja meta kasutatakse võrdluspunktina ortohappega:
- Pyrus: 2 orto molekuli miinus 1 H molekul2O
Näide: H4P2O7 kutsutakse hape pirofosfor kuna see on võrdne kahe ortofosforhappe molekuliga (H3TOLM4) miinus üks veemolekul.
2. H3TOLM4 = H6P2O8
H6P2O8 - H2O = H4P2O7
See protsess on a intermolekulaarne dehüdratsioon:
- Eesmärk: 1 orto molekul miinus 1 H molekul2O
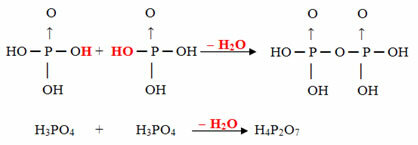
Näide: HPO3 kutsutakse hape eesmärkfosfor kuna see on võrdne ortofosforhappe molekuliga (H3TOLM4) miinus üks veemolekul.
H3TOLM4 - H2O = HPO3
See protsess on a intramolekulaarne dehüdratsioon:
Autor Jennifer Fogaça
Lõpetanud keemia
Allikas: Brasiilia kool - https://brasilescola.uol.com.br/quimica/grau-hidratacao-dos-acidos.htm