Keemiline tasakaal on üks aineid, mis Enemis ja sisseastumiseksamitel kõige enam langevad.
Pöörduvate reaktsioonide aspekte käsitletakse küsimustes ja kandidaate hinnatakse nii arvutuste kui ka seda teemat hõlmavate mõistete abil.
Seda silmas pidades koostasime selle küsimuste loetelu keemilise tasakaalu eri lähenemisviisidega.
Eksamiteks valmistumiseks kasutage resolutsiooni kommentaare ja vaadake üksikasjalikke juhiseid küsimuste lahendamiseks.
Keemilise tasakaalu üldised mõisted
1. (Uema) Võrrandis , pärast keemilise tasakaalu saavutamist võime järeldada tasakaalu konstanti
, mille kohta on õige öelda, et:
a) mida suurem on Kc väärtus, seda väiksem on otsese reaktsiooni saagis.
b) Kç olenemata temperatuurist.
c) kui edasi- ja pöördreaktsioonide kiirused on võrdsed, siis Kc = 0.
d) Kç see sõltub reaktiivide esialgsest molaarsusest.
e) mida suurem on Kc väärtus, seda suurem on toodete kontsentratsioon.
Õige vastus: e) mida suurem on Kc väärtus, seda suurem on toodete kontsentratsioon.
Otsest reaktsiooni tähistab number 1, kus:
Pöördreaktsiooni tähistab
K väärtusç see arvutatakse toodete ja reagentide kontsentratsioonide suhte järgi.
Lugeja (mis sisaldab tooteid) on otseselt proportsionaalne tasakaalukonstandiga. Seetõttu on suurem K väärtusç, seda suurem on otsese reaktsiooni saagis, kuna moodustub rohkem produkti ja järelikult on ka toodete kontsentratsioon suurem.
K väärtusç varieerub sõltuvalt temperatuurist, sest kui me selle väärtust muudame, võib endotermiline (soojuse neeldumine) või eksotermiline (soojust eraldav) reaktsioon olla eelistatud ja sellega saab tarbida või luua rohkem reagenti või toodet, muutes seeläbi kontsentratsioonist sõltuvat tasakaalu konstanti reaktiivid.
Kc sõltub komponentide molaarsetest kogustest tasakaalu saavutamisel ning siis, kui edasi- ja vastupidiste reaktsioonide kiirused on võrdsed.
2. (UFRN) Keemilist tasakaalu iseloomustab dünaamilisus mikroskoopilisel tasemel. Kvantitatiivse teabe saamiseks keemilise tasakaalu ulatuse kohta kasutatakse tasakaalu konstantset suurust. Mõelge järgmisele ribale:

Keemilise tasakaalu korral on tegelase idee tasakaalust:
a) See on õige, kuna keemilises tasakaalus on pool kogustest alati saadused ja teine pool reaktiive.
b) See ei ole õige, kuna keemilises tasakaalus võivad toodete ja reagentide kontsentratsioonid olla erinevad, kuid need on konstantsed.
c) See on õige, kuna keemilises tasakaalus on reagentide ja saaduste kontsentratsioonid alati ühesugused, kui välist mõju ei häiri tasakaalu.
d) See ei ole õige, kuna keemilises tasakaalus on toodete kontsentratsioonid alati suuremad kui reagentidel, kui tasakaalu ei mõjuta väline tegur.
e) See on õige, kuna keemilises tasakaalus ei ole reagentide ja saaduste kontsentratsioonid alati ühesugused.
Õige vastus: b) See pole õige, kuna keemilises tasakaalus võivad toodete ja reagentide kontsentratsioonid olla erinevad, kuid need on konstantsed.
Tasakaalu korral saab toodete ja reagentide koguseid arvutada konstanti järgi tasakaal ja see ei peaks tingimata olema pool toodete kogusest ja teine pool reaktiivid.
Tasakaalukontsentratsioonid ei ole alati ühesugused, need võivad olla erinevad, kuid konstantsed, kui tasakaaluhäireid ei esine.
Tasakaalukontsentratsioonid peaksid sõltuma sellest, millist reaktsiooni eelistatakse, kas otsest või pöördvõrdelist. Seda saame teada K väärtuse järgiç: kui Kç 1, eelistatakse otsest reaktsiooni. juba siis, kui Kç
1 eelistatakse vastupidist reaktsiooni.
Keemilise tasakaalu tabelid
3. (UFPE) 20. sajandi alguses tekitas Esimese maailmasõja ootus suurt vajadust lämmastikuühendite järele. Haber oli õhus lämmastikust ammoniaagi tootmise eestvedaja. Kui ammoniaak pannakse suletud anumasse, laguneb see järgmise tasakaalustamata keemilise võrrandi järgi: NH3g) → N2 g) + H2 g). Kontsentratsioonide varieerumist ajas illustreerib järgmine joonis:

Ülaltoodud joonise analüüsist võime öelda, et kõverad A, B ja C tähistavad vastavalt järgmiste reaktsioonikomponentide kontsentratsioonide ajalist muutust:
a) H2, ei2 ja NH3
b) NH3, H2 ja ei2
c) NH3, ei2 ja H2
d) Ei2, H2 ja NH3
e) H2, NH3 ja ei2
Õige vastus: d) N2, H2 ja NH3.
1. samm: tasakaalustage keemiline võrrand.
2 NH3g) → N2 g) + 3 H2 g)
Tasakaalustatud reaktsiooniga saime aru, et lämmastiku ja vesiniku lagunemiseks on vaja 2 mooli ammoniaaki. Samuti on reaktsioonis tekkiva vesiniku kogus kolm korda suurem kui ammoniaagi kogus.
2. samm: tõlgendage diagrammi andmeid.
Kui ammoniaak laguneb, on graafikus selle kontsentratsioon maksimaalne ja väheneb, nagu nähtub kõverast C.
Saadud tooted on reaktsiooni alguses kontsentratsiooni tekkimisel nullid ja suurenevad, kui reaktiivist saab produkt.
Kuna toodetud vesiniku kogus on kolm korda suurem kui lämmastiku kogus, on selle gaasi kõver suurim, nagu on märgitud punktis B.
Teine moodustuv produkt on lämmastik, nagu on näha kõverast A.
4. (Cesgranrio) Süsteem, mida esindab võrrand oli tasakaalus. Tasakaalu seisundit muudeti järsult aine G lisamisega. Süsteem reageerib tasakaalu taastamiseks. Milline järgmistest diagrammidest kujutab kõige paremini kirjeldatud protsessi käigus toimunud muudatusi?
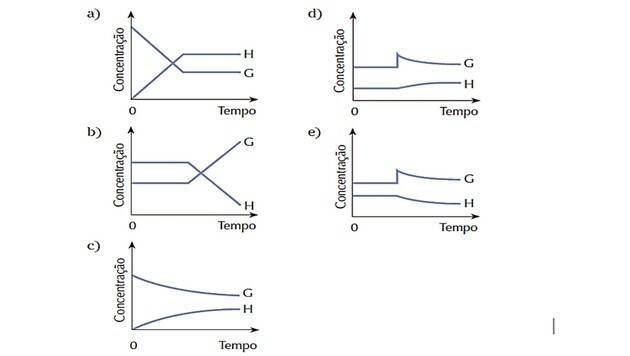
Õige vastus: d).

Kuna süsteem oli alguses tasakaalus, jäid ainete G ja H kogused konstantseks.
Häire ilmnes siis, kui G kontsentratsioon suurenes ja süsteem reageeris selle muundamisega reaktiiv rohkemas produktis H, nihutades tasakaalu paremale ehk soosides reaktsiooni otsene.
Vaatleme, et reagendi kõver G väheneb selle tarbimisel ja toote kõver H suureneb selle moodustumisel.
Uue tasakaalu saavutamisel muutuvad suurused uuesti konstantseks.
Tasakaalukonstant: kontsentratsiooni ja rõhu suhe
5. (UFRN) Teades, et KP = Kç (RT)n, võime öelda, et KP = Kç,
terasest2g) + H2 g) ↔ COg) + H2Og)
b) H2 g) + ½2 g) H2O(1)
c) Ei2 g) + 3 H2 g) ↔ 2 NH3g)
d) EIg) + ½ O2g) ↔ EI2g)
e) 4 FeSs) + 7 O2 g) ↔ 2 Fe2O3 (s) + 4 SO2g)
Õige vastus: a) CO2g) + H2 g) ↔ COg) + H2Og)
K-leP olema võrdne K-gaç moolide arvu varieerumine peab olema võrdne nulliga, kuna mis tahes nulli tõstetud arv annab tulemuseks 1:
KP = Kç (RT)0
KP = Kç x 1
KP = Kç
Moolide arvu muutus arvutatakse järgmiselt:
∆n = toodete moolide arv - reagentide moolide arv
Selles arvutuses osalevad ainult gaasilises olekus olevate ainete koefitsiendid.
Iga alternatiivse võrrandi korral on meil:
| terasest2g) + H2 g) ↔ COg) + H2Og) | ∆n = [(1 + 1) - (1 + 1)] = 2 - 2 = 0 |
| b) H2 g) + ½2 g) H2O(1) | ∆n = [0 - (1 + 1/2)] = 0 - 3/2 = - 3/2 |
| c) Ei2 g) + 3 H2 g) ↔ 2 NH3 g) | ∆n = [2 - (1 + 3)] = 2 - 4 = - 2 |
| d) EIg) + ½2 g) ↔ EI2 g) | ∆n = [1 - (1 + 1/2)] = 1 - 3/2 = - 1/2 |
| e) 4 FeSs) + 7 O2 g) ↔ 2 Fe2O3 (s) + 4 SO2 g) | ∆n = [(0 + 4) - (0 + 7)] = 4-7 = - 3 |
Nende tulemuste abil võime täheldada, et alternatiiv, mille väärtus vastab nõutavale tulemusele, on esimene võrrand.
6. (UEL-kohandatud) Reaktsiooniks, mida tähistab tasakaalu konstandid Kç ja K.P väljendatakse võrranditega: (Arvestades: p = osaline rõhk)
Õige alternatiiv:
Tasakaalukonstant arvutatakse järgmiselt:
Tahked ühendid nende konstantsete kontsentratsioonide tõttu ei osale K arvutamiselç, seega on antud võrrandi tasakaalukonstant:
Tasakaalukonstandi jaoks osalevad arvutuses rõhu osas ainult gaasid, seega:
Tasakaalukonstandi arvutamine
7. (Enem / 2015) Tööstustes, kus heitvesi visatakse veekogudesse, näiteks jõgedesse ja järvedesse, kasutatakse mitmeid happeid, mis võivad mõjutada keskkonnatasakaalu. Happesuse neutraliseerimiseks võib heitveele lisada sobivas koguses kaltsiumkarbonaatsoola, kuna see toodab vesinikkarbonaati, mis neutraliseerib vett. Esitatakse protsessiga seotud võrrandid:
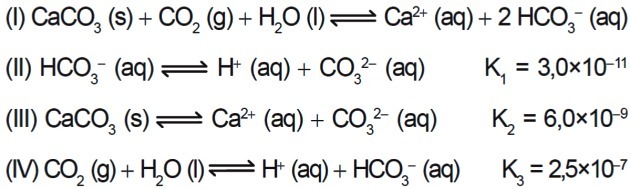
Kui võtta aluseks reaktsioonide II, III ja IV tasakaalukonstandide väärtused temperatuuril 25 ° C, siis milline on reaktsiooni I tasakaalukonstandi arvuline väärtus?
a) 4,5 x 10-26
b) 5,0 x 10-5
c) 0,8 x 10-9
d) 0,2 x 105
e) 2,2 x 1026
Õige vastus: b) 5,0 x 10-5
1. samm: kasutage vajalike muudatuste tegemiseks Hessi seadust.
Antud keemiline võrrand:
Konstant arvutatakse järgmiselt:
Kuid kui võrrandi ümber pöörame, saame tulemuseks:
Ja konstant muutub pöördvõrdeliseks:
Küsimuses toodud võrrandi 1 jõudmiseks peame pöörama võrrandi II, nagu eelmises näites.
2. samm: võrrandi I tulemuse saamiseks manipuleerige võrranditega II, III ja IV.
3. samm: arvutage võrrandi I tasakaalukonstant.
K arvutamineMina tehakse korrutades püsiväärtused.
Kuna arvutustes on meil võrdsed aluste võimsused, kordame baasi ja lisame eksponendid.
Kuna meil on nüüd aluste võrdse võimsusega jagunemine, siis korrame baasi ja lahutame eksponendid.
8. (UnB) Fosforpentakloriid on orgaanilises keemias väga oluline reaktiiv. See valmistatakse gaasifaasis läbi reaktsiooni:
3,00 L mahutav pudel sisaldab tasakaalus 200 ° C juures: 0,120 mol PCI5g), 0,600 mol PCI3g) ja 0,0120 mol CL2g). Kui suur on sellel temperatuuril tasakaalukonstandi väärtus?
Õige vastus: 50 (mol / L)-1
1. samm: koguge reaktsiooni tasakaalukonstandi avaldis.
2. etapp: arvutage tasakaalu iga komponendi kontsentratsioon mol / l.
Molaarse kontsentratsiooni valem:
| PCl3 | Cl2 | PCl5 |
3. etapp: asendage konstantses avaldises kontsentratsioonid ja arvutage K väärtusç.
Tasakaalu tasakaalu rakendused
9. (Enem / 2016) Pärast nende täielikku kulumist saab rehve energia saamiseks põletada. Vulkaniseeritud kummi täielikul põlemisel tekkivate gaaside hulgas on mõned saasteained ja põhjustavad happevihmasid. Et vältida nende atmosfääri pääsemist, saab need gaasid mullitada sobivat ainet sisaldavasse vesilahusesse. Võtke arvesse tabelis loetletud teavet ainete kohta.
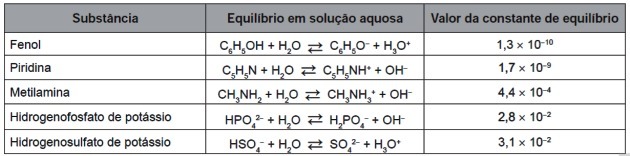
Tabelis loetletud ainete hulgas on saasteaineid kõige tõhusamalt kõrvaldada (a)
a) fenool.
b) püridiin.
c) metüülamiin.
d) kaaliumvesinikfosfaat.
e) kaaliumvesiniksulfaat.
Õige vastus: d) kaaliumvesinikfosfaat.
CO2, vääveloksiidid (SO2 ja nii3) ja lämmastikoksiidid (NO ja NO2) on peamised saastavad gaasid.
Kui nad reageerivad atmosfääris oleva veega, on a happe moodustumine mis põhjustavad vihma happesuse tõusu, mistõttu seda nimetatakse happevihmaks.
Tabelis toodud tasakaalukonstandid arvutatakse toodete ja reagentide kontsentratsioonide suhte järgi järgmiselt:
Pange tähele, et tasakaalukonstant on proportsionaalne toodete kontsentratsiooniga: mida suurem on toodete kogus, seda suurem on K väärtusç.
Pange tähele K tabeli esimene ja viimane liitväärtusç:
| Püridiin | ||
| Kaaliumvesiniksulfaat |
Neid kahte arvu võrreldes näeme, et mida väiksem on negatiivne võimsus, seda suurem on konstandi väärtus.
Saasteainete tõhusamaks eemaldamiseks OH- reageerida H ioonidega+ esinevad hapetes läbi a neutraliseerimisreaktsioon.
Esitatud ainete hulgas on happeliste ühendite neutraliseerimiseks vajalikud hüdroksüülrühmad püridiin, metüülamiin ja kaaliumvesinikfosfaat.
Selleks, et teada saada, milline ühend on kõige tõhusam, jälgime tasakaalu konstante: mida suurem on konstantne väärtus, seda suurem on OH kontsentratsioon-.
Seega on selleks otstarbeks sobivat ainet sisaldav vesilahus kaaliumvesinikfosfaat, kuna see on aluselisem ja neutraliseerib happeid tõhusamalt.
Lisateabe saamiseks lugege neid tekste.:
- iooniline tasakaal
- Neutraliseerimisreaktsioon
10. (Enem / 2009) Seebid on pika ahelaga karboksüülhapete soolad, mida kasutatakse pesemisprotsesside käigus vees vähelahustuvate ainete, nt õlide ja rasvad. Järgmine joonis näitab seebimolekuli struktuuri.
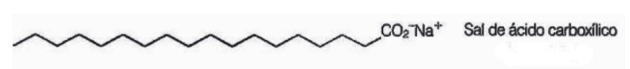
Lahuses võivad seebianioonid vett hüdrolüüsida ja moodustada seeläbi vastava karboksüülhappe. Näiteks kehtestatakse naatriumstearaadi jaoks järgmine tasakaal:
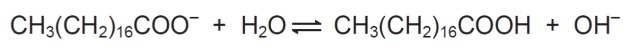
Kuna moodustunud karboksüülhape on vees halvasti lahustuv ja rasvade eemaldamisel vähem efektiivne, sööda pH-d tuleb kontrollida, et vältida ülaltoodud tasakaalu nihkumist paremale.
Tekstis sisalduva teabe põhjal on õige järeldada, et seebid toimivad teatud viisil:
a) Efektiivsem aluselisel pH-l.
b) efektiivsem happelises pH-s.
c) Efektiivsem neutraalse pH juures.
d) Tõhus igas pH vahemikus.
e) efektiivsem happelise või neutraalse pH juures.
Vastus: a) Efektiivsem aluselisel pH-l.
Näidatud tasakaalus näeme, et veega reageerimisel moodustab naatriumstearaat karboksüülhappe ja hüdroksüülrühma.
PH reguleerimise eesmärk ei ole lubada karboksüülhappe moodustumist ja seda tehakse tasakaalu nihutamisega OH kontsentratsiooni muutmisega-.
seda rohkem OH- lahuses on tootepoolel häire ja keemiline süsteem reageerib aine, mille kontsentratsioon on suurenenud, antud juhul hüdroksüülrühma tarbimisega.
Järelikult toimub toodete muundamine reagentideks.
Seetõttu toimivad seebid kõige tõhusamalt aluselise pH juures, kuna hüdroksüüli ülejääk nihutab tasakaalu vasakule.
Kui pH oleks happeline, oleks H suurem kontsentratsioon+ mis mõjutaks tasakaalu OH-i tarbimisega- ja tasakaal toimiks, tootes rohkem hüdroksüülrühma, nihutades tasakaalu vasakule ja tootes rohkem karboksüülhapet, mis ei paku käesolevas protsessis huvi.
Keemiline tasakaalu nihe
11. (Enem / 2011) Karastusjookidest on üha enam saanud rahvatervise poliitika. Liimitooted sisaldavad fosforhapet, ainet, mis on kahjulik kaltsiumi fikseerimisele, mineraalile, mis on hammaste maatriksi põhikomponent. Kaaries on dünaamiline tasakaaluhäire protsess hammaste demineraliseerumise protsessis, mineraalide kadu happesuse tõttu. On teada, et hambaemaili põhikomponent on sool, mida nimetatakse hüdroksüapatiidiks. Sooda vähendab sahharoosi olemasolu tõttu biokile (bakteriaalne naast) pH-d, põhjustades hambaemaili demineraliseerumist. Sülje kaitsemehhanismid võtavad pH taseme normaliseerimiseks 20–30 minutit, hamba remineraliseeruvad. Järgmine keemiline võrrand tähistab seda protsessi:
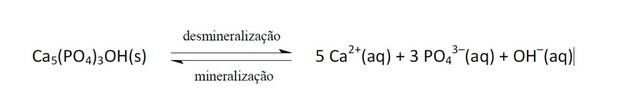 GROISMAN, S. Hinnatakse sooda mõju hammastele ilma seda dieedist välja võtmata. Saadaval: http://www.isaude.net. Juurdepääs: 1. mai 2010 (kohandatud).
GROISMAN, S. Hinnatakse sooda mõju hammastele ilma seda dieedist välja võtmata. Saadaval: http://www.isaude.net. Juurdepääs: 1. mai 2010 (kohandatud).
Arvestades, et inimene tarbib karastusjooke iga päev, võib suurenenud kontsentratsiooni tõttu tekkida hammaste demineraliseerumisprotsess.
a) OH–, mis reageerib Ca-ioonidega2+, nihutades tasakaalu paremale.
b) H+, mis reageerib OH hüdroksüülidega–, nihutades tasakaalu paremale.
c) OH–, mis reageerib Ca-ioonidega2+, nihutades tasakaalu vasakule.
d) H+, mis reageerib OH hüdroksüülidega–, nihutades tasakaalu vasakule.
e) Ca2+, mis reageerib OH hüdroksüülidega–, nihutades tasakaalu vasakule.
Õige vastus: b) H+, mis reageerib OH hüdroksüülidega–, nihutades tasakaalu paremale.
Kui pH langeb, on selle põhjuseks happesuse tõus, see tähendab H-ioonide kontsentratsioon+, nagu öeldakse avalduses, esineb fosforhapet.
Need ioonid reageerivad OH-ga- põhjustades selle aine tarbimist ja sellest tulenevalt tasakaalu nihutamist paremale, kuna süsteem toimib, tootes rohkem neid eemaldatud ioone.
Tasakaalumuutus reaktiivide ja saaduste vahel toimus OH kontsentratsiooni vähenemise tõttu-.
Kui Ca ioonid2+ ja oh- kui kontsentratsioon oleks suurenenud, nihutaks see tasakaalu vasakule, kuna süsteem reageeriks neid tarbides ja moodustades rohkem hüdroksüapatiiti.
Eelmise saldo muutmine seoses külmutusagensi lekkega kirjeldatud tingimustel annab tulemuseks:
a) CO vabastamine2 keskkonna jaoks.
b) Mahuti temperatuuri tõstmine.
c) Mahuti siserõhu tõus.
d) CO kontsentratsiooni tõus2 vedelikus.
e) märkimisväärse koguse H moodustumine2O.
Õige vastus: a) CO eraldumine2 keskkonna jaoks.
Pudeli sees lahustati süsinikdioksiid vedelikus kõrge rõhu tõttu.
Pudeli avamisel võrdub rõhk anumas (mis oli suurem) rõhuga keskkonnas ja sellega pääseb välja süsinikdioksiid.
Reaktantide ja saaduste tasakaalumuutus toimus rõhu languse tõttu: rõhu langedes nihkub tasakaal suurima mahuni (moolide arv).
Reaktsioon nihkus vasakule ja CO2 vedelikus lahustunud aine vabanes, pudeli avamisel lekkis.
