Füüsikalise seisundi muutused sõltuvad mõnest tegurist, mis on seotud temperatuuri, rõhu ja protsessiga seotud energiahulgaga.
Looduses on aine kolm füüsikalist olekut: tahke, vedel ja gaasiline. Ja füüsilise seisundi muutused tähistavad viit muutumisprotsessi ühest olekust teise.
Muudatused on: kondenseerumine või veeldamine, tahkestumine, sulandumine, aurustamine ja sublimatsioon. Igal muudatuse tüübil on mõned eripärad ja need on seotud asja omadustega.
Kondensatsioon
Kondensatsioon tähistab riigi möödumist gaasiline kuni vedel.
Selle põhjuseks on gaasi jahutamine, mis kipub kondenseeruma ja muutuma vedelaks.
Tahkumine
Tahkumine on vedelast tahkesse olekusse.
Vedelas olekus kipub jahtununa tahkuma. Vee korral toimub tahkestumine temperatuuril 0 ° C

Fusioon
Sulandumine on tahkis olekust vedelaks.
Iga aine molekulid vajavad liikumiseks teatud kogust energiat. Kui energiat on vähem, kipuvad nad vähem liikuma ja materjal kipub olema tahke.
Soojusallikast energiat saades (küte) muutuvad nad erutatumaks ja võivad muuta olekut.

Aurustamine
Aurustamine on vedelast kuni gaasilise olekuni. See võib juhtuda kahel viisil:
- Keemine: kiire kuumutamine.
- Aurustamine: aeglane kuumutamine.
1 ° C kuni 100 ° C on see vedel.

Sublimatsioon
Sublimatsioon on tahkis kuni gaasiline See on pärit gaasiline olek tahkeks (reublimatsioon).
Seda tüüpi muutused toimuvad sõltuvalt teatud rõhu ja temperatuuri tingimustest. Igal elemendil on oma Faaside skeem, kus paiknevad selle liitmise, aurustamise ja sublimatsiooni kõverad.

Vee füüsikalised olekud
Vesi on kergesti leitav kolmes füüsikalises olekus: tahke, vedel ja gaasiline.
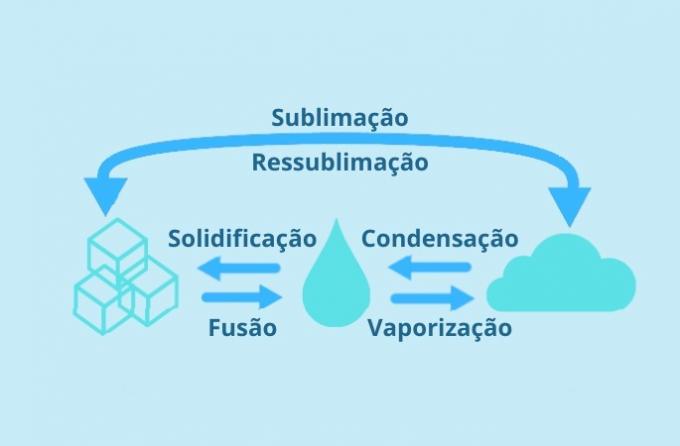
Iga vee füüsikaline olek on võimalik vastavalt temperatuuri ja rõhu kõikumisele.
Normaalsel rõhul (1atm) sulab vesi temperatuuril 0 ° C ja keeb temperatuuril 100 ° C.
Vee molekulid temperatuuril -1 ° C on tahkes olekus ja temperatuuril 0 ° C toimub muutus (sulamistemperatuur) jääl temperatuuril 0 ° C vees temperatuuril 0 ° C.
Kui see jõuab temperatuurini 100 ° C, läbib see uue oleku muutuse (aurustumine), liikudes vedelast gaasilisse olekusse.
Nagu selle faasiskeemilt nähtub:
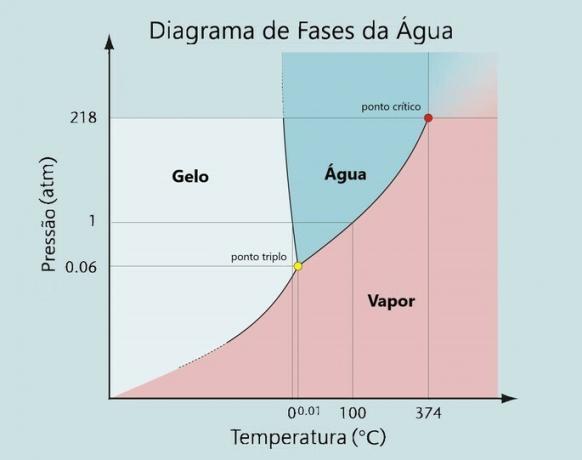
Selle teema kohta lisateabe saamiseks lugege ka järgmist:
- Vee füüsikalised olekud
- Mateeria füüsilised seisundid
- Füüsikalised ja keemilised muundamised
- Füüsikalised ja keemilised nähtused



