Sublimatsioon on muutus tahkest olekust gaasiliseks ja vastupidi, ilma vedelat olekut läbimata.
Aine sublimatsiooniprotsessi läbiviimiseks tuleb sellele rakendada teatud temperatuuri ja rõhu väärtusi.
Koipallid ja CO2 tahke (kuivjää) on näited ainetest, mis läbivad keskkonnatingimustes sublimatsiooni.

Faaside skeem
Aine füüsikalise oleku võime avastada, kui teame selle temperatuuri ja rõhu väärtusi.
Selleks kasutame iga aine jaoks koostatud skeeme eksperimentaalselt leitud väärtustest.
Helistatud "Faaside skeem", see on jagatud kolmeks piirkonnaks, mis tähistavad tahkeid, vedelaid ja gaasilisi olekuid. Need piirkonnad piiritlevad jooned tähistavad aine faasi muutumise punkte.
Diagrammi kolmikpunkt näitab temperatuuri ja rõhku, mille juures aine võib kolmes faasis koos eksisteerida. Selle punkti all on sublimatsioonikõver.
Selle kõvera punktid määravad rõhu ja temperatuuri väärtused, mille korral sublimatsioon toimub.
Tahke aine rõhu all, mis on väiksem kui kolmekordne punkt, läheb kuumutamisel tahke aine otse gaasilisse olekusse.
Otsese tahke oleku gaasiliseks muutumine võib toimuda ka rõhu vähendamisega, kui selle temperatuur on kolmikpunktist madalam.
Lisateave aadressil: Füüsikalise seisundi muutused.
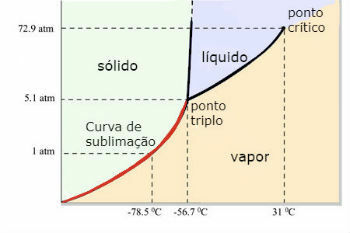
Süsinikdioksiidi (CO) faaside skeem2 )
CO kolmikpunkt2 tekib siis, kui rõhk on 5 atm. See asjaolu õigustab, et kuiva jää puhul on tavaline näha sublimatsiooni esinemist, kuna ümbritsev rõhk on 1 atmosfäär.
Sel põhjusel ei saada vedelat süsinikdioksiidi keskkonnatingimustes. Nendes tingimustes on see kas tahkes või auru olekus.
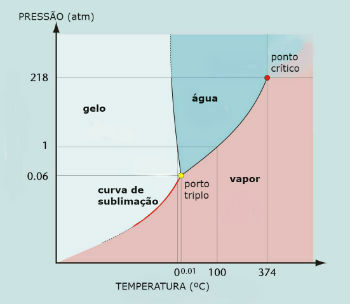
Vee faasiskeem (H2O)
Vee kolmikpunkt tekib siis, kui rõhk on ainult 0,06 atm. Seega pole ümbritsevates tingimustes vee sublimatsioon tavaline.
Lisateabe saamiseks lugege ka järgmist:
- Vee füüsikalised olekud
- Mateeria füüsilised seisundid
- Veeldamine või kondenseerumine
- Mateeria omadused
- Tahkumine
- Fusioon
- Aurustamine
- Keemine
- Aurustamine