Gallium on keemiline element, mille aatomnumber (Z) on 31 ja selle sümbol on Ga. See kuulub perekonda 13 (või vana numeratsiooni järgi IIIA rühma), mis on nende perekond boor, mis on alumiiniumiga sarnane “hõbedane” metall.
Üks selle huvitavamaid omadusi on sulamistemperatuur, mis on peaaegu kõigi varem teadaolevate metallidega (välja arvatud elavhõbe) madal, umbes 29,76 ° C. Seega on keskkonnatingimustes tavaliselt tahkis. Soojematel päevadel sulab see aga vedelas olekus. Sellepärast, kui me hoiame seda metalli oma kätes, hakkab see sulama, sest meie temperatuur on selle sulamistemperatuurist kõrgem.

Galliumi hoiustamisel ei saa see tahkestumisel kogu anumat täita, kuna see paisub
Internetis on palju videoid, mis näitavad lusikat, mis veeklaasi pannes sulab. Tegelikult on need lusikad valmistatud galliumist, mitte muudest tavalisematest metallidest või metallisulamitest nagu alumiinium või terasest. Seega, kui galliumlusikas asetatakse sooja vette, muutub see vedelaks. Vaadake selle kohta lisateavet tekstist “Ettepanek sulamistemperatuuri katseklassi kohta”.
Galliumil on ka teine eripära, milleks on tohutu vahemik sulamis- ja keemistemperatuuride vahel. Nagu juba mainitud, on selle sulamistemperatuur umbes 29,76 ° C, kuid selle keemistemperatuur on umbes 2204 ° C.
Prantsuse keemik Paul Lecoq de Boisbaudran avastas gallium 27. augustil 1875 kella 3–4 hommikul. Huvitav aspekt on see, et aastaid varem, 1868. aastal, oli vene keemik Dimitri Ivanovitš Mendelejev (1834-1907) pakkus välja perioodilise tabeli, kuid jättis tühiku seni seni olnud elemendi jaoks teadmata. Mendelejev nimetas seda ekalumiiniumiks, kuna ennustas suurejooneliselt, et horisontaalses boorireas alumiiniumi ja uraani vahel see element lebab.

Prantsuse keemik Paul Lecoq de Boisbaudran - gallium avastaja
Mendelejev ennustas isegi selle elemendi omadusi, nagu aatommass, mis oleks 68, ja erikaal, mis oleks 5,9. Nii avastas Lecoq elemendi, mille aatommass oli 69 ja erikaal 4,7, mis näitab, et Mendelejev eksis. Mendelejev ütles siiski, et Lecoqi proov ei olnud piisavalt puhas ja ta peaks katseid kordama.
Seda Lecoq tegi ja üllatuslikult oli Mendelejevil õigus, selle uue elemendi erikaal oli 5,9. Nii et see oli tõesti eka-alumiinium, mida Mendelejev oli ette kujutanud.
Lecoq andis avastatud elemendile nime Gallium, viidates Prantsusmaa ladinakeelsele nimele, milleks on Gallia. Kuid on mõned, kes ütlevad, et tegelikult oli nende eesmärk teine, sest prantsuse keeles tähendab Le coq “kukke” ja ladina keeles gallus.
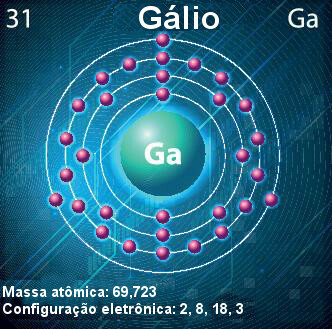
Galliumi aatom - sümbol, aatomnumber, aatommass ja elektronide konfiguratsioon
Galliumi teine omadus on see, et see söövitab teisi metalle. Internetis on mõned videod, mis näitavad väikese vedeliku galliumit alumiiniumpurgi kohale. Mõne tunni pärast on võimalik seda oma kätega murda.
Galliumi rakenduste hulgas võime esile tõsta:
* Seda kasutatakse peeglite valmistamiseks;
* See on pooljuht ja juhib soojust kaks korda rohkem kui rauda. Seetõttu kasutatakse seda dioodide, valgusdioodide, transistoride ning temperatuuri-, valguse- ja magnetvälja andurite tootmisel;
* Termomeetrites, mida kasutatakse väga kõrgel temperatuuril;
* Tootmisel metallisulamid millel peavad olema madalad sulamistemperatuurid;
* Vesinikgaasi saamine alumiiniumi galliumisulami ja vee kokkupuutel;
* Ga-37 isotoop on radioaktiivne ja seda kasutatakse märgistusmaterjalina haiguste ja kasvajate avastamise testides.
Autor Jennifer Fogaça
Lõpetanud keemia



