Süsivesinikud, mida nimetatakse ka vesinikkarbiididon orgaanilised ühendid, mille koostises on ainult aatomid süsinik (C) ja alates vesinik (H), seega üldvalemiga CxHy.
Süsivesinik koosneb süsiniku struktuurist, millega vesiniku aatomid seonduvad kovalentne side.
See on orgaanilise keemia kõige olulisem ühend.
Igat tüüpi süsivesinikud oksüdeeruvad kergesti, vabastades seeläbi soojust. Enamik neist ei ole vees lahustuvad.
Looduslikud süsivesinikud on keemilised ühendid, mis moodustuvad Maa sees (enam kui 150 km kaugusel sügavus) kõrgel rõhul ja jõuavad geoloogiliste protsesside kaudu madalama rõhuga tsoonidesse.
Kust on leitud süsivesinikke?
Peamine süsivesinike allikas on nafta. Seetõttu on süsivesinik mitmetes derivaatides, näiteks petrooleum, parafiin, maagaas, Bensiin, Vaseliin, diisliõli, LPG (Veeldatud naftagaas), polümeerid (näiteks plast ja kumm).
See orgaaniline ühend moodustab 48% Brasiilia energiamaatriksist.
Süsinikuahel, mis moodustab osa süsivesiniku koostisest, on neljavalentnesee tähendab, et see võib luua neli ühendust.
Süsinik on võimeline läbi teiste süsinikuaatomite ja vesinikega siduma lihtsad lingid, kahekordistab või kolmekordsed.
Süsivesinike klassifikatsioon
Süsivesinike klassifikatsioon põhineb kolmel eripäral: a vormis peamise süsinikuahela, Ühendused süsinikuahelatest, alküülradikaalide olemasolu süsinikuahelas ja heteroaatomite olemasolu süsinikuahela jagamine.
rohkem teada vesinik.
Peamine süsinikuahela kuju
Peamise süsinikuahela kuju osas jaotatakse süsivesinike klassifikatsioon järgmiselt: alifaatne ja tsükliline.
Kontrollige, millest need süsinikuahela vormid koosnevad.
alifaatsed süsivesinikud
Alifaatsed süsivesinikud moodustuvad süsinikuahelate kaudu avatud või atsükliline. Nendes ahelates on süsinikud klemmid.
Näited:
alkaan
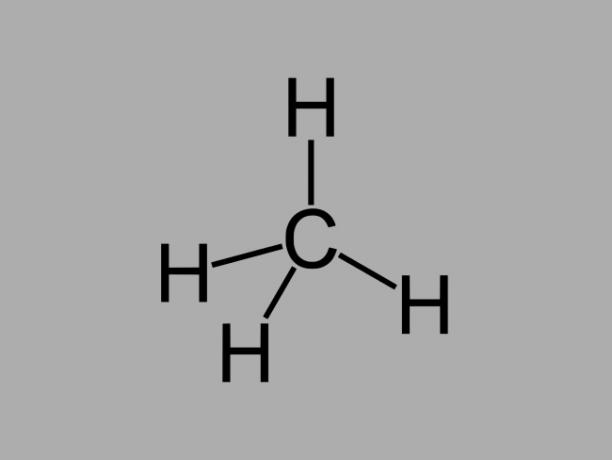
Alkaanisüsivesinikud, mida nimetatakse ka parafiinid või parafiinne, on õliühendid, kus süsinike vahel on ainult üksiksidemed.
Alkaani üldvalem on CeiH2ei + 2 (n = täisarv).
alkeen
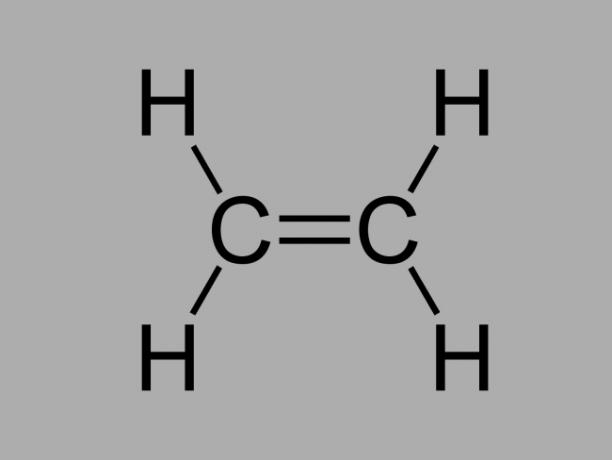
Nimetatud ka olefiin, alkeen või etüleensüsivesinik, alkeen on halvasti reageeriv ühend, kus süsinike vahel on kaksikside.
Alkeeni üldvalem on CeiH2ei.
alküün
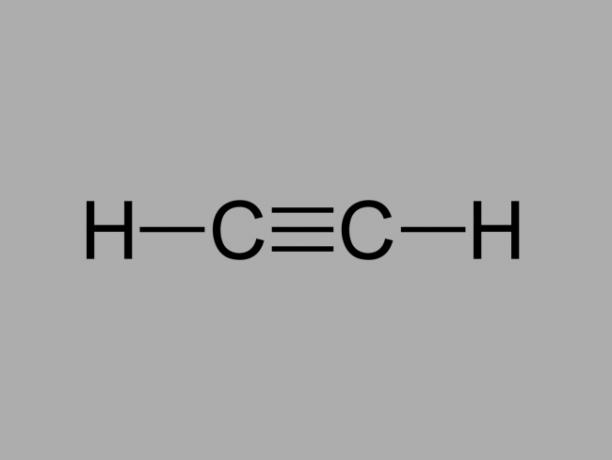
Nimetatud ka metüülatsetüleen, alküün on süsivesinik, kus olemasolevad sidemed süsinike vahel on kolmekordsed.
Alküüni üldvalem on CeiH2ei-2.
alkadieen

Alkaanid, mida nimetatakse ka dieenideks või diolefiinideks, on süsivesinikud, kus süsinikuvahelised sidemed on topelt.
Alkadieeni üldvalem on CeiH2ei-2.
Tsüklilised süsivesinikud
Tsüklilised süsivesinikud moodustuvad suletud või tsükliliste süsinikahelate abil. Nendel ahelatel ei ole terminaalseid süsinikke.
Näited:
Cyclan
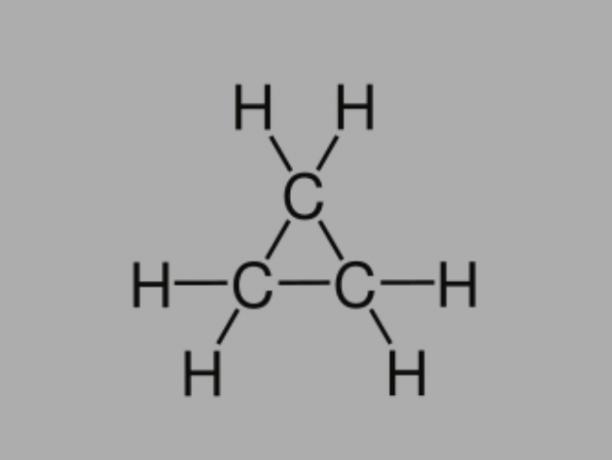
Nimetatud ka tsükloalkaan, tsükloparafiin või nafteenne süsivesinik, tsüklane on küllastunud süsivesinik, mis koosneb üksiksidemetest.
Sellel on suletud süsinikuahel ja selle üldvalem on CeiH2ei.
Tsüklooniline

Nimetatud ka tsükloalkeenid, tsükleenid on küllastumata süsivesinikud, mis koosnevad kaksiksidemetest.
Tsükleenil on suletud süsinikuahel ja selle üldvalem on CeiH2ei−2.
jalgrattur
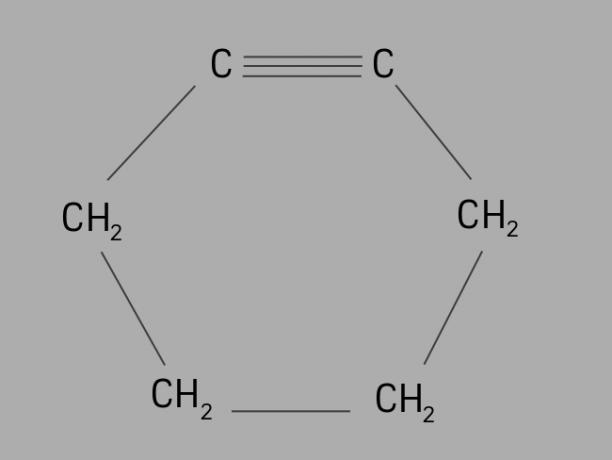
Nimetatud ka tsükloalküün või tsükloalküün, on tsükliin tsükliline ja küllastumata süsivesinik.
Selle moodustab suletud süsinikahel, milles on kolmiksidemed ja selle üldvalem on CeiH2ei-4.
Aromaatne

või

Nimetatud ka areenid, aromaatsed süsivesinikud on küllastumata ühendid, mis moodustuvad kaksiksidemetega.
Aromaatsel on suletud või tsükliline süsinikuahel ja selle üldvalem on C6H6.
Süsinikahelate sidumise tüüp
Sõltuvalt süsinikuahelate ühendamise tüübist võib süsivesinikke klassifitseerida küllastunud või küllastumata.
Vaadake allpool, millest igaüks neist klassifikatsioonidest koosneb.
Küllastunud süsivesinikud
Küllastunud süsivesinikud moodustuvad lihtsad lingid.
Näited: alkaanid, tsüklaanid.
küllastumata süsivesinikud
Küllastumata süsivesinikud moodustuvad kaksiksidemed või kolmekordsed.
Näited: alkeenid, alküünid, alkadieenid.
Alküülradikaalide olemasolu
Alküülradikaalide olemasolu korral võivad süsivesinikud olla süsinikuahelaga normaalne või hargnenud.
tavaline süsinikuahel
Tavalisel süsinikahelaga süsivesinikul ei ole alküülradikaale.
Näide: pentaan
hargnenud süsinikahel
Kui süsivesinikul on hargnenud süsinikuahel, tähendab see, et selle peamises süsinikuahelas on alküülradikaalid.
Näide: metüülpropaan
Süsinikuahelat jagavate heteroaatomite olemasolu
Järjestikune süsinikuahel võib lõheneda või mitte, sõltuvalt heteroaatomite olemasolust.
Homogeenne süsinikuahel
Kui süsivesinikul on homogeenne süsiniku peamine ahel, tähendab see seda ahelat pole jagatud heteroaatomite abil.
Heterogeenne süsinikuahel
Kui süsivesinikul on heterogeenne süsiniku peamine ahel, oli sellel ahelal oma lõhenenud süsinikuahel heteroaatomi poolt.
Süsivesinike nomenklatuur
Süsivesinike nomenklatuur määratletakse kolme osa kombinatsiooni kaudu:

Eesliide tähistab süsinike kogust, vaheühend seob tüübi ja sufiks tähistab funktsiooni, kuhu ühend kuulub (antud juhul süsivesinike klass).
Allpool leiate süsivesinike tähistamiseks kombineeritud eesliidete ja vaheühendite loendi.
Eesliidete loend
| Süsinike arv | Eesliide |
|---|---|
| 1 | Kohtusime- |
| 2 | Et- |
| 3 | Prop- |
| 4 | Aga- |
| 5 | pent- |
| 6 | Hex- |
| 7 | Hept- |
| 8 | Okt- |
| 9 | Mitte- |
| 10 | Detsember |
Vahendajate nimekiri
| Ühenduse tüüp | Vahendaja |
|---|---|
| Ainult üksikud kõned | -ja- |
| Paar | -en- |
| kolmekordne | sisse |
| kaks paari | -dien- |
Vaadake mõnda süsivesinike nimetamise näidet.
Näited:
CH3 - CH2 - CH2 - CH3
Ülaltoodud struktuurivormis näeme 4-süsinikühendit, millel on ainult üksiksidemed (tähistatud sümboliga - -).
- 4 süsiniku eesliide = but-
- Ühekordse sidumise vahe = -an-
- Süsivesinike järelliide = -o
Vaadake, et liit eesliide + vahe + järelliide annab nime BUTAAN.
CH2 = CH2
Ülaloleval struktuurivormil on 2 süsinikku ja 1 kaksikside (tähistatud sümboliga = =).
- 2 süsiniku eesliide = et-
- Kaksiksidemete vahe = -en-
- Süsivesinike järelliide = -o
Vaadake, et liit eesliide + vahe + järelliide annab nime KAHEKSAS.
CH2 = CH - CH2 - CH3
CH3 - CH = CH2 - CH3
Pange tähele, et mõlemal ülaltoodud struktuurivormil on 4 süsinikku ja 1 kaksikside (tähistatud sümboliga = =).
Seega on meil:
- 4 süsiniku eesliide = but-
- Kaksiksidemete vahe = -en-
- Süsivesinike järelliide = -o
Vaadake, et liit eesliide + vahe + järelliide annaks nime BUTENE kahe struktuurivormi jaoks.
Pange tähele, et struktuurivormid pole identsed, seega ei saa ka nomenklatuurid olla.
Kahe struktuurivormi erinevus seisneb kaksiksideme asukohas.
Sellisel juhul peame ahelas olevad süsinikud loendama topeltile lähimast otsast. Seetõttu peame kõnesolevate juhtumite korral vasakult paremale nummerdama.
Sisse CH2 = CH - CH2 - CH3:
- CH2 saab 1
- CH on 2
- CH2 saab 3
- CH3 saab 4
Pange tähele, et kaksikside on süsinik 1 see on süsinik 2.
Kaksiksideme leidmiseks peame kasutama väikseimat arvu (1): BUTENE -1
Sisse CH3 - CH = CH2 - CH3:
- CH3 saab 1
- CH on 2
- CH2 saab 3
- CH3 saab 4
Pange tähele, et kaksikside on süsinik 2 see on süsinik 3.
Kaksiksideme leidmiseks peame kasutama väikseimat arvu (2): BUTENE -2
Vastavalt IUPAC (Rahvusvaheline puhta ja rakenduskeemia liit - Rahvusvaheline puhta ja rakendusliku keemia liit), tuleks asukoht märkida veidi enne asetsevad (ülalolevate struktuuriformaalide korral kaksikside, mida tähistab vaheühend “-En-”).
Sellega on meil teine võimalus, mis on muide kõige õigem, kirjutada olemasolevate struktuurivormide nomenklatuur.
CH2 = CH - CH2 - CH3: BUTENE -1 või BUT-1-ENO (õigem vorm)
CH3 - CH = CH2 - CH3: BUTENE -2 või BUT-2-ENE (õigem vorm)
Lisateave IUPAC ja nomenklatuur.



