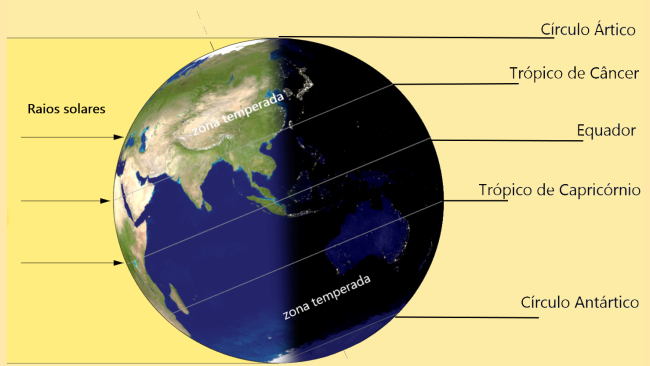
Apolaar on millegi kvaliteet pole polaarsust, mis on tavaliselt seotud orgaaniliste molekulidega.
Keemias on orgaaniliste molekulide polaarsus seotud neid molekule moodustavate aatomite elektronegatiivsuse intensiivsusega. Kui aatomite elektronegatiivsusel pole vahet, loetakse seda molekuli mittepolaarseks.
Mittepolaarses molekulis on erinevus aatomite seondumise elektronegatiivsuses peab alati olema null, kuna need tühistavad.
Tavaliselt koosnevad mittepolaarsed ühendused Süsivesinikud, see tähendab süsinikuaatomite või / ja vesiniku moodustunud ühendid.
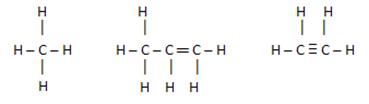
Nendel ühenditel on sarnased elektronlaengud, mistõttu nende vahel ei toimu laengunihet, vaid nende laengute nullimine.
Vt ka tähendust molekul.
Kui näiteks süsivesiniksidemes on erinevaid orgaanilisi ühendeid, peetakse seda juba polaarseks.
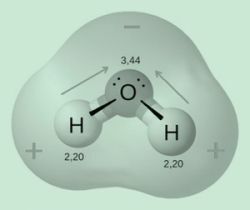 Näide: vee (H2O) molekulaarne geomeetria on moodustatud kahest vesiniku ja ühest hapnikust et selle ühendi elektronid on rohkem hapnikus kontsentreeritud, põhjustades selle nihkumist koormused. Seega muutub hapnik elektronegatiivsemaks kui vesinik, iseloomustades seda molekuli polaarsena.
Näide: vee (H2O) molekulaarne geomeetria on moodustatud kahest vesiniku ja ühest hapnikust et selle ühendi elektronid on rohkem hapnikus kontsentreeritud, põhjustades selle nihkumist koormused. Seega muutub hapnik elektronegatiivsemaks kui vesinik, iseloomustades seda molekuli polaarsena.
Teisisõnu on vesi polaarühend.
rohkem teada Süsivesinikud.
mittepolaarne ja polaarne
Erinevalt mittepolaarsetest ühendustest polaarmolekulid on need, millel on aatomite vahel nullist erinev elektronegatiivsus.
Erinevate elektronitiheduse tõttu akumuleerivad mõned aatomid rohkem elektrone kui teised, muutes tõmbejõu intensiivsemaks.
Mõned peamised mittepolaarsed ühendid on: bensiin, metaan ja etaan.
Mõned peamised polaarsed ühendid on: vesi, suhkur ja alkohol.