Gaasi iseloomustavad kolm omadust, mida nimetatakse olekumuutujaks, milleks on: rõhk, maht ja temperatuur. Kui üks või mitu neist muutujatest muutub, a gaaside muundamine, mida saab liigitada isotermilisteks, isovolumeetrilisteks või isobaarseteks.
kutsutakse isotermiline muundumine gaasi muundamine, milles süsteemi temperatuur püsib konstantsena, variatsioonid, mis esinevad ainult surve ja gaasi mahus.
Seda transformatsiooni nimetatakse kaBoyle-Mariotte'i seadus - nimi, mis on antud Iiri keemiku Boyle auks, kes 1660. aastal võttis vastu seaduse selle kohta, antud valimis ideaalne gaason rõhu ja gaasi hõivatud mahu korrutis püsiv, kui temperatuur ei muutu, ja ka Prantsuse füüsiku Mariotte auks, kes 1676. aastal iseseisvalt sama seaduse avastas.
Kokkuvõttes võib seaduse, mis kirjeldab gaasi käitumist isotermilise muundumise ajal, öelda järgmiselt:
“Isotermilise muundamise korral on ideaalse gaasiproovi rõhk pöördvõrdeline selle mahu muutusega. "
Ärge lõpetage kohe... Peale reklaami on veel;)
Selle seaduse põhjal võime järeldada, et gaasimassi rõhu suurendamisel väheneb selle hõivatud maht ja vastupidi. Seetõttu jääb nende kahe koguse vaheline toode konstantseks.
Matemaatiliselt saab Boyle-Mariotte'i seadust kirjeldada järgmisega:
P. v = konstant
Kuna rõhu ja mahu vaheline korrutis on konstantne, võime järeldada, et:
P1. V1 = lk2 . V2
Lisaks on see seadus ka graafiliselt kujutatud:
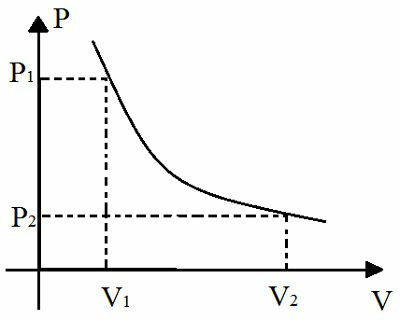
See graafik esindab rõhu muutuse ja temperatuuri muutuse suhet isotermilise muundamise ajal
Isotermilise transformatsiooni graafiline esitus on hüperbool. Mida suurem on toode lk. Selle teisenduse V, seda kaugemale jääb see hüperbool graafi telgedest. Sellele graafikul kujutatud kõverale antud nimi on isoterm.
Autor Mariane Mendes
Lõpetanud füüsika
Kas soovite sellele tekstile viidata koolis või akadeemilises töös? Vaata:
TEIXEIRA, Mariane Mendes. "Mis on isotermiline muundumine?"; Brasiilia kool. Saadaval: https://brasilescola.uol.com.br/o-que-e/fisica/o-que-e-transformacao-isotermica.htm. Juurdepääs 28. juunil 2021.


