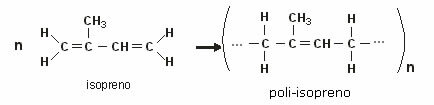
Sina Süsivesinikud koosnevad moodustatud süsinik (C) ja vesinik (H). Süsiniku paindlikkus, mis on nende ühendite põhielement, soosib tohutu struktuuride mitmekesisuse olemasolu Seetõttu võivad mõned omadused, näiteks sulamistemperatuur ja keemistemperatuur, erineda ühe süsivesiniku vahel.
Need on enamasti molekulid apolaarne, koos tugevuss molekulidevaheline indutseeritud dipooli tüüp ja tihedus väiksem kui The veest. Neid ühendeid saab identifitseerida nomenklatuuri kaudu, mis järgib Rahvusvahelise puhta ja rakendusliku keemia liidu (Iupac) kehtestatud reegleid.
Loe ka: Süsinik - üks kõige rikkalikum element Universumis
Süsivesinike omadused

Polaarsus: süsivesinikud ilma heteroaatomite olemasoluta on apolaarne.
Molekulidevahelised jõud: süsivesiniku molekulide vahelised sidemed on seda tüüpi indutseeritud dipool.
sulamistemperatuur jakeemine: need varieeruvad vastavalt molekuli suurusele, funktsioonile ja struktuurilisele korraldusele.
füüsiline seisund: normaalsetes temperatuuri- ja rõhutingimustes on nelja või vähem süsinikuaatomiga süsivesinikud gaasilises olekus. 5 kuni 17 süsinikuga süsivesinikud on vedelas olekus ja enam kui 17 süsinikuga süsivesinikud on tahked ained.
Tihedus: on väiksem kui tihedus vett, st vähem kui 1,0 g / cm³.
Reaktsioonivõime: alifaatsed ja küllastumata süsivesinikud on halvasti reageerivad; küllastumata ühendid reageerivad tõenäolisemalt teiste molekulidega ja kuni viie süsinikuga tsüklilised süsivesinikud on väga reaktiivsed.
Ärge lõpetage kohe... Peale reklaami on veel;)
Süsivesinike klassifikatsioon
Süsivesinikud saab klassifitseerida keti struktuurse korralduse järgi ja asutuste poolt.Küllastumatus on kahe- või kolmiksideme olemasolu süsinike vahel, on pi tüüpi ühendused (π). juba oksad need on nagu “oksad”, mis on kinnitatud suurema süsivesinikstruktuuri külge. Tsüklilised ahelad võivad sisaldada ka harusid ja / või küllastumataid - suletud ahelaga süsivesinike struktuuriline korraldus moodustab muude hulgas hulknurki nagu ruut, kolmnurk, heksaan.
Aatomite paigutuse osas võib süsivesinik olla normaalse või hargnenud ahelaga.
→ C süsivesiniktavaline, sirge või sirge: stringiga, millel on ainult kaks otsa.

→ C süsivesinikvihkab hargnenud: see, millel on kett, millel on rohkem kui kaks otsa. Selleks, et teada saada, kus ja mis harud asuvad, on oluline põhikett õigesti valida. Peaahel peab sisaldama kõiki küllastumata ja heteroaatomeid (kui neid on), sama hästi kui kõige rohkem järjestikuseid süsinikke. Süsinikud, mis ei sisaldu peaahelas, on harud.
Näide:

Sulgemisel võib süsivesinikul olla suletud, avatud või segatud ahel.
→ Ahelaga süsivesinikuds suletud või tsükliline: need, millel on ahelad, milles aatomid ise organiseeruvad, moodustades tsükli, hulknurga või aromaatse ringi (suletud süsivesinik vahelduvate küllastumata). Ärge otsake lahti, kui pole haru. Hulknurga iga tipp tähistab süsinikku ja selle vastavaid vesiniksidemeid.
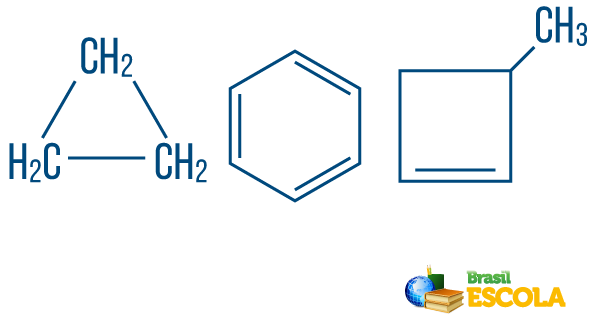
→ Avatud ahelaga või atsüklilised süsivesinikud: on need, mille ketid on vähemalt kahe otsaga.

→ Süsivesinik segatüüpi string: on moodustatud lineaarse osa külge kinnitatud tsükli või tsüklilise ahela abil; sellel on vähemalt üks ots.
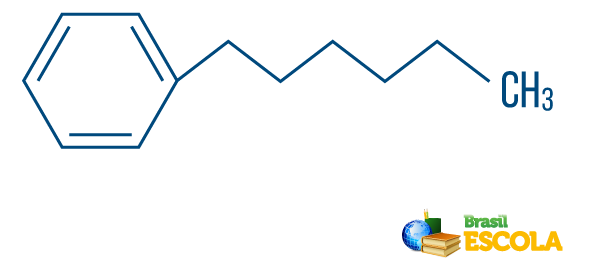
Loe ka: Aromaatsed süsivesinikud - näited ja omadused
Süsivesinike nomenklatuur
Igale süsivesinikutüübile kehtib Iupaci kehtestatud reegel. Nende ühendite nomenklatuur toimub järgmiselt:
1. osa: filiaali (filiaalide) asukoht ja nimi (kui on);
2. osa: kehtib termin tsükkel kui ühend on suletud ahel, kuid kui see on alifaatne (avatud) ahel, pole see vajalik;
3. osa: eesliide, mis näitab, kui palju süsinikke on peaahelas;
4. osa: molekuli küllastumatuse tüüpi tähistav asukoht ja infix;
5. osa: süsivesinike järelliide “o”.
Kui molekul on avatud struktuuriga, ilma hargnemiseta, algab nomenklatuur 3. osast.
Järgmine tabel näitab süsivesinike nomenklatuuri jaoks nõutavat teavet (ees-, järelliide ja järelliide) üldiselt. O eesliide varieerub sõltuvalt süsinike arvust; O infix, küllastumata arvude järgi; see on järelliide“O " Termin "süsivesinik" viitab ühenditele.
Eesliide |
Infix |
Liide |
||
1 süsinik |
kohtusime- |
Ainult üksikud kõned |
-ja- |
-O |
2 süsinikku |
et- |
|||
3 süsinikku |
prop- |
1 kaksikside |
-en- |
|
4 süsinikku |
aga- |
|||
5 süsinikku |
pent- |
2 kaksiksidet |
-dien- |
|
6 süsinikku |
kuus- |
|||
7 süsinikku |
hept- |
1 kolmekordne side |
sisse |
|
8 süsinikku |
okt- |
|||
9 süsinikku |
mitte- |
2 kolmiklinki |
-diin- |
|
10 süsinikku |
detsember |
Esimene samm orgaanilise ühendi nomenklatuuri avastamisel on tuvastada peaahel süsinikke, mis peavad sisaldama küllastumata ja võimalikult palju järjestikuseid süsinikke. Pärast peaahela tuvastamist süsinikud tuleb loendada - loendamise alustamine harudele ja küllastumata jäämistele (kui neid on) kõige lähemal. THE lokaliseerimine on selle süsiniku arv, kus haru või küllastumatus leitakse. Mõnikord on radikaalse või topelt- või kolmiksideme jaoks ainult üks võimalik asukoht, mistõttu pole vajalik ühendava süsiniku asukohta nomenklatuuris väljendada.

THE harude nomenklatuur antakse süsinike arvu järgi mõlemas pluss lõpetamine rida või ll. Kui harusid on rohkem kui üks, kasutatakse tähestikulist järjekorda.
Vaadake järgmisi näiteid:
→ Näide 1
CH3 - CH2 - CH3 → Propaan
1. osa: eesliide “prop-”Näitab, et ketil on kolm süsinikku.
2. osa: infix "-ja-”Annab märku, et molekul loob ainult seda tüüpi ühendusi sigma või lihtne.
3. osa: järelliide "-O”On iseloomulik süsivesinikele.
→ Näide 2
CH2= CH-CH2-CH3 → But-1-een
Küllastumata süsivesinikel on vaja loendada ja leida süsinik, milles paar leidub, ja numeratsioon peab olema võimalikult väike. Selleks peab süsinikuarv algama kaksiksidemele kõige lähemal asuvast küljest.
1. osa: "aga-" näitab, et ahelas on neli süsinikku.
2. osa: "1-et" Termin "süsinik 1" tähistab küllastumatust, mis asub süsiniku 1 ja 2 vahel.
3. osa: "-O" on süsivesinike iseloomulik järelliide.
→ Näide 3

1. osa: "3-etüül" annab märku, et süsinikul 2 on kahe süsinikuga haru.
2. osa: "pent" näitab viie süsiniku olemasolu peaahelas.
3. osa: "-an-" on küllastumata ahelatele rakendatav infiks (ei topelt- ega kolmiksidemeid).
4. osa: "-O" on süsivesinike iseloomulik järelliide.
→ Näide 4
Ketidega koos rohkem kui üks haru, asetage radikaalid nomenklatuuri tähestikulises järjekorras. Kui samas molekulis on harusid ja küllastumata küllastumisi, tuleks süsinike arv peaahelas teha nii, et asukohanumbrite summa oleks võimalikult väike.
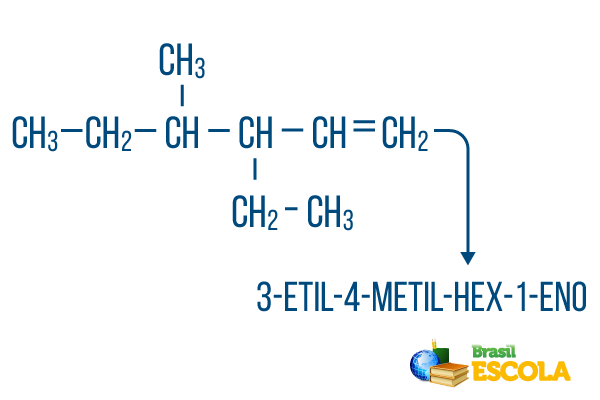
Peamise ahela süsinikuarvestus tehti vasakult paremale ning küllastumata ja haru asukoha numbrite summa on: 1 + 4 + 3 = 8. Kui süsiniku arv oleks olnud paremalt vasakule, oleks liitnomenklatuur 4-etüül-3-metüül-5-een, mille asukohtade summa oleks: 4 + 3 + 5 = 12, mis on suurem kui teine hüpotees, seega ei tohiks seda kasutada.
1. osa: 3-etüül-4-metüül viitab radikaalidele tähestikulises järjekorras ja nende vastavale asukohale.
2. osa: kuus- tähendab, et peaahelas on 6 süsinikku.
3. osa: 1-et tähistab kaksiksideme olemasolu süsinikul 1.
4. osa: "-O" on süsivesinike iseloomulik järelliide.
→ Näide 5
Suletud stringide puhul kehtivad nimereeglid, kuid sõna tsükkel algab ühendi nimi, näidates, et see on suletud või tsükliline süsivesinik.
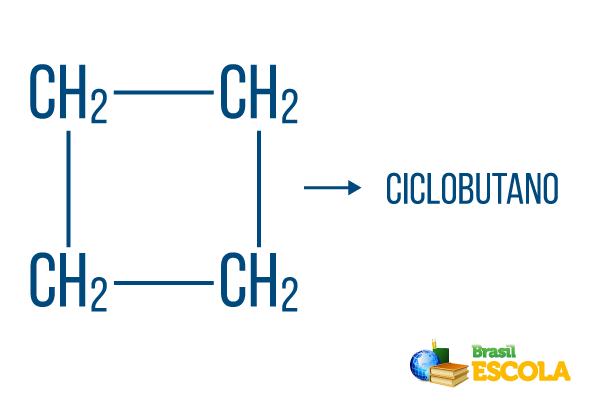
1. osa: tsükkel- näitab, et see on suletud string.
2. osa: -aga- tähistab 4 süsiniku olemasolu ahelas
3. osa: -Oon süsivesinike iseloomulik järelliide.
Loe ka: Süsinikuahelate klassifikatsioon
Süsivesinike tüübid
Süsivesinikke võib jagada alkaanideks, alkeenideks, alküünideks ja alkadieenideks, mis on klassifitseeritud kui vastavalt ahela loomisele (kaksik- või kolmiksidemed) - ja tsüklaanid, mis on ahelad suletud.
→ Alkaanid: on süsivesinikud, millel pole küllastumata. Alkaanide üldvalem on CeiH2n + 2, ja eiomenklatuur selle koostas eesliide + an + O.
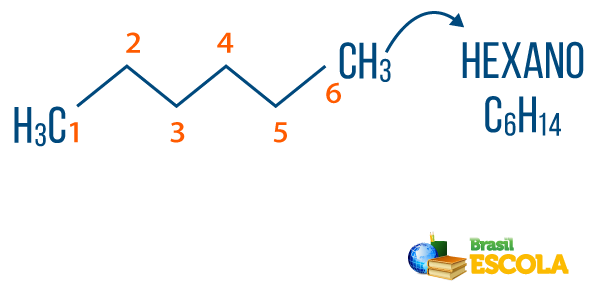
Sina alkaanid võib leida loodusest, nagu gaas metaan (CH4), mille loomad eraldavad ja toodavad laguprotsessides, samuti rafineerimistehastes ja naftakeemiatööstuses. Sellised ühendid nagu propaan (Ç3H7), butaan (Ç4H10), mis moodustab meie keedugaasi (LPG) ja oktaanarv (Ç8H18), mis on autokütuses, on ettevõtte kõrvalsaadused Nafta.

→ alkeenid või alkeenid: kas süsinikuahelad on küllastumata, kaksiksidemed. Selle üldvalem on CeiH2n, ja sinu eiomenklatuur selle koostas Pparandama + et + o.

O etüleengaas (Ç2H4), mida kasutatakse põllumajanduses puuviljade küpsemise kiirendamiseks, kuulub funktsiooni alkeen. Ühendit kasutatakse ka tooraine tootmisel polüetüleen, mida kasutatakse plastnõude valmistamiseks.
→ Alküünid või atsetüleen: kolmiksidemega süsivesinikud. Selle üldvalem on CeiH2n - 2. THE nomenklatuur selle koostas eesliide + sisse + o.

O atsetüleen või etiin (C2H2) on alküünfunktsiooni gaas, mida kasutatakse keevisõmblused ja metallilõiked. Selle ühendi temperatuur võib ulatuda kuni 3000 ° C-ni, mis võimaldab remonti teostada laeva sukeldatud osades.

→ alkadieenid või dieenid: süsinikahelad, millel on kaks küllastumata, see tähendab, et süsinike vahel on kaks kaksiksidet. Selle funktsiooni üldvalem on C.eiH2n - 2. Mõistke, et see on sama valem kui alküünidel, mis tähendab, et see võib juhtuda isomeeria ühendite vahel (sama molekulivalem erinevatele ühenditele).
Alkadieeni nomenklatuur koosneb Pparandama + dien + o.
Näide:

→ Suletud ahelaga süsivesinikud: molekulid organiseeruvad ise tsükliliselt, kipuvad moodustama hulknurka ja nagu ka avatud ahelates, võivad esineda asutused ja / või tagajärjed. Tsüklonid, tsükleenid, tsükliinid ja benseenid on suletud ahelaga süsivesinikud.
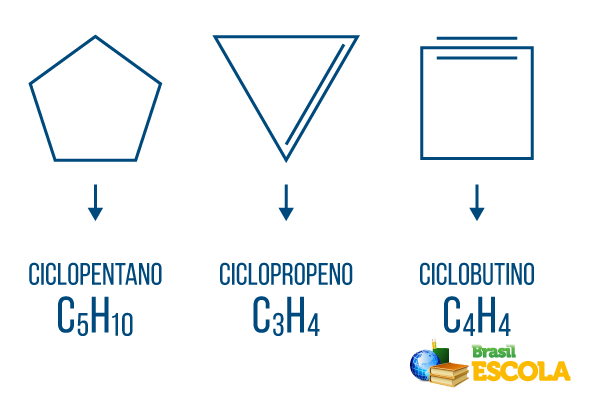
Tsüklonid või tsükloalkaanid: tsüklilised ahelad, mis koosnevad ainult üksiksidemetest. Selle üldvalem on CeiH2n. Nomenklatuur: ciclo + eesliide + an + o.
Tsüklid või tsükloalkeenid: ettevõttega suletud süsivesinikahelad. Selle üldvalem on CeiH2n-2. Nomenklatuur: çiclo + prefiks + et + O.
-
Tsükliinid või tsükloalküünid: suletud ahelaga süsivesinikud kahe kaksiksideme olemasolul. Selle üldvalem on CeiH2n-4. Nomenklatuur: çiclo + eesliide + sisse + o.
benseenid
Benseen on suletud ahelaga süsivesinike tüüp kuus süsinikku kus võlakirjad varieeruvad ühe- ja kahekordse vahel. Need ühendid on mürgine ja väga kantserogeenne, mida kasutatakse keemiliste protsesside käigus orgaaniliste lahustitena.
Selleks, et süsivesinikku saaks pidada aromaatseks, peab see olema vähemalt üks benseeni ring, mis on väga reaktsioonivõimeline, seetõttu allub kahele või enamale asendused, mida näeme siin kui tagajärgi. Kui on kaks ühendavat radikaali, on meil iga positsioonipaari jaoks konkreetsed nimed.
Radiaalid 1,2 süsiniku benseenil → orto
Radikaalid benseeni 1,3 süsiniku juures → eesmärk
Radiaalid benseeni süsinikul1,4 → eest
Aromaatse ühendi anomenklatuur tehakse järgmiselt:
1. osa: ligandide positsioneerimine (orto, eesmärk või).
2. osa: benseeniga seotud radikaali või radikaalide nimetus (metüül, etüül, propüül…). Radikaalidele antud nimi järgib teiste süsivesinike reeglit.
- 3. osa: -Bmürk, mis on aromaatsete süsivesinike iseloomulik termin.
Näited:
→ Orto-dimetüülbenseen

1. osa: Orto- näitab, et radikaalid paiknevad süsinikel 1 ja 2.
2. osa: -dimetüül- Termin "radikaal" tähistab kahte radikaali, millel on mõlemad üks süsinikuaatom.
3. osa: -benseen on aromaatsete süsivesinike iseloomulik termin.
→ Orto-etüül-metüül-benseen
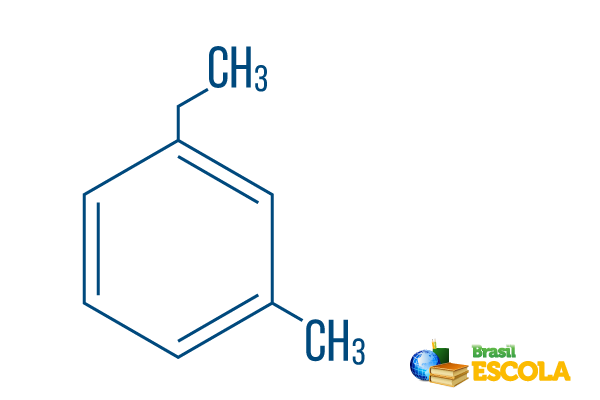
1. osa: moh- näitab, et radikaalid on paigutatud süsinikele 1 ja 3.
2. osa: etüülmetüül- Termin "süsinikuaatom" tähistab süsiniku hulka igas radikaalis, olles etüül The kahe süsiniku haru ja metüül ühe süsinikuga hargnev - paigutatud nomenklatuuri tähestikulises järjekorras.
3. osa: -benseen on aromaatsete süsivesinike iseloomulik termin.
→ Para-dietüülbenseen
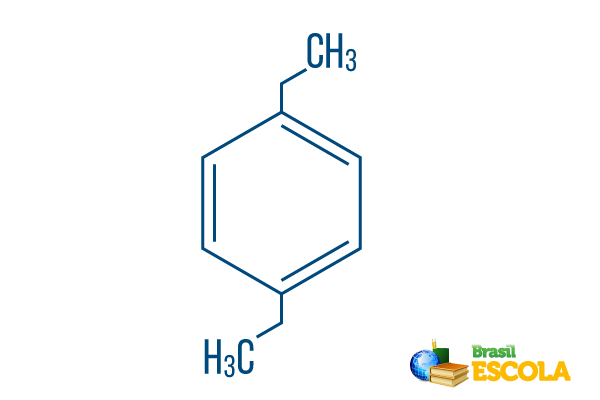
1. osa: Pader- näitab, et radikaalid on benseeni süsinikel 1 ja 4.
2. osa: -dietüül- viitab kahele seda tüüpi radikaalile etüül, see tähendab kaks haru kahe süsinikuga.
3. osa: -benseen on aromaatsete süsivesinike iseloomulik termin.
Loe ka:Benseeni struktuuri avastamine
lahendatud harjutused
(Unesp) - Oktaan on süsivesinike segu bensiini üks peamisi koostisosi. Oktaani molekulaarne valem on:
a) C8H18
b) C8H16
c) C8H14
d) C12H24
e) C18H38
Vastus: täht a). Liitnomenklatuuri analüüsimine oktaanarv, see on alkaan, see tähendab molekul, mis koosneb ainult üksiksidemetest. Kui alkaanide üldvalemiks on CeiH2n + 2, asendades kaheksa, mis on süsinikukogus põhiahelas - ja antud juhul ainulaadne, asendades n -, saame teada, et oktaani molekulaarne valem on C8H18.
(UFSCar-SP) - Mõelge järgmistele väidetele süsivesinike kohta.
I) Süsivesinikud on orgaanilised ühendid, mis koosnevad ainult süsinikust ja vesinikust.
II) Alkaanideks nimetatakse ainult sirge ahelaga küllastumata süsivesinikke.
III) Tsükloalkaanid on küllastunud alifaatsed süsivesinikud üldvalemiga CnH2n.
IV) on aromaatsed süsivesinikud: bromobenseen, p-nitrotolueen ja naftaleen.
Järgmised väited on õiged:
a) ainult mina ja III.
b) Ainult I, III ja IV.
c) ainult II ja III.
d) ainult III ja IV.
e) ainult I, II ja IV.
Vastus: Kiri a).
II - alkeenid on kaksiksidemega, st küllastumata ühendid, kuid nende ahelas võivad olla hargnemised, mitte ainult lineaarsed.
IV - brometobenseen ja p-nitrotolueeni ühendid kuuluvad teistesse orgaanilised funktsioonid.
autor Laysa Bernardes
Keemiaõpetaja