Daltoni seadus ütleb, et iga gaasisegu gaasi osaline rõhk on võrdne rõhuga, mida see avaldaks segu mahu hõivamiseks samal temperatuuril. Seetõttu on gaasisegu kogurõhk iga seda moodustava gaasi osarõhkude summa.
Vaatleme kahte tüüpi gaase, A ja B. Neil kõigil on sama ruumala V ja sama temperatuur T. Kui rakendame Clapeyroni võrrandit kahele gaasile A ja B, on meil:
PTHE. V = nTHE .R .T ja lkB. V = nB .R .T
Nagu ülaltoodud joonisel näidatud, kui segame kahte gaasi, tuleb segus olevate gaaside moolide arv (eim) saab:
eim= nTHE+ nB
Kus:
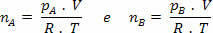
Kuid nm = (Pm.V) / R. T; nii et meil on:
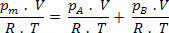
Tehes ülaltoodud avaldises mõningaid lihtsustusi, on meil:
Pm= lkTHE+ lkB (Daltoni seadus)
Sama põhjendust saame rakendada erineva mahu ja temperatuuriga gaaside puhul. Vaatame allolevat joonist, kus kahel tühise mahuga toruga ühendatud õhupallil on kontaktkraan. Nendel õhupallidel on kaks gaasi A ja B, mille temperatuur ja maht erinevad üksteisest. Jooniselt näeme, et kraan on suletud, seetõttu:
Ärge lõpetage kohe... Pärast reklaami on veel rohkem;)
PTHE. V = nTHE .R .T ja lkB. V = nB .R .T
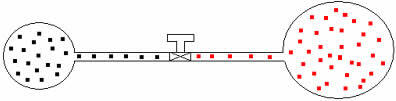
Hiljem, kui kraan avada, näeme, et gaasid segunevad, nagu on näidatud alloleval joonisel:
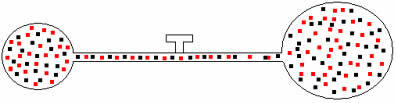
Selle segu jaoks on meil järgmised seosed:
Vm= VTHE+ VB
PTHE. V = nTHE .R .T
PB. V = nB .R .T
Nii et meil on selle segu lõplikku suhet laiendada segule ei gaasid. Seega:
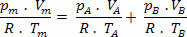
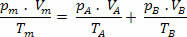
Autor Domitiano Marques
Lõpetanud füüsika
Brasiilia koolimeeskond
Kas soovite sellele tekstile viidata koolis või akadeemilises töös? Vaata:
SILVA, Domitiano Correa Marques da. "Gaasisegu"; Brasiilia kool. Saadaval: https://brasilescola.uol.com.br/fisica/mistura-gasosa.htm. Juurdepääs 27. juunil 2021.