aatom on aine põhiühik, see tähendab väikseim osa, milleks saab elemendi jagada, kaotamata selle keemilisi omadusi.
Aatomid moodustavad tuum, mis koosneb prootonite ja neutronite osakestest ning elektronidest, mis tuuma ümber tiirlevad, moodustades elektrosfääri.
Sõna aatom on Kreeka päritolu ja tähendab "jagamatut". Kuni 19. sajandini usuti, et aatom on aine väikseim osa, see tähendab, et seda on võimatu jagada.
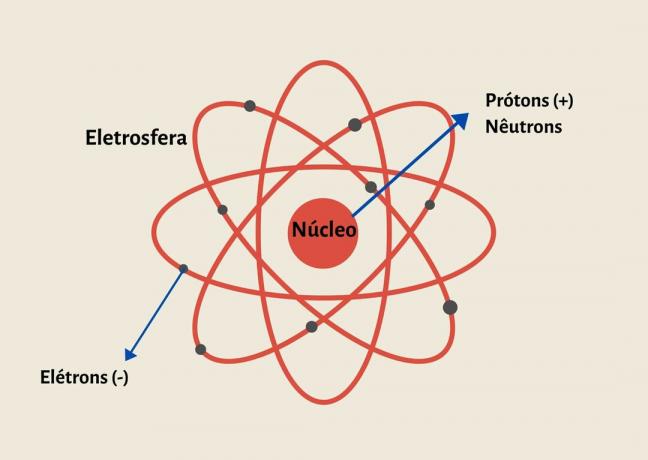
Aatom koosneb prootonitest ja neutronitest tuumas ja elektronidest elektrosfääris.
Aatomi struktuur ja koostis
Aatomid on väga väikesed ainetükid, nii väikesed, et neid ei saa tavaliste mikroskoopidega näha.
Selle struktuuri moodustavad lõpmatult väike ja tihe tuum, mis koosneb prootonitest ja neutronitest, ja elektrosfäär, mis koosneb elektronidest.
- Prootonid (p): positiivsed osakesed ja ühiku massiga.
- Neutronid (n): neutraalsed osakesed (laenguta) ja ühiku massiga.
- Elektronid (e): negatiivsed ja praktiliselt massivabad osakesed pidevas orbiidi liikumises tuuma ümber.
Tuum moodustab 99,9% aatomi massist. Elektronide massil pole praktiliselt mingit tähtsust: elektroni mass on 1836 korda väiksem kui prootonite ja neutronite mass.
Elektronide liikumine tuuma ümber moodustab a elektromagnetväli. Elektronid tiirlevad tuuma ümber nii suure kiirusega, et kui näete aatomit, nähakse elektrosfääri tuuma ümber oleva pilvena.
Aatomid on elektriliselt neutraalsed - neil on sama absoluutväärtus kui prootonitel (+) ja elektronidel (-), mistõttu nende laeng muutub nulliks.
Kui aatom võtab vastu või kaotab elektrone, lakkab ta olemast aatom ja muutub a-ks ioon, millel võib olla positiivne või negatiivne laeng:
- Kui see võtab vastu elektrone, laetakse see negatiivselt ja muutub a-ks anioon.
- Kui see kaotab elektrone, muutub see positiivselt laetud ja muutub a katioon.
aru saada, mis see on asja ja saate lisateavet katioonid ja anioonid.
Elektrosfääri struktuur
Elektrosfääri moodustavad orbiidi liikumises olevad elektronid, kuid need elektronid ei ole juhuslikult paigutatud, vaid on elektroonilised kihid kus need osakesed jaotuvad.
Aatomil võib olla kuni seitse elektroonilist kihti. Kõigil neil kihtidel on erinev energiatase, kusjuures välimine kiht on kõige energeetilisem kiht.
Neid kihte tähistavad järgmised tähed: K, L, M, N, O, P, Q. K on südamikule lähim kiht.
Kõigil aatomitel pole 7 kihti, näiteks elavhõbedal on ainult 6. Kuid olenemata kestade arvust on reegel, et viimases ei tohi olla rohkem kui 8 elektroni.
Elektroonilised kihid jagunevad veelgi energia alatasemed, mida tähistavad tähed: s, p, d, f.
Aatomi ajalugu ja aatomimudelid
Idee, et ainet võib jagada väikesteks osadeks, kuni see jõuab nii väikese üksuseni, et seda ei saa enam jagada, eksisteeris juba Kreeka antiikajast.
Demokritos, umbes 400 eKr C. oli esimene teadlane, kes postuleeris selle väikese osakese olemasolu ja nimetas selle „aatomiks“, mis kreeka keeles tähendab „jagamatut“.
Esimene aatomite teooria töötati välja 1803. aastal. John Dalton väitis, et aatom on aine väikseim osa ja see on jagamatu.
Järgnevate sajandite jooksul tehti teaduse ja tehnika arenguga selle osakese kohta uusi avastusi ja postuleeriti erinevates aatomimudelites.
1803 - Daltoni mudel
Professor John Daltoni poolt 1803. Aastal välja töötatud mudel sai tuntuks "basseinipall", sest tema sõnul olid aatomid massiivsed, jagamatud ja hävimatud sfäärid.

1898 - Thomsoni mudel
Joseph Thomson avastas elektronide olemasolu ja tema mudeli järgi jaotuksid need laengud positiivse laenguga kogu aatomisse ühtlaselt.
Thomsoni mudeli aatom oli pigem sfääriline kui massiline ja sai nimeks "rosinapuding", kus pudingu rosinad esindasid positiivseid ja negatiivseid laenguid.

1911 - Rutherfordi mudel
Rutherford tegi aatomi kohta olulise avastuse: tuuma olemasolu. Tema mudel ütles, et aatom koosnes tuumast ja elektrosfäärist.
Tuumas oleksid prootonid ja neutronid ning elektrosfääris elektronid. See mudel sai nimeks "Päikesesüsteem".
Mida Rutherford ei suutnud seletada, oli see, kuidas elektronid ei lagunenud aatomi tuumaga.

1913 - Rutherford-Bohri mudel
Rutherfordi mudelit täiendati füüsiku Niels Bohri 1913. aastal tehtud avastustega. Bohr jõudis järeldusele, et elektronid tiirlevad elektrosfääri ümber erineva energiatasemega kihtides.
Elektroonid ei ima ega eralda selles liikumises energiat, seega jäävad nad pidevale orbiidile, mis takistab neil tuumaga kokku põrkamast.

Aatomi omadused
Mis eristab ühte aatomit teisest, on prootonite, neutronite ja elektronide hulk selle koostises. Peamised aatomite tuvastamiseks kasutatavad väärtused on aatommass ja aatomnumber.
aatommass
Aatomimassi väärtust esindab aatomi tuumas leiduvate prootonite ja neutronite summa.
A = z + n
aatomnumber
Aatomnumber on prootonite arv aatomi tuumas, selle väärtust tähistab täht z. Kuna aatomis on prootonite arv võrdne elektronide arvuga, on meil:
z = p = e
Mitmest sama aatomnumbriga aatomist moodustub a keemiline element. Kõik teadaolevad keemilised elemendid on perioodilisustabelis esindatud aatomite arvu järjest kasvavas järjekorras.
Keemilised elemendid on perioodilisustabelis esindatud nende akronüümi ja nimega keskel, aatommassi allosas ja aatomnumbriga ülaosas, nagu on näidatud pildil:

- Aatomimass = 196,967
- Aatomnumber = 79
Aatomid ja molekulid
Aatom on aine väga väike osa, see koosneb tuumast, mille prootonid ja neutronid ning tuuma ümber pöörlevad elektronid.
Molekul on ühesuguste või erinevate elementide aatomite rühm, mis kokku moodustavad aine. Näiteks:
- Kaks hapniku aatomit ühinevad ja moodustavad hapniku molekuli (O2).
- Kaks vesiniku aatomit ühinevad ühe hapniku aatomiga ja moodustavad veemolekuli (H2O).
Vaadake ka:
- Molekulid
- Linus Paulingi diagramm


