Mõelge allpool toodud üldisele pöörduvale reaktsioonile, kus väiketähed vastavad tasakaalustatud reaktsioonikoefitsientidele, suurtähed on reaktiivid ja saadused on kõik gaasilised:

Arvestades kõiki reaktsioonisuundi eraldi, on nende arengukiirused (Td) antud järgmiselt:
* Otsene reaktsioon: aA + bB → cC + dD
Kõikotsene = Kotsene. [THE]The. [B]B
* Pöördreaktsioon: cC + dD → aA + bB
Kõiktagurpidi = Ktagurpidi. [Ç]ç. [D]d
Keemiline tasakaalukonstant kontsentratsiooni osas aine koguses (Kç) ja osalise rõhu osas (KP) antakse jagades Kotsene autor Ktagurpidi.
Nii et meil on:
Kotsene. [THE]The. [B]B = 1 → Kotsene__ = __[Ç]ç. [D]d___
Ktagurpidi. [Ç]ç. [D]d Ktagurpidi [THE]The. [B]B
Olles Kç =_Kotsene_
Ktagurpidi
Nii et meil on:
Kç =__[Ç]ç. [D]d___ või K.P =__(Praça)ç. (pD)d___ |
Kus p on iga aine osarõhk tasakaalus.
Sel viisil tõstetakse iga kontsentratsioon eksponendini, mis vastab vastava aine koefitsiendile reaktsioonis, ja Kç pole ühikut *.
Lisaks tuleb selles avaldises välja tuua väga oluline aspekt
tahkeid komponente ega puhtaid vedelikke ei tohiks esitada., kuna selles väljendis osalevad ainult need asjad, mis võivad varieeruda. Tahkes olekus on aine kontsentratsioon aine koguses konstantne ja sisaldub seega juba K enda väärtuses.ç. Sama kehtib puhaste vedelike nagu vee kohta. Lühidalt, ekspressioonis osalevad ainult gaasilises olekus ja vesilahuses olevad ained.Ärge lõpetage kohe... Peale reklaami on veel;)
Pange tähele allpool olevaid näiteid:
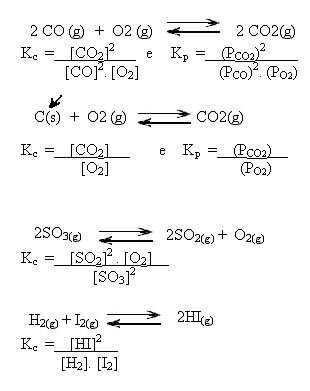
K väärtusedç näitab meile, kas reagentide ja saaduste kontsentratsioon on sama või kui üks on suurem kui teine:
- kui Kç või K.P on võrdne ühega (Kç = 1), see tähendab, et reagentide ja saaduste kontsentratsioon on võrdne;
- kui väärtus Kç või K.P ole pikk, see tähendab, et produkti kontsentratsioon on suurem, kuna Kç tooted on loendis;
- kui väärtus Kç või K.P on madal, see tähendab, et reaktiivid on suuremas kontsentratsioonis, kuna K ekspressioonisç reaktiivid on nimetavas.
* Kç ja K.P need on mõõtmeteta arvud, see tähendab puhtad arvud, mille ühik pole seotud ühegi suuruse ega suuruste vahelise seosega.
Autor Jennifer Fogaça
Lõpetanud keemia
Kas soovite sellele tekstile viidata koolis või akadeemilises töös? Vaata:
FOGAÇA, Jennifer Rocha Vargas. "Tasakaalukonstandid Kc ja Kp"; Brasiilia kool. Saadaval: https://brasilescola.uol.com.br/quimica/constantes-equilibrio-kc-kp.htm. Juurdepääs 28. juunil 2021.



