Sina karboksüülhapped on orgaanilised ühendid, mida iseloomustab karboksüül (COOH) olemasolu, on tsitrusviljades, äädikas, farmaatsiatoodetes ja säilitusainetes.
Sina happed karboksüülrühm osaleda reaktsioonides, esterdamisena, mida kasutatakse muu hulgas lõhna- ja maitseainete tootmiseks. Selle funktsionaalse rühma ühendite omadused on erinevad. vastavalt süsinikuahela suurusele ja struktuurile.
Loe rohkem: Atsetüülsalitsüülhape - ühend karboksüülhappe ja esterrühmadega

Karboksüülhapete omadused
- Karboksüülhappeid esindab keemiliselt RCOOH või CO2H, kus R on orgaaniline radikaal seotud karbonüülrühma (C = O) ja hüdroksüülrühma (-OH) külge.
- Karboksüül (-COOH) olemasolu annab erinevuse polaarsus molekuli külge, muutes selle polaarseks ühendiks.
- THE lahustuvus ja välimus varieeruvad sõltuvalt ahela süsinike arvust. Karboksüülhapped koos:
- kuni neli süsinikku on värvusetud ja vedelad, veega segunevad;
- viis kuni üheksa süsinikku on viskoossed vedelikud, värvusetud, vees halvasti lahustuvad;
- 10 või enam süsinikku on valge tahke aine, vees lahustumatu.
- Kuni kuue süsinikuga avatud ahelaga happed on tugeva lõhnaga ja iseloomulikud rääsunud võile, need on suhteliselt lenduvad.
- Karboksüülhape on orgaaniline funktsioon, millel on kõige rohkem rõhutatud happe iseloom, selle funktsiooni ühendite pH on vahemikus 3 kuni 5.
Karboksüülhapete klassifikatsioon
Karboksüülhappeid saab klassifitseerida molekulis sisalduvate karboksüülide arvu järgi:

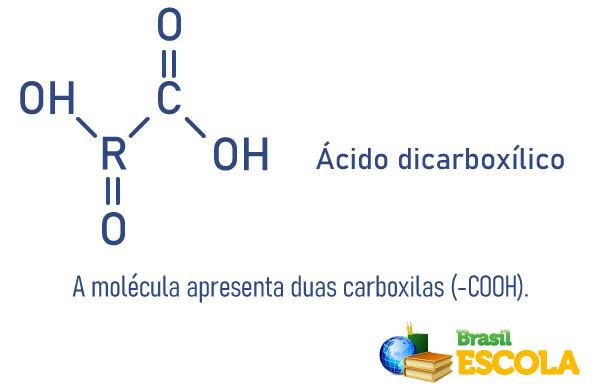
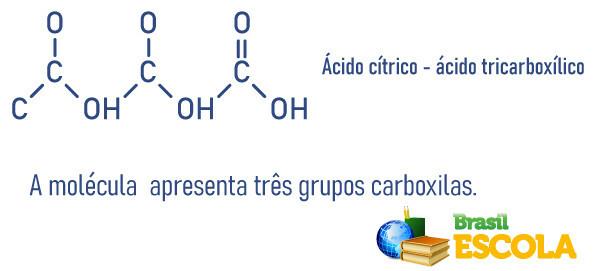
Vaadake ka:Väävelhape - aine, mida tööstused laialdaselt kasutavad
Karboksüülhapete nomenklatuur
Karboksüülhapete nomenklatuuri iseloomustab Rahvusvahelise Puhta ja Rakendatud Keemia Liidu (Iupac) andmetel funktsioon alustage terminiga hape ja lõpeb järelliitega -oic.
Reeglid selle rolli nomenklatuur, sest see on a orgaaniline funktsioon, st süsinikuahela olemasolu tõttu:
1. samm: loenda peaahela süsinikud, alustades otsast, kus karboksüül (-COOH) asub. Nomenklatuuri eesliide antakse vastavalt peaahela süsinike arvule.
2. samm: nimetage ja leidke oksad: eesliide (süsinike arv) + lõpp (-il või -ila). Kui ahelas on rohkem kui üks haru, tuleb need paigutada tähestiku järgi nimetamisse.
3. samm: kontrollida ettevõtete olemasolu ahelas.
Tähelepanek: Eesliiteid di-, tri- või penta- kasutatakse kahe, kolme või nelja sama liigi rühma esinemise väljendamiseks. Näide: diohape two kahe karboksüülrühma olemasolu.
Vaadake allolevast tabelist, kuidas peaks karboksüülhapete nomenklatuur olema üles ehitatud:
Eesliide (süsinike arv) |
Infix (ahela küllastus) |
Sufiks (funktsionaalne rühm) |
||||
Hape |
1 süsinik |
Kohtusime- |
Ainult üksikud kõned |
-ja- |
karboksüülhape |
-Tere kaas |
2 süsinikku |
Et- |
|||||
3 süsinikku |
Prop- |
1 kaksikside |
-en- |
|||
4 süsinikku |
Aga- |
|||||
5 süsinikku |
pent- |
2 kaksiksidet |
-dien- |
|||
6 süsinikku |
Hex- |
|||||
7 süsinikku |
Hept- |
1 kolmekordne side |
sisse |
|||
8 süsinikku |
Okt- |
|||||
9 süsinikku |
Mitte- |
2 kolmiklinki |
-diin- |
|||
10 süsinikku |
Detsember |
Näited:



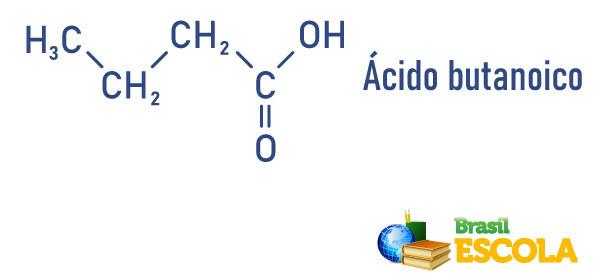


Karboksüülhapped esinevad igapäevaelus
- Süsinikhape (OHCOOH): sisalduvad veres ja gaseeritud jookides.
- Äädikhape või etanool (CH3COOH): äädikas.
- Või- või butaanhape (CH3(CH2)2COOH): piimas ja piimatoodetes.
- sipelghape või metanoolne (HCOOH): esinevad punase sipelga mürgis.
- Palder- või pentaanhape (CH3(CH2)3COOH): ravim, mida kasutatakse rahustava / rahustina, kasutatakse ka akne ravis.
- Bensoehape või karboksüülbenseen (Ç6H5COOH): kasutatakse toiduainetööstuses säilitusainena ja meditsiiniliselt fungitsiidina.
- Sidrunhape või 2-hüdroksü-1,2,3-propaantrikarboksüülhape: esineb tsitrusviljades, nagu apelsin ja sidrun.
Vaadake ka: Näpunäitedkui happe tugevus

Happelised reaktsioonidkarboksüülrühm
dimeerid
Karboksüülhapped kipuvad läbi moodustamine vesiniksidemed, moodustades dimeeri, milles kaks molekuli hakkavad käituma nagu üks ainult molekul, kahekordse molekuliga molekulmass.
Neutraliseerimisreaktsioon
karboksüülhapped reageerida alused, moodustades karboksüülitud soolad või orgaanilised soolad. Vaadake reaktsiooni üldvalemitega allpool, pidage R orgaaniliseks radikaaliks ja A kui a metallist:
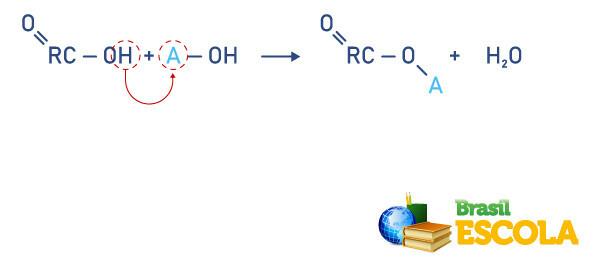
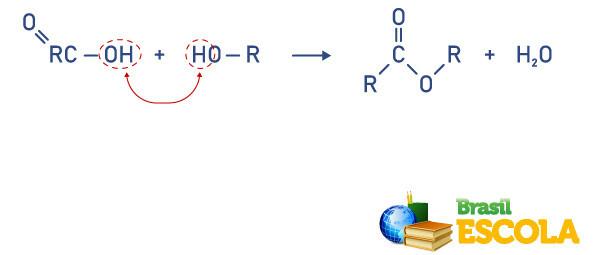
esterdamisreaktsioon
Seda tüüpi reaktsioone kasutatakse peamiselt lõhna- ja maitseainete tootmisel, see toimub molekuli vahel karboksüülhape ja a alkohol, moodustades a ester ja molekul Vesi.
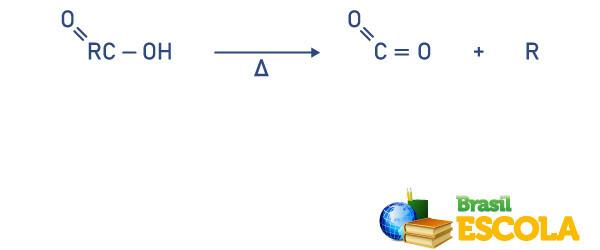
Dekarboksüülimisreaktsioon
Seda tüüpi reaktsioonides on karboksüüli eemaldamine happest, millel on tootena süsinikdioksiid see on alkaan või alkeen, alküün, orgaaniline molekul, mis on saadud happe karboksüüli siduvast radikaalist, vt:
lahendatud harjutused
Küsimus 1 - Karboksüülhapete puhul märkige alternatiiv INCORRECT.
A) Karboksüülhapped on orgaanilised molekulid, millel on karboksüülfunktsionaalne rühm (-COOH).
B) Karboksüülhappe süsinikuahela suurus määratleb sellised omadused nagu välimus, sulamistemperatuur ja tihedus.
C) Karboksüülhapped võivad kuumutades läbida dekarboksüülimisreaktsiooni, vabastades süsinikdioksiidi ja molekuli algse molekuli orgaanilisest rühmast.
D) Propaanhapet tuntakse ka sipelghappena, seda ainet leidub punaste sipelgate mürgis.
E) Trikarboksüülhapped on orgaanilised ühendid, milles molekulil on kolm karboksüülrühma. Trikarboksüülhape, mida on meie igapäevaelus väga palju, on sidrunhape, mida leidub puuviljades nagu sidrunid ja apelsinid.
Resolutsioon
Alternatiiv D Propaanhape ei ole sama mis sipelghape. Sipelghappe Iupaci nomenklatuur on: metaanhape - molekul, mis koosneb ainult ühest süsinikust.
2. küsimus - Järgmine molekul on monokarboksüülhape, kirjutage alla alternatiivile, mis sisaldab Iupaci järgi õiget nomenklatuuri.

A) Propaanhape
B) monobutaanhape
C) butaanhape
D) 1-metüülbutaanhape
E) 3-metüülbutaanhape.
Resolutsioon
Alternatiiv E. Süsinikuarvestus peab algama karboksüülsüsinikust, nii et meil on ketis neli süsinikku, mis vastavad eesliitele “but-”. Molekul on küllastunud, see tähendab, et sellel ei ole topelt- ega kolmiksidemeid, seega kasutame infiksi „-an-”. Metüülharu asub süsiniku kolmes, seega on vastavaks nomenklatuuriks 3-metüülbutaanhape.
Autor Laysa Bernardes Marques de Araujo
Keemiaõpetaja
Allikas: Brasiilia kool - https://brasilescola.uol.com.br/quimica/acidos-carboxilicos.htm
