THE EsiteksSeadusannabTermodünaamika on rakenduse põhimõttelannabkaitseannabenergia termodünaamiliste süsteemide jaoks. Selle seaduse kohaselt on variatsioon siseenergia termodünaamilise süsteemi erinevus on kuumus neelab süsteem ja selle tehtud töö.
Vaataka:Termoloogia põhimõtted ja kokkuvõte
Mis on termodünaamika esimene seadus?
Esimene termodünaamikaseadus on energiasäästu põhimõtte otsene tagajärg. Selle põhimõtte kohaselt süsteemi koguenergiajääb alati konstantseks, kuna ta pole kadunud, vaid muutunud.
Kohaldamisala Termodünaamikakasutatakse täpsemad mõisted ja vähem üldised kui need, mida kasutatakse energiasäästu põhimõttes. Termodünaamika esimeses seaduses kasutame selliseid mõisteid nagu energiasisemine,kuumus ja töö, mis on asjakohased programmi Soojusmasinad (termodünaamika seisukohalt olulise tähtsusega tehnoloogilised rakendused).

Kujutage ette auruga töötavat masinat, kui selle masina töövedelik (veeaur) saab soojust välisest allikast, on võimalik kaks energiamuundamist: aurul võib olla oma
temperatuur mõne kraadi võrra suurenenud või isegi võib laienema ja liigutage selle masina kolbe, sooritades nii teatud koguse töö."Termodünaamilise süsteemi siseenergia varieeruvus vastab selle neeldunud soojushulga ja selle süsteemi töö vahelise vahe erinevusele."
Ärge lõpetage kohe... Peale reklaami on veel;)
Termodünaamika esimese seaduse valem
Termodünaamika esimese seaduse matemaatiliseks kirjeldamiseks kasutatud valem on toodud allpool:

U - energia sisemine variatsioon (cal või J)
Q - soojus (lubi või J)
τ - töö (lubi või J)
Selle valemi kasutamiseks peame pöörama tähelepanu mõnele signaalireeglile:
ΔU - on positiivne, kui süsteemi temperatuur tõuseb;
ΔU - on negatiivne, kui süsteemi temperatuur langeb;
Q - on positiivne, kui süsteem neelab soojust väliskeskkonnast;
Q - see on negatiivne, kui süsteem annab väliskeskkonnale soojust;
τ – on positiivne, kui süsteem laieneb, tehes väliskeskkonnaga seotud tööd;
τ – see on negatiivne, kui süsteem sõlmib lepingu, saades tööd väliskeskkonnast.
energia sisemine variatsioon
Termin ΔU viitab energia muutusele, mis on omistatud energiale kineetiline energia süsteemi ideaalosakestest võib ideaalse gaasi korral öelda, et ΔU on samaväärne:
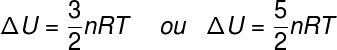
ei - moolide arv (mol)
R - ideaalsete gaaside universaalne konstant (0,082 atm.l / mol. K või 8,31 J / mol. K)
T - absoluutne temperatuur (kelvin)
Valemeid analüüsides on näha, et kui süsteemis temperatuurimuutust ei toimu, siis selle siseenergia jääb samuti muutumatuks. Lisaks on oluline öelda, et tsükliliselt töötavate termiliste masinate puhul siseenergia variatsioon peab iga tsükli lõpus olema null, sest sel hetkel naaseb mootor algtemperatuuriga.
Vaataka:Soojusmasinate jõudlus: kuidas see arvutatakse?
Kuumus
Järgmisele terminile Q, mis viitab süsteemile ülekantud soojushulgale, liigume tavaliselt kalorimeetria põhivõrrand, näidatud allpool:
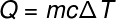
Q -kuumus (lubi või J)
m - mass (g või kg)
ç - erisoojus (cal / gºC või J / kg. K)
ΔT - temperatuuri kõikumine (celsius või kelvin)
Töö
Esimene termodünaamika esimese seadusega seotud suurustest on töö (τ), millel on a analüütiline valem ainult muutustele, mis toimuvad pideva rõhu all, tuntud ka meeldib isobaarsed teisendused, vaata:
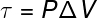
P - rõhk (Pa või atm)
ΔV - mahu kõikumine (m³ või l)
Kui süsteemile avaldatav rõhk pole püsiv, saab tööd arvutada rõhu ja mahu graafiku pindala (P x V) järgi. Selle skalaarse suuruse kohta lisateabe saamiseks külastage aadressi: töö.
lahendatud harjutused
Küsimus 1)(CefetMG) Suletud termotsüklis tehtav töö on võrdne 100 J ning soojusvahetuses osalev soojus võrdub vastavalt 1000 J ja 900 J kuumade ja külmade allikatega.
Esimesest termodünaamikaseadusest alates on selle termilise tsükli siseenergia varieerumine džaulides
a) 0
b) 100
c) 800
d) 900
e) 1000
Resolutsioon
Alternatiiv a.
Lahendame harjutuse, kasutades termodünaamika esimest seadust, märkus:

Avalduse kohaselt palutakse meil arvutada siseenergia variatsioon suletud termodünaamilises tsüklis, mille puhul teame, et sisemine energia variatsioon peab olema null, kuna masin töötab uuesti temperatuuril, mis oli tsükli alguses.
2. küsimus)(Upf) Ideaalse gaasi proov laieneb isobaarse ja adiabaatilise muundumise käigus selle mahu kahekordistamisega. Arvestades, et gaasi kogetud rõhk on 5,106 Pa ja selle algmaht 2.10-5 m³, võime öelda:
a) Gaas, mis protsessi käigus neeldub, on 25 cal.
b) Gaasi paisumise ajal tehtud töö on 100 cal.
c) Gaasi siseenergia variatsioon on –100 J.
d) Gaasi temperatuur püsib konstantsena.
e) Ükski ülaltoodust.
Resolutsioon
C alternatiiv
Kasutades harjutuse avalduses esitatud teavet, kasutame õige alternatiivi leidmiseks termodünaamika esimest seadust:
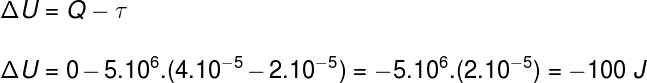
3. küsimus)(vau) Köögikanister sisaldab kõrgsurvegaasi. Selle ballooni avamisel märkame, et gaas pääseb kiiresti atmosfääri. Kuna see protsess on väga kiire, võime seda pidada adiabaatiliseks protsessiks.
Arvestades, et termodünaamika esimese seaduse annab ΔU = Q - W, kus ΔU on energia muutus gaasi sees on Q soojuse kujul ülekantav energia ja W on gaasi töö, see on õige märkida, et:
a) Gaasi rõhk tõusis ja temperatuur langes.
b) Gaasi tehtud töö oli positiivne ja gaasi temperatuur ei muutunud.
c) Gaasi tehtud töö oli positiivne ja gaasi temperatuur langes.
d) Gaasi rõhk tõusis ja tehtud töö oli negatiivne.
Resolutsioon
C alternatiiv
Kui gaasimaht on laienenud, ütleme, et tehtud töö oli positiivne, see tähendab, et gaas ise tegi väliskeskkonna tööd. Kuna protsess toimub väga kiiresti, ei ole gaasil aega soojusega keskkonnaga vahetada, seega toimub järgmine:
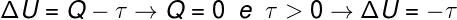
Arvestuse kohaselt väheneb gaasi siseenergia summa võrra, mis võrdub tehtud tööga. lisaks sellele, kuna gaasi siseenergia väheneb, väheneb ka gaas temperatuur.
4. küsimus)(Udesc) Füüsikalaboris tehakse katseid gaasiga, mida võib termodünaamilise analüüsi eesmärgil pidada ideaalseks gaasiks. Ühe katse analüüsi põhjal, kus gaasile viidi läbi termodünaamiline protsess, jõuti järeldusele, et kogu gaasile tarnitud soojus muudeti tööks.
Märkige alternatiiv, mis tähistab õigesti katses sooritatud termodünaamiline protsess.
a) isovolumetriline protsess
b) isotermiline protsess
c) isobaarne protsess
d) adiabaatiline protsess
e) liitprotsess: isobaarne ja isovolumeetriline
Resolutsioon
B. Alternatiiv
Selleks, et kogu gaasile tarnitud soojus muunduks tööks, ei tohi sisemine energia neelduda see tähendab, et gaas peab läbima isotermilise protsessi, see tähendab protsessi, mis toimub temperatuuril pidev.
Autor Rafael Hellerbrock
Füüsikaõpetaja