Vesinikkloriidhape on kõrge ionisatsioonipotentsiaaliga vesinikhape, see on kollakas vedelik, väga söövitav ja mürgine. Seda kasutatakse erinevates tööstusprotsessides, näiteks puhastusvahendite ja farmatseutiliste vesinikkloriidide valmistamisel, toiduainetes ja terasetootmisprotsessides.
Seda leidub ka inimese organismis; O maomahl mis toimib seedimisel valgud on happe lahus; vesinikkloriid- ja muude ainete, näiteks ensüümid ja soolad. Kokkupuude, sissehingamine või allaneelamine kontsentreeritud vesinikkloriidhape on tervisele väga kahjulik, mis võib põhjustada isegi surma.
Loe ka: Väävelhape - aine, millel on suur söövitav jõud
Soolhappe omadused
- anorgaaniline ühend
- tugev hape
- Kõrge ionisatsioonipotentsiaal
- Vedelik
- kollakas välimus
- Mürgine
- Sööbiv
- Lenduv
- Hügroskoopne (kipub imenduma ávesi keskkonnale)
- Lahustub vees
Ärge lõpetage kohe... Peale reklaami on veel;)
Vesinikkloriidhappe tootmine
Vesinikkloriidhape oli avastas moslemi alkeemik kutsus Jabir Ibne Haiane, tuntud ka kui Gaber ja keda peetakse araabia keemia isaks. Ta sünteesis aine põhinedes a
reaktsioon meresoola (NaCl) ja väävelhape (Kell2AINULT4).2NaCl + H2AINULT4 → Sisse2AINULT4 + 2HCl
Praegu vesinikkloriidhape toodetakse suures mahus läbi elektroonilineólüüs naatriumkloriidi vesilahus. Sellest protsessist saadakse gaas kloor (Cl2), gaas vesinik (H2) ja naatriumhüdroksiid (NaOH). Kloor- ja vesinikgaasid reageerivad vesinikkloriidhappeks:
Cl2 + H2 → 2HCl
Kuid, see reaktsioon on äärmiselt eksotermiline ja väga ohtlik. Praegu on suurem osa tööstuslikult toodetud vesinikkloriidhappest seotud orgaaniliste ühendite tootmisega, olles ökonoomsem ja ohutum protsess.
R-H + Cl2 → R-Cl + HCl
(Pidage R-d orgaaniliseks radikaaliks.)
Vaadake ka: Näpunäitedkui hapete tugevus

Vesinikkloriidhappe kasutamine
- Metalli marineerimine: Vesinikkloriidhapet kasutatakse metallide enne nende töötlemist „puhastamiseks“, eemaldades nende pinnalt rooste, katlakivi ja muud lisandid.
- Orgaaniliste ühendite tootmine: vesinikkloriidhapet kasutatakse reagendina vinüülkloriidi saamiseks, mida kasutatakse plastide valmistamisel. Vesinikkloriidhape pärineb ka kloropreenist, mida kasutatakse sünteetilistes kummides.
- Anorgaaniliste ühendite tootmine: vesinikkloriidhapet leidub mitmetes reaktiivide ja ühendite tootmise tööstusprotsessides anorgaanilised ained, nende hulgas veetöötluseks mõeldud tooted, nagu raud (III) kloriid ja alumiinium.
- Kasutatakse puhastusvahendina: Soolhapet, mida turustatakse ka muriinhappena, kasutatakse tööriistade ja masinate ehitusjärgseks, koduseks ja keemiliseks puhastamiseks.
- Toidu töötlemine: Vesinikkloriidhapet kasutatakse toidu ja lisaainete tootmiseks erinevates reaktsioonides, näiteks tärklise ja valkude hüdrolüüsil, või lõpptootes pH tasakaalu saavutamiseks.
- Narkootikumide tootmine: Vesinikkloriidhapet kasutatakse lahustuvate vesinikkloriidide tootmiseks, mis esinevad mitmetes ravimites, näiteks doksütsükliinvesinikkloriidis, mida kasutatakse kõhutüüfus ja rõuged.
Vesinikkloriidhape kehas
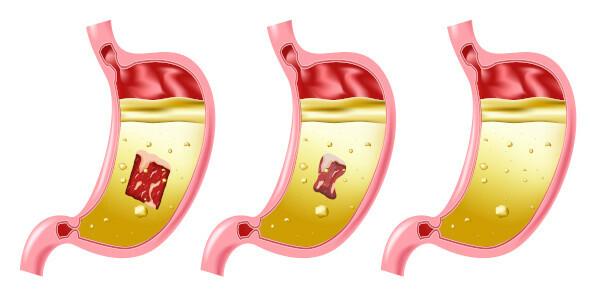
Vesinikkloriidhapet on meie koostises seedeelundkond, meie mao toodetud maomahl on vee, ensüümide, vesinikkloriidhappe, anorgaaniliste soolade ja väikese protsendi piimhappe lahus.
O toidukook muudetakse chyme'iks, happeline mass (tänu maomahla ja selle happelise koostise toimele) on just siis seedimine valgud, ümber kujundatud polüpeptiidid ja aminohapped mida keha neelab.
Soolhappe ohud
Vesinikkloriidhape on väga tugev ja söövitav hape, mistõttu kokkupuude ainega põhjustab mitmeid kahjustusi:
- Nahk: Põhjustab põletusi ja ärritust.
- Silmad: Põhjustab tugevat ärritust ja võib põhjustada pimedaksjäämist.
- Sissehingamine: Põhjustab ülemiste hingamisteede ärritust ja vigastusi.
- allaneelamine: põhjustab korrosiooni kogu suusüsteemis ja seedetraktis võib põhjustada oksendamist, verejooksu, kõhulahtisust, vereringehäireid, mis võivad põhjustada surma.
- Kokkupuudejätkub: ründab kõigepealt limaskesta piirkondi, põhjustades dermatiiti ja konjunktiviitigemete verejooks, valgustundlikkus; sagedane sissehingamine, isegi ühendi madala kontsentratsiooni korral, võib põhjustada gastriit ja ninaverejooks.
Juurdepääs ka: Äädikhappe omadused ja omadused

lahendatud harjutused
Küsimus 1 - (Udesc) Seoses vesinikkloriidhappega võib öelda, et:
A) vesilahuses olles võimaldab see läbida elektrivoolu.
B) on dihape.
C) on nõrk hape.
D) on madala ioniseerimisastmega.
E) on ioonne aine.
Resolutsioon
Alternatiiv A. Vesinikkloriidhape ei ole dihape, kuna sellel on ainult üks ioniseeritav H, vaid üks tugev hape, kõrge ionisatsioonipotentsiaaliga molekulaarne aine. THE ionisatsioon veekeskkonnas soodustab elektrivool vabade ioonide olemasolu tõttu.
2. küsimus - Soolhappe ja vee lahuses võime öelda, et molekulaarse vesinikkloriidi (HCl) esinemine on minimaalne, seda seetõttu, et
A) veega kokkupuutuv vesinikkloriidhape lahjendatakse.
B) vesinikkloriid on aine, mis ei lahustu vees.
C) vesinikkloriidil on kõrge ionisatsioonipotentsiaal, seetõttu moodustab HC1 molekul vesikeskkonnas H-ioone+ Cl-.
D) vesinikkloriidhape, olles väga lenduv, eraldub lahusest, jättes alles ainult veemolekulid.
E) vesinikkloriidhape on ioonne aine, seetõttu vesilahuses see dissotsieerub, moodustades ioone.
Resolutsioon
Alternatiiv C.
A) Vastus ei ühti küsimusega, vesinikkloriidhappe lahjendamine vees ei õigusta molekulaarse HCl puudumist.
B) Vale, vesinikkloriid on lahustuv ja sellel on afiinsus vee suhtes.
C) Õige
D) Kuigi vesinikkloriidhape on lenduv, ei toimu seda kahe liigi eraldamist lahuses märkimisväärselt.
E) Vesinikkloriidhape on vesinikkloriidi ja vee lahus, kus vesinikkloriid on mitteioonne molekulaarne aine.
Autor Laysa Bernardes Marques de Araujo
Keemiaõpetaja
Kas soovite sellele tekstile viidata koolis või akadeemilises töös? Vaata:
ARAúJO, Laysa Bernardes Marques de. "Vesinikkloriidhape"; Brasiilia kool. Saadaval: https://brasilescola.uol.com.br/quimica/Acido-cloridrico.htm. Juurdepääs 27. juunil 2021.