El carbono tiene cuatro electrones en su capa de valencia, lo que significa que puede formar cuatro enlaces, por lo que puede unirse a otros átomos. como: H, O, N, Cl. Esta propiedad que tiene el carbono explica la variedad de compuestos orgánicos que existen en la naturaleza, por eso se dice que el carbono es tetravalente.
En el año 1874, Van’t Hoff y Le Bel crearon un modelo espacial para el carbono. Este modelo tenía átomos de carbono representados por tetraedros regulares, con el carbono ocupando el centro del tetraedro y sus cuatro valencias correspondientes a sus cuatro vértices.
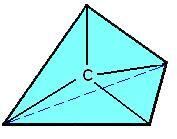
Fórmula espacial de carbono.
En este modelo, los diferentes tipos de enlaces que ocurren entre los átomos de carbono se representaron de la siguiente manera:
La) enlace simple - los tetraedros están conectados por un vértice (enlace sencillo);


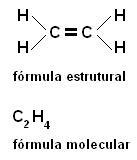
b) Doble enlace - los tetraedros están unidos por dos vértices (un borde);

c) Triple enlace - los tetraedros están unidos por tres vértices (una cara);
No pares ahora... Hay más después de la publicidad;)

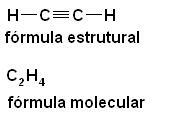
La evolución del modelo atómico mostró que el átomo tiene un núcleo y una electrosfera, lo que permitió la aparición de nuevos modelos. para explicar los enlaces formados por el carbono: en el año 1915, Lewis presentó una nueva propuesta para el enlace de los átomos de carbón. Según Lewis, los átomos se unieron a través de pares electrónicos en la capa de valencia. Esta representación se llamó fórmula electrónica de Lewis, y el tipo de enlace en el que los átomos se unen a través de pares electrónicos se conoce como enlace covalente.
Fórmula electrónica Lewis
La gran mayoría de moléculas orgánicas son tridimensionales, por lo que es necesario utilizar modelos que muestren no solo la estructura, sino también la geometría. Por tanto, la fórmula espacial es más adecuada para comprender la estructura del carbono.
Por Líria Alves
Licenciada en Química
Equipo Escolar de Brasil
Química Orgánica - Química - Escuela Brasil
¿Le gustaría hacer referencia a este texto en una escuela o trabajo académico? Vea:
SOUZA, Líria Alves de. "Fórmulas estructurales de carbono"; Escuela Brasil. Disponible: https://brasilescola.uol.com.br/quimica/formulas-estruturais-carbono.htm. Consultado el 28 de junio de 2021.
