LA La capa de ozono, como su nombre lo indica, es una capa o revestimiento formado por moléculas de gas ozono (O3 (g)), una forma alotrópica de oxígeno cuya molécula se muestra a continuación:
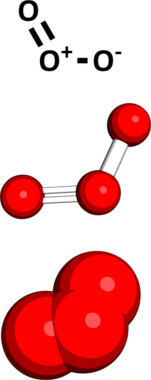
Se encuentra ubicado en una capa exterior a la atmósfera, a una altitud entre 20 y 35 km, llamándose el estratosfera. Pero este gas también se puede encontrar en cantidades más pequeñas en la troposfera (altitud de unos 10 km).

La capa de ozono juega un papel vital en el mantenimiento de la vida en la Tierra, ya que es capaz de absorber hasta el 99% de la Radiación ultravioleta (UV) del sol. Dado que esta radiación tiene longitudes de onda cortas y alta energía, tiene un alto poder de penetración en la piel. Es esta radiación la que provoca el bronceado, pero también es responsable de muchos efectos nocivos, ya que puede dañar el ADN (ácido desoxirribonucleico), provocando mutaciones genéticas.
La radiación UV se divide en tres distintos rangos de energía: UVA (320 nm a 400 nm), UVB (290 nm a 320 nm) y UVC (200 nm a 290 nm). Entre ellos, el más dañino y energético es el UVC, que, afortunadamente, no llega a la superficie terrestre porque es filtrado por la capa. de ozono.
Entonces, la capa de ozono es realmente un escudo versátil y eficiente que ayuda a proteger de esta radiación dañina. muchas formas de vida, como el plancton, que son responsables de producir gran parte de nuestra oxígeno.
La cantidad de ozono en la estratosfera no es constante, pero es directamente proporcional a la intensidad de la radiación ultravioleta. La formación de moléculas de este gas ocurre a través de la descomposición de moléculas de gas oxígeno (O2 (g)), formando oxígeno libre que reacciona, en un segundo paso, con el oxígeno gaseoso:
1er paso: El2 (g) → 2 O(gramo)
2da etapa: La(gramo) + O2 (g) → 1 El3 (g)
Luego se forma un equilibrio químico en la capa de ozono:
2 O2 (g) ↔ 1 O3 (g) + O(gramo) ∆H = + 142,35 kJ / mol
Desafortunadamente, sin embargo, con el tiempo, los seres humanos han liberado algunos compuestos contaminantes que desplazaron este equilibrio hacia la descomposición de la ozono, disminuyendo su concentración en la estratosfera y dejando al planeta más desprotegido.
Una de las mayores causas de la destrucción de la capa de El ozono son los CFC (clorofluorocarbonos, también conocidos como Fréons®), que son compuestos formados por átomos de carbono, flúor y cloro. Los CFC se liberan a la atmósfera principalmente mediante su uso como propulsor de aerosoles. (aerosoles), en refrigeradores y refrigeradores, como agente expansor de plásticos y en solventes para limpiar circuitos electrónicos.

Como puede ver en las reacciones a continuación, cuando el CFC golpea la estratosfera, la radiación solar descompone sus moléculas y libera cloro. El cloro, a su vez, reacciona con el ozono y esto reduce su concentración:
CH3Cℓ(gramo) → CH3(gramo)+Cℓ(gramo)
Cℓ(gramo) + O3 (g) → CℓO(gramo) + O2 (g)
Además, la CℓEl formado también reacciona con los átomos de oxígeno libres en la atmósfera, liberando más átomos de cloro, que reaccionarán con el ozono, destruyendo cada vez más nuestra capa protectora:
ClO(gramo) + O(gramo) → Cl(gramo) + O2 (g)
El lugar más afectado es la Antártida, donde el agujero en la capa de ozono era dos veces más grande que en Europa en septiembre de 2000. El satélite de monitoreo de ozono de la NASA registró la El agujero más grande jamás visto sobre la Antártida, que mide alrededor de 28,3 millones de kilómetros cuadrados, lo que representa más de tres veces el área de Australia. Esta situación es peor en la Antártida porque allí la formación de átomos de cloro es muy grande y permanece sin cambios, debido a la atípica Las nubes estratosféricas se formaron durante el invierno austral, y es en la superficie de las partículas de estas nubes donde ocurren las reacciones. mostrado.
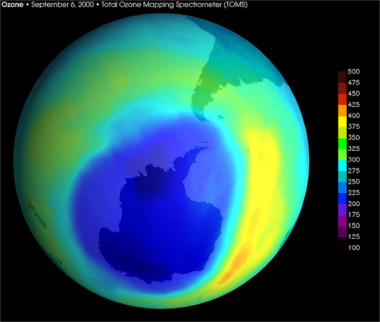
Imagen de satélite de la NASA de un "agujero" en la capa de ozono sobre la Antártida, septiembre de 2000
Las posibles consecuencias de la destrucción de la capa de ozono son lasaumento de la incidencia de cáncer de piel, debido a la acción de los rayos ultravioleta, y la intensificación del calentamiento global, la lo que lleva a varios resultados catastróficos, como el derretimiento de los glaciares polares, elevando el nivel del agua en el océanos.
Pero todavía hay un rayo de esperanza, ya que desde 2000 las concentraciones enLos CFC han disminuido casi un uno por ciento al año.
Por Jennifer Fogaça
Licenciada en Química
Fuente: Escuela Brasil - https://brasilescola.uol.com.br/quimica/camada-de-ozonio2.htm

