La gran mayoría de los materiales que se encuentran en la naturaleza, en nuestra sociedad y en nuestros cuerpos no son sustancias puras, sino, de hecho, mezclas de dos o más sustancias.
Aunque nos referimos, la mayoría de las veces, al agua mineral solo como “agua”, en realidad no solo contiene la sustancia pura H2O, porque es el resultado de un proceso en el que el agua de lluvia penetra en el suelo y atraviesa diversas rocas.
Entonces, como su nombre lo indica, además de agua, también tiene varios minerales disueltos. Si tienes curiosidad por comprobar la etiqueta de cualquier agua mineral, verás que tiene en su composición química sulfatos de estroncio, calcio, sodio, potasio, bicarbonato de sodio, fluoruro de sodio, entre otros.
Mapa mental: mezclas
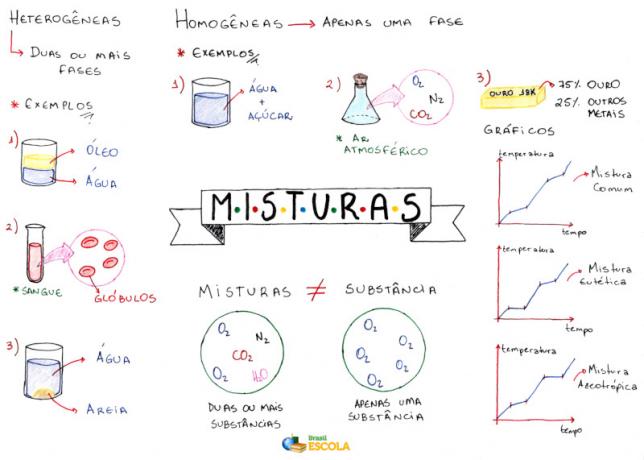
* Para descargar el mapa mental en PDF, Haga clic aquí!
¿Cómo es posible diferenciar una sustancia de una mezcla?
El agua destilada que se muestra a continuación es una sustancia pura que contiene solo H2O:

Agua destilada utilizada en laboratorio
Visualmente, se ve exactamente como una mezcla de agua y sal; sin embargo, se pueden diferenciar de la definición de mezcla. Vea:
→ Mezclas son materiales cuyas propiedades físicas no son constantes, sino que varían a una determinada temperatura y presión.
Entonces, solo mida el propiedades físicas, como los puntos de fusión y ebullición y la densidad. Si son constantes y bien definidos, es un Sustancia pura (en el caso del agua destilada, a 4 ° C, su densidad es de 1.0 g / cm3 y, a nivel del mar, los puntos de fusión y ebullición son 0 ° C y 100 ° C, respectivamente).
Sin embargo, si se presentan variaciones, es una mezcla. Si calienta la mezcla de agua y sal para comprobar el punto de ebullición, verá que durante el cambio de estado líquido a gas, la temperatura no permanece constante, como con el agua destilada, que permanece a 100 ° C hasta que todo el líquido se vuelve vapor.
Ahora hay mezclas que ni siquiera es necesario determinar sus propiedades físicas para saber que son mezclas, basta con mirar, como es el caso de la siguiente mezcla de agua y aceite:

Mezcla formada por agua y aceite
Esto indica que existen diferentes tipos de mezclas, que se pueden clasificar en homogéneo y heterogéneo. Ver cada uno:
Mezclas homogéneas:
Son los que tienen un aspecto uniforme, con una sola fase (fase única). Ejemplos:
solución salina (0,9 g de cloruro de sodio en 100 ml de agua);
salmuera (36 g de sales como cloruro de sodio, cloruro de magnesio, yodato de potasio, antihumectantes y 100 ml de agua);
alcohol hidratado (etanol y agua);
aire (78% gas nitrógeno, 20% gas oxígeno, 2% otros gases y vapor de agua);
acero (aleación metálica formada por 98,5% de hierro y 1,5% de carbono).

Solución salina, acero y formaldehído, ejemplos de mezclas homogéneas
Los ejemplos anteriores muestran que mezclas homogéneas pueden estar en estado sólido, líquido o gaseoso. Estas mezclas homogéneas se denominan soluciones y no pueden separarse mediante métodos físicos, sino únicamente mediante técnicas químicas. Para separar el alcohol del agua, por ejemplo, es necesario realizar un proceso de destilación, Porque un centrífugo o filtración no serviría.
Además, es importante enfatizar que deben ser homogéneo incluso cuando se mira con un ultramicroscopio. A simple vista, la leche y la sangre, por ejemplo, pueden parecer homogéneas, pero bajo el ultramicroscopio vemos que en realidad son heterogéneo. Vea la imagen de la sangre bajo el ultramicroscopio y sus fases separadas después de que se haya colocado en una ultracentrífuga:
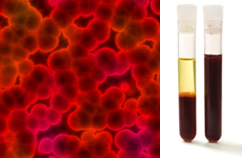
Imagen microscópica y fases sanguíneas.
Mezclas heterogéneas:
Son aquellos que tienen más de una fase. Ejemplos: agua y aceite, agua y arena, hielo y agua, granito, agua y hierro, sal sin disolver en agua, etc.
Los componentes de mezclas heterogéneas aparecen, en la mayoría de los casos, en diferentes estados físicos y pueden separarse por métodos físicos. Un ejemplo ocurre cuando hacemos café y filtramos el sólido, separándolo del líquido.
Pero esto no siempre ocurre, como se muestra en el caso del aceite y el agua, que a pesar de ser ambos líquidos, no se disuelven por diferentes polaridades de sus moléculas.
Mapa mental Por Madre Víctor Ricardo Ferreira
Profesor de química
Por Jennifer Fogaça
Licenciada en Química
Fuente: Escuela Brasil - https://brasilescola.uol.com.br/quimica/tipos-misturas.htm
