LA geometría angular es uno de varios tipos de Geometría molecular, que aún puede ser lineal, piramidal, trigonal plano, tetraédricoetc. La geometría angular solo se puede encontrar en moléculas que tengan las siguientes características:
Los triatómicos, es decir, tienen solo tres átomos;
Tener al menos tres nubes de electrones en el átomo central.
Nota: la nube electrónica lo es todo enlace covalente (simple, doble, triple o coordinado) entre átomos y pares de electrones del capa de valencia que no están participando en una llamada.
Vea algunos ejemplos de moléculas que tienen geometría angular:
1er Ejemplo: agua (H2O)

estructura de agua convencional
En la estructura del agua, tenemos:
Tres átomos: dos hidrógenos y un oxígeno;
El oxígeno es el átomo central porque forma un mayor número de enlaces (dos, ya que pertenece a la familia VIA);
Dos enlaces simples entre oxígeno e hidrógenos. Esto se debe a que cada hidrógeno solo puede formar un enlace y el oxígeno dos enlaces;
Cuatro electrones no enlazantes en oxígeno, ya que tiene seis electrones en la capa de valencia y usa solo dos en los enlaces.
Por lo tanto, como en la molécula de agua hay tres átomos y cuatro nubes electrónicas (dos enlaces simples y dos pares de electrones no enlazantes) en el átomo central, el la geometría es angular.
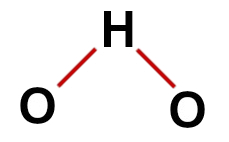
Correcta fórmula estructural del agua.
Nota: Siempre que la molécula presente estos patrones, el ángulo formado entre los átomos es de aproximadamente 109º 28'.
2do Ejemplo: Dióxido de azufre (SO2)

Estructura convencional de dióxido de azufre.
En la estructura del dióxido de azufre, tenemos:
Tres átomos: dos oxígenos y un átomo de azufre;
El azufre es el átomo central ya que es el elemento más pequeño de la molécula, ya que todos los elementos deben formar el mismo número de enlaces (dos);
Un doble enlace entre el azufre y uno de los oxígenos. Eso es porque ambos necesitan dos conexiones;
Uno enlace covalente coordinado o dativo, porque el azufre se mantuvo estable después de hacer el emparejamiento con el otro oxígeno, pero todavía hay un átomo de oxígeno que necesita dos electrones;
Cuatro electrones no enlazantes en oxígeno. Eso es porque el oxígeno tiene seis electrones en la capa de valencia y usa solo dos en los enlaces.
Así, como en la molécula de dióxido de azufre, hay tres átomos y cuatro nubes electrónicas (dos enlaces simples y dos pares de electrones no enlazantes) en el átomo central, el la geometría es angular.
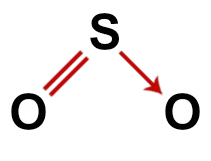
Fórmula estructural correcta del dióxido de azufre.
Nota: Siempre que la molécula tenga estos patrones, el ángulo formado entre los átomos es de aproximadamente 120O.
Por mí. Diogo Lopes Dias
Fuente: Escuela Brasil - https://brasilescola.uol.com.br/o-que-e/quimica/o-que-e-geometria-angular.htm


