¿Qué significa decir que un gas ha sufrido una transformación gaseosa?
Para responder a la pregunta inicial, es importante recordar que el estado del gas o estado gaseoso está determinado por las variables de estado: presión, volumen y temperatura. Pronto, un transformación de gas no es más que cualquier situación en la que una cierta cantidad de gas sufre variación en una de sus tres variables de estado. Siempre que una variable sufre un cambio, el valor de otra cambiará en consecuencia.
En el siglo XVII, varios científicos llevaron a cabo experimentos para descubrir las particularidades de las transformaciones de gas. Entre ellos, podemos mencionar: Torriceli, Robert Boyle, Mariotte, Guericke, entre otros. En sus estudios, el procedimiento consistió en cambiar una de las variables de estado y observar el comportamiento de las demás. Al hacerlo, observaron que para determinar significativamente la relación entre una variable y otro, era necesario hacer que el tercero no cambiara, es decir, que permaneciera constante. Así, las investigaciones se realizaron de tres formas distintas, cada una con sus particularidades, son:
transformación isotérmica, transformación isobárica y transformación isovolumétrica.Antes de detallar las tres transformaciones mencionadas anteriormente, recordemos cuál es el Ley general de los gases perfectos: De acuerdo con esta ley, una masa de gas inicialmente definida por variables de estado (p1, V1 y T1), cuando sufre una transformación gaseosa, tiene las variables de estado (p2, V2 y T2) que caracterizan el estado final del gas. Estas variables siguen la siguiente relación:
No pares ahora... Hay más después de la publicidad;)

De la ecuación anterior podemos ver que la presión, el volumen y la temperatura varían durante la transformación del gas.
Transformación isotérmica oLey de Boyle-Mariotte: es la transformación en la que la temperatura T del gas permanece constante, variando su presión PAG y su volumen V. La siguiente lista es válida:

Transformación isobárica oLey Gay-Lussac: es la transformación en la que la presión PAG del gas permanece constante, variando su volumen V y temperatura T. La siguiente lista es válida:
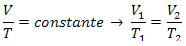
Transformación isovolumétrica o ley de Charles: también conocida como transformación isométrica, es la transformación en la que el volumen V del gas permanece constante, variando su presión PAG y temperatura T. La siguiente lista es válida:

Por Nathan Augusto
Licenciada en Física
¿Le gustaría hacer referencia a este texto en una escuela o trabajo académico? Vea:
FERREIRA, Nathan Augusto. "Transformaciones de gas"; Escuela Brasil. Disponible: https://brasilescola.uol.com.br/fisica/as-transformacoes-gasosas.htm. Consultado el 27 de junio de 2021.