isómeros activos u isómeros ópticamente activos (IOA) son moléculas de una determinada sustancia química que pueden llevar a cabo la polarización y desviación de la plan de luz derecha o izquierda. Para comprobar si una sustancia tiene isómeros activos o no, basta con comprobar si hay un carbono asimétrico en su fórmula estructural:

Analizando la cadena representada en la imagen de arriba, podemos ver que el el carbono central tiene cuatro ligandos diferentes (OH, H, CH3 y Cl), lo que lo convierte en un carbón asimétrico, también llamado carbono quiral. Por tanto, siempre que una cadena tenga uno o más carbonos quirales, habrá isómeros activos.
Tú tipos de isómeros activos(IOA) ellos son:
Diestro: Isómero óptico activo que dobla la luz polarizada hacia la derecha;
Levogiro: Isómero óptico activo que dobla la luz polarizada hacia la izquierda.
Observación: La presencia de carbono asimétrico en una fórmula estructural indica que la sustancia debe tener el isómero levorrotatorio y el isómero dextrorrotatorio. No nos corresponde a nosotros saber en qué dirección se desvió la luz, ya que la presencia del carbono quiral ya evidencia este hecho. Siempre la mitad de las moléculas existentes son zurdas y la otra mitad son diestras.
Las moléculas diestras y zurdas de cualquier sustancia orgánica siempre tienen las mismas propiedades físicas (punto de fusión, punto de ebullición, densidad, solubilidad, etc.), pero presentan actividades químicas (comportamiento en el organismo) muchas diferentes. Un ejemplo es la adrenalina. Solo la molécula de adrenalina levogyra actúa en el cuerpo, mientras que la dextrogyra no.
Vea ahora la fórmula estructural de la sustancia butan-2-ol para comprobar si tiene o no isómeros activos:
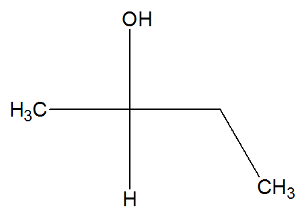
Podemos observar, en la estructura del butan-2-ol, que el carbono 2 tiene cuatro carpetas diferentes (OH, H, CH3, CH2-CH3), por lo que es un carbono quiral y presenta un isómero activo dextrorrotatorio y otro isómero activo levorrotatorio.
Cálculo de isómeros activos (IOA)
El químico holandés Jacobus Henricus van't Hoff desarrolló una fórmula que permite calcular cuántos isómeros activos (IOA) puede presentar una determinada sustancia. Vea:
IOA: 2No
norte: es el número de carbonos quirales en la fórmula estructural de la sustancia.
Siga dos ejemplos de aplicación de la fórmula de Vant't Hoff:
Ácido 5-dicloro-2,3-dihidroxi-hexanodioico

En la fórmula estructural del compuesto, hay tres carbonos quirales o asimétrico, por lo tanto:
IOA = 2No
IOA = 23
IOA = 8
2,3,4,5-tetrahidroxihexanal

En la fórmula estructural del compuesto, hay cuatro carbonos quirales (flechas rojas) o asimétrico, por lo tanto:
IOA = 2No
IOA = 24
IOA = 16
Observación: Existe la posibilidad de que una fórmula estructural tenga dos carbonos asimétricos que tengan exactamente los mismos ligandos. Si esto ocurre, consideramos en los cálculos solo 1 para el valor de n, no 2. Vea un ejemplo:
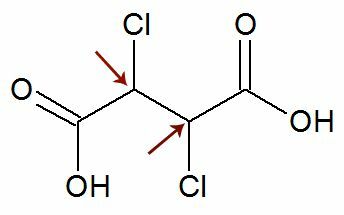
Como dos carbonos quirales ellos son es igual a, consideramos solo uno carbono en el cálculo:
IOA = 2No
IOA = 21
IOA = 2
Por mí. Diogo Lopes Dias
Fuente: Escuela Brasil - https://brasilescola.uol.com.br/quimica/isomeros-ativos.htm

