Uno reacción de oxidación en compuestos orgánicos ocurre cuando hay un entrada de oxigeno (o salida de hidrógeno) en la molécula orgánica.
| Uno oxidación leve solo ocurre en hidrocarburos con insaturación, es decir, con enlaces dobles (alquenos) o triples (alquinos). |
Para que los hidrocarburos saturados se oxiden, se necesita una oxidación más enérgica.
La oxidación leve utiliza el Baeyer reactivo, que corresponde a una solución acuosa de permanganato de potasio (KMnO4) en un medio frío neutro o ligeramente alcalino (básico - OH1-). Este reactivo se llama así porque el químico alemán Adolf Von Baeyer propuso una prueba, llamada Prueba de Baeyer, para identificar alquenos y sus isómeros ciclan.
Esta prueba funciona de la siguiente manera: como veremos más adelante, un alqueno reacciona con el permanganato de potasio, por lo que su color, inicialmente violeta, se vuelve incoloro y aparece un precipitado marrón (MnO2). Sin embargo, los ciclanos no reaccionan con el permanganato de potasio. Entonces, si la solución permanece violeta, es un ciclan.
La siguiente figura muestra que la prueba fue positiva para alquenos solo en el tubo de ensayo izquierdo, ya que apareció el precipitado marrón.

La reacción de oxidación de los alquenos comienza con la descomposición del permanganato, produciendo oxígeno:
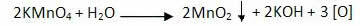
Oxidación leve de alquenos:
Este oxígeno producido reaccionará con el doble enlace del alqueno formando un epóxido que luego, por hidrólisis, se convierte en un alcohol o diol vecinal (glicol), es decir, dos grupos OH en carbonos vecinos.
En el siguiente ejemplo, vemos la oxidación leve del propeno:
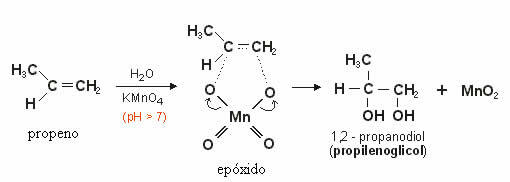
Oxidación leve de alquinos:
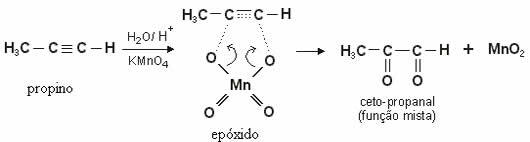
En el caso de alquinos, el producto formado será dicetonas. Con la excepción del etino (HC≡CH), donde hay dos hidrógenos unidos en cada carbono que participa en el triple enlace, un aldehído.
Nótese la oxidación leve del propino, con formación de dicetona:
Por Jennifer Fogaça
Licenciada en Química
Equipo Escolar de Brasil
Fuente: Escuela Brasil - https://brasilescola.uol.com.br/quimica/oxidacao-branda.htm
