A estereoisomería, o isomería espacial, ahí está el isomería óptica, que ocurre cuando los compuestos son ópticamente activos, es decir, desvían el plano de la luz polarizada.
Los isómeros que exhiben actividad óptica se denominan enantiómeros, tienen tres características principales:
- Tu molécula es asimétrico. Esto significa que si lo dividimos por la mitad, las partes resultantes no serán iguales;
- Los enantiómeros son los imagen de espejo el uno del otro;
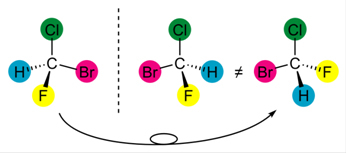
- Ellos no son superponibles, es decir, si colocamos una molécula encima de la otra, no serán iguales, la disposición de sus átomos de unión será diferente.
Estos enantiómeros, cuyas moléculas son asimétricas y no se superponen, se denominan moléculas quirales, porque la palabra "quiral" proviene del griego cofre que significa "mano", porque las manos son asimétricas y no se superponen.

Además, si colocamos la mano izquierda frente al espejo, su imagen se verá exactamente como la mano derecha y viceversa. En otras palabras, las manos son iguales a los enantiómeros, en el sentido de ser la imagen especular entre sí.

Los enantiómeros se diferencian de diastereoisómeros debido al hecho de que estos últimos no son imágenes especulares entre sí. Tanto los enantiómeros como los diastereoisómeros son estereoisómeros o isómeros espaciales.
Sin embargo, los enantiómeros se consideran los más importantes, especialmente en lo que respecta a los fenómenos bioquímicos. La actividad que ejerce cada enantiómero en el organismo es diferente entre sí.
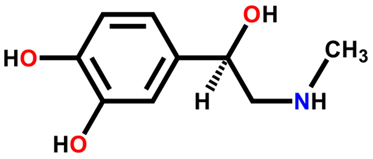
Por ejemplo, la hormona adrenalina tiene dos enantiómeros, dextrogyro y levogyro. El dextrogyrus suele ser menos activo como hormona que el levogyrus. La acción de la adrenalina levorrotatoria es importante porque actúa como un vasoconstrictor potente e hipertensivo, que tiene un efecto pronunciado sobre el metabolismo, provoca un aumento de la frecuencia cardíaca y la tensión arterial.
Por Jennifer Fogaça
Licenciada en Química
Fuente: Escuela Brasil - https://brasilescola.uol.com.br/quimica/o-que-sao-enantiomeros-na-isomeria.htm
