usted óxidos básicos son aquellos que, al reaccionar con el agua, dan lugar a bases. Cuando reaccionan con un ácido, forman sal y agua.
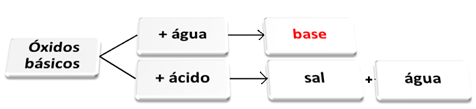
Óxidos básicos que reaccionan con agua y ácido.
Por ejemplo, tenemos óxido de sodio (Na2O), que es un óxido básico. Vea a continuación que, al reaccionar con el agua, forma una base de hidróxido de sodio:
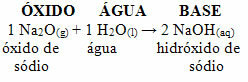
Si ese mismo óxido reacciona con un ácido como el ácido sulfúrico (H2SOLAMENTE4), se producirá una sal (sulfato de sodio) y agua.
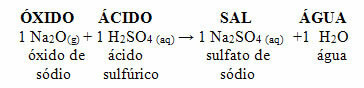
Si un óxido básico reacciona con un óxido ácido, también se produce una sal, pero sin agua.
Como se muestra en el ejemplo mostrado, los otros óxidos básicos también son compuestos iónicos, que se forman en su principalmente por metales, elementos que son altamente electropositivos, que normalmente presentan una "carga" igual a +1 o +2.
Ejemplos:
A2O = Na1+
K2O = K1+
CaO = Ca2+
MgO = Mg2+
Estos compuestos tienen altos puntos de fusión y ebullición y todos encierran el anión oxígeno (O2-).
Aplicaciones de algunos óxidos básicos:
• Perro: Óxido de calcio
Este compuesto se conoce comúnmente como cal viva. Al reaccionar con agua, según la reacción a continuación, se forma una base (hidróxido de calcio) que se utiliza para pintar paredes, troncos de árboles y otros materiales, con el objetivo principal de repeler insectos, preservar el sello y evitar infiltraciones del agua. Esta base formada se llama cal hidratada y, por lo tanto, cuando pintes con él, lo nombras pintura blanqueada.
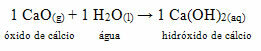

Pintura encalada.
• K2O: óxido de potasio
El óxido de potasio se encuentra comúnmente en la madera y la ceniza de cigarrillos. Al reaccionar con el agua, forma la base de hidróxido de potasio (KOH), que se utiliza en la fabricación de jabones. Incluso en el pasado, en lugares donde no había KOH, se usaban cenizas vegetales, que contenían K2O, reaccionar con las grasas y producir el llamado "jabón gris".
Por Jennifer Fogaça
Licenciada en Química
Fuente: Escuela Brasil - https://brasilescola.uol.com.br/quimica/oxidos-basicos.htm


