Los alcoholes pueden sufrir oxidación cuando se exponen a un agente oxidante, como una solución acuosa de dicromato de potasio (K2Cr2O7) o permanganato de potasio (KMnO4) en un medio ácido.
Un oxígeno naciente [O] en el medio atacará el carbono vinculado al grupo funcional alcohol (hidroxilo - OH), formando un compuesto muy inestable, llamado diol gemelo, que tiene dos hidroxilos unidos al mismo carbón. Al ser inestable, este compuesto libera agua y da lugar a un nuevo producto.
Este producto dependerá del tipo de alcohol que se haya oxidado, ya sea primario, secundario, terciario o metanol.
Brevemente, tenemos:
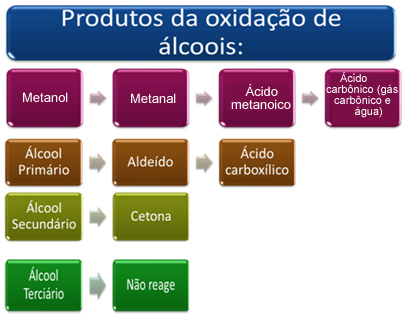
Vea cada caso a continuación:
- Metanol (H3C─ OH):
El metanol es el único alcohol que tiene tres hidrógenos unidos al carbono que se oxidarán. En este caso, dado que hay tres puntos en la molécula que un oxígeno naciente puede atacar, ocurrirán tres oxidaciones sucesivas, como se muestra en el siguiente diagrama:
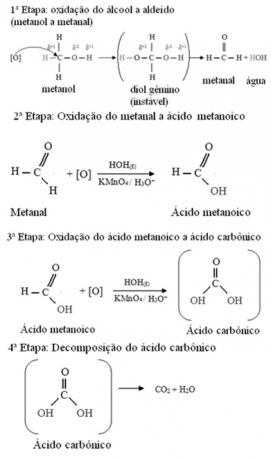
- Alcoholes primarios:
En estos compuestos, el carbono hidroxilo está unido a un solo átomo de carbono, es decir, los otros dos ligandos son hidrógenos, y hay dos lugares para que ataque el oxígeno naciente.
Primero, habrá la formación de un aldehído, como se muestra a continuación:
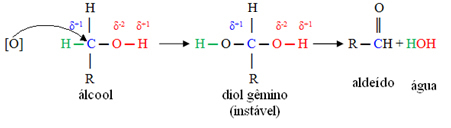
Pero la oxidación continúa, porque los reactivos utilizados para oxidar el alcohol son más fuertes que los utilizados para oxidar un aldehído. Luego, otro oxígeno naciente ataca el carbono carbonilo y produce un ácido carboxílico.
El siguiente es un ejemplo, la oxidación de etanol, primero a etanal y luego a ácido etanoico (ácido acético). Esta reacción total es la transformación del vino en vinagre.
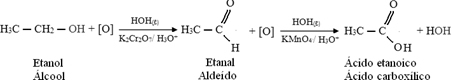
La oxidación parcial de etanol a etanal ocurre cuando una persona alcohólica se somete a una prueba de alcoholímetro desechable. Dentro de este dispositivo hay una mezcla sólida de dicromato de potasio y sílice en un medio ácido, con la siguiente reacción que ocurre:
K2Cr2O7 (aq) + 4H2SOLAMENTE4 (aq) + 3 CH3CH2Oh(gramo) → Cr2(SOLAMENTE4)3 (aq) + 7 a. M.2O(1) + 3 CH3CHO(gramo) + K2SOLAMENTE4 (aq)
naranjaetanol (incoloro)verdeethanal (incoloro)
Tenga en cuenta que, además de la oxidación del etanol (alcohol) a etanal (aldehído), hay una reducción simultánea de dicromato, que es naranja, a cromo (III), o incluso cromo (II), que es verde. El cambio de color indicará que la persona tiene más alcohol en la sangre del permitido.
- Alcoholes secundarios:
Estos son compuestos en los que el carbono hidroxilo está unido a otros dos átomos de carbono y solo a un átomo de hidrógeno. Por lo tanto, solo habrá una ubicación en la molécula donde el oxígeno naciente pueda atacar y solo se formará un tipo de producto, que siempre será una cetona:
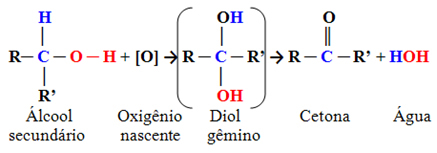
Dado que el carbono carbonilo de una cetona no tiene ningún enlace de hidrógeno directamente a él, ya no existe ninguna posibilidad de oxidación adicional. Por tanto, la reacción se detiene en la cetona.
- Alcoholes terciarios:
Los alcoholes terciarios son aquellos en los que el carbono que tiene el grupo -OH forma tres enlaces con otros átomos de carbono. Dado que no se unen a los hidrógenos, no hay ningún punto de la molécula que pueda ser atacado por el oxígeno naciente. Debido a este hecho, los alcoholes terciarios no sufren oxidación.
* Fuente y autor de la imagen: CostaPPPR.
Por Jennifer Fogaça
Licenciada en Química
Fuente: Escuela Brasil - https://brasilescola.uol.com.br/quimica/oxidacao-dos-alcoois.htm

