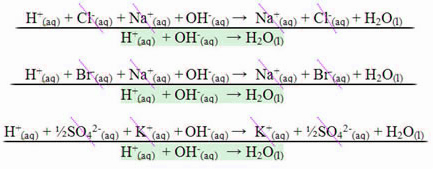La química inorgánica es la rama de la química que estudia los compuestos que no son de carbono. Eso es porque los hechos de carbono son estudiados por química orgánica.
Inicialmente, la química inorgánica se definió como la parte de la química que estudiaba los compuestos minerales. Por esta razón, también se le llamó química mineral.
Mientras tanto, el estudio de la química orgánica se orientó hacia compuestos de origen vegetal y animal.
La principal característica de los compuestos inorgánicos es la ausencia de carbono en su composición. Además, la mayoría de estos compuestos tienen como propiedad física el hecho de que son sólidos. Como propiedad química, destaca el hecho de que son iónicos, lo que significa que ganan o pierden electrones.
Funciones inorgánicas
Fue Arrhenius quien propuso la agrupación de compuestos inorgánicos. Esto se hizo basándose en el descubrimiento de componentes que se disuelven en agua y se descomponen en partículas electrificadas, los iones.
A partir de la Teoría de Arrhenius (1887), los compuestos inorgánicos se agruparon según la similitud que existía entre ellos. Esto facilitó el estudio de la química inorgánica.
Las principales funciones inorgánicas son ácidos, bases, sales y óxidos.
Los ácidos son compuestos que reaccionan con bases, formando sales y agua (neutralización). Tienen un sabor amargo, pH menor a 7 y en solución acuosa ionizan y originan, con uno de los iones, el catión H+.
Algunos ejemplos de ácidos: Ácido sulfúrico (H2SOLO4), Ácido clorhídrico (HCN), ácido fluorhídrico (HF).
A diferencia de los ácidos, las bases son sustancias que tienen un pH superior a 7 y un sabor amargo y astringente. En solución acuosa sufre la llamada "disociación iónica", ya que libera el anión OH- (Hidróxido).
Algunos ejemplos de bases: Hidróxido de sódio (NaOH), hidróxido de magnesio (Mg (OH)2), Hidróxido de potasio (KOH).
Las sales son compuestos iónicos con sabor salado que reaccionan con sales, ácidos, hidróxidos y metales para formar otras sales.
Algunos ejemplos de sales: Cloruro de sodio (NaCl), Bicarbonato de sodio (NaHCO3), Nitrato de sodio (NaNO3).
Los óxidos son compuestos binarios que tienen oxígeno (O) clasificado en: óxidos de ácido o anhídrido, óxidos básicos y peróxidos.
Algunos ejemplos de óxidos: óxido de calcio (CaO), monóxido de carbono (CO), dióxido de azufre (SO2).
Obtenga más información sobre cada una de estas funciones en Funciones inorgánicas.
En ejercicios sobre funciones inorgánicas ¡También puedes poner a prueba tus conocimientos con preguntas del examen de ingreso!
Ahora que sabe qué es la química inorgánica, lea también:
- Teoría de Arrhenius
- Química Orgánica
- Indicadores ácido-base