LA constante de ionización da Agua(Kw), O potencial de hidrógeno(pH) es el potencial hidroxiliónico (pOH) ellos son medidas importante para cálculos que involucran equilibrio químico en soluciones ácidas y básicas, así como en la determinación de la concentración de iones H+ y oh- de las soluciones en cuestión.
¿Qué es Kw?
El producto iónico del agua, o Kw (este wmedio agua - agua, en inglés), es la constante utilizada para representar el equilibrio generado por la autoionización del agua. Incluso a una velocidad muy pequeña, el agua se ioniza produciendo iones H+ y oh-, según la siguiente ecuación química:
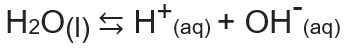
Analizando la ecuación, nos damos cuenta de que cuando el ionización a partir de una molécula de agua pura se genera un ion H.+ y un ion OH-, eso es el La concentración de estos iones siempre será la misma.. Incluso cuando hay un aumento de temperatura, lo que provoca un aumento en la tasa de ionización, las concentraciones siguen siendo las mismas.
Lea también:Energía de ionización
No pares ahora... Hay más después de la publicidad;)
Basado en mediciones experimentales, se calculó la concentración de iones H+ y oh- (resultante de la autoionización del agua) a 25 ° C y el valor de 1. 10-7 prostituta. Esto es, de un total de mil millones de moléculas de agua, solo dos se someten a ionización. Esto muestra que el agua pura tiene un bajo grado de ionización y explica la muy baja Conductividad eléctrica de agua pura.
Teniendo en cuenta lo que se mostró arriba, podemos escribir el expresión de la constante del balance hídrico:

Usando valores de concentración de iones H+ y oh- a 25 ° C, podemos calcular el valor de Kw:
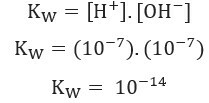
Como se dijo anteriormente, este valor de Kw cambia con el aumento de temperatura, como se muestra en la tabla siguiente:
T (° C) |
Kw |
10 |
0,29. 10-14 |
20 |
0,68. 10-14 |
25 |
1,00. 10-14 |
30 |
1,47. 10-14 |
40 |
2,92. 10-14 |
60 |
9,40. 10-14 |
Para obtener más información sobre este tema, lea nuestro texto: Producto de agua iónica.
¿Qué es pH y pOH?

el acrónimo pH medio potencial de hidrógeno y fue creado por el bioquímico danés Soren Sorensen, en 1909, para facilitar el trabajo con el concentraciones de iones de hidrógeno [H+], que generalmente se expresan en números decimales. Para obtener más información sobre este tema, lea nuestro texto: ¿Qué es el pH?
Este tipo de notación indica el contenido de iones H+ presente en la solución y está definido por la expresión matemática:
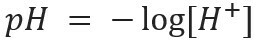
Del mismo modo, podemos definir el pOH o potencial hidroxiliónico, que nos dice el Contenido de iones OH- presente en la solución. Su expresión matemática es:
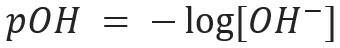
En una solución acuosa siempre habrá iones H+ y oh- (debido a la ionización que sufre el agua) que se utilizará para caracterizar una solución en ácido o básico. Cuantos más iones H+ hay en la solución, más ácida será. En consecuencia, la presencia de iones OH- en la solución lo hará más básico. Si hay un equilibrio en la cantidad de estos iones, la solución se clasificará como neutral.
escala PH
La escala de pH se muestra con valores que van de 0 a 14 (valores medidos a 25 ° C). Vea la escala de pH en la imagen a continuación:

Cuanto menor sea el pHde la solución,mayor es su acidez, y cuanto más cerca del final de la escala, es decir, más cerca del 14, mayor es su carácter básico. Por ejemplo, el jugo de limón tiene un pH de 2, mientras que los blanqueadores tienen un pH de 12.
Cómo calcular el pH y la pOH
conociendo el concentración de iones, podemos calcular los valores de pH y pOH de las soluciones y, conociendo los valores potenciales, calculamos la concentración de iones en soluciones. Para ello se utilizan las siguientes expresiones:
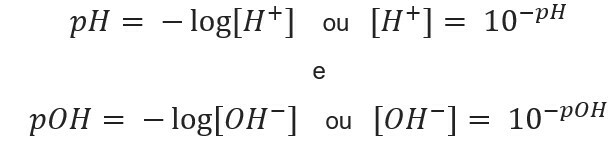
Vayamos a los ejemplos:
Ejemplo 1
Si queremos saber el pH de una solución con [H+] = 0.001 mol / L, solo use la fórmula presentada anteriormente:
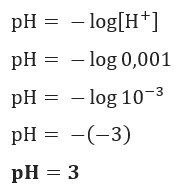
Ejemplo 2
Ahora, para averiguar cuál es la concentración de OH- de una solución con pOH = 5, simplemente reemplace el valor en la siguiente fórmula:

Si aplicamos la misma escala de potenciales para el balance iónico del agua, tendremos:
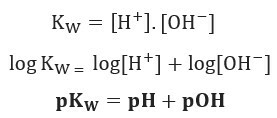
Como se indicó, a 25 ° C, Kw = 10-14. Por lo tanto:

Con esto, podemos calcular el pOH de una solución en función de su pH. Si tenemos una solución con un pH de 3, entonces su pOH será 11.
Sepa mas: Medios neutros, ácidos y básicos
Ejercicios resueltos
Pregunta 1 (UEFS-BA) La concentración de iones OH–(aquí) en una solución de hidróxido de amonio dada, a 25 ° C, es igual a 1,10–3 prostituta. El pOH de esta solución es:
a) 0
b) 1
c) 3
d) 11
e) 13
Resolución: Letra c. Si tenemos [OH–] = 10–3 mol / L, por lo que su pOH será igual a 3.
Vea:
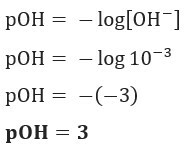
Pregunta 2 (UEA-AM) Considere la siguiente información, obtenida de una etiqueta de agua mineral en la ciudad de Porto Seguro (BA):
nitrato 1,45 mg / L
pH a 25 ° C 4,51
Esta agua mineral es
a) ácido y tiene [H+] –].
b) ácido y tiene [H+]> [OH–].
c) neutral y tiene [H+] = [OH–].
d) básico y tiene [H+]> [OH–].
e) básico y tiene [H+] –].
Resolución: Letra b. Como el pH del agua mineral informado en la etiqueta es menor a 7, podemos decir que es una solución ácida y, por tanto, la concentración de iones H+ es más grande que OH-.
Pregunta 3 (UEA-AM) Una forma de producir hidrógeno gaseoso rápidamente en el laboratorio es haciendo reaccionar zinc metálico en polvo con ácido clorhídrico (HCl), a una concentración de 1.0 mol / L:
Zn (s) + 2 HCl (ac) → ZnCl2 (aq) + H2 (gramo)
Considerando que el ácido clorhídrico está 100% ionizado y que la solución está a 25 ° C, es correcto afirmar que el pH de la solución de ácido clorhídrico mencionada en el texto es
- 0
- 1
- 3
- 13
- 14
Resolución:Letra a. Podemos calcular el pH de la solución utilizando la concentración de HCl informada en el texto, ya que, al estar 100% ionizado, la concentración de [H+] será el mismo, porque por cada molécula de HCl ionizado, un ion H+ se generará. Por lo tanto:
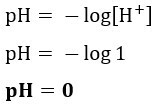
Por Victor Ferreira
Profesor de química