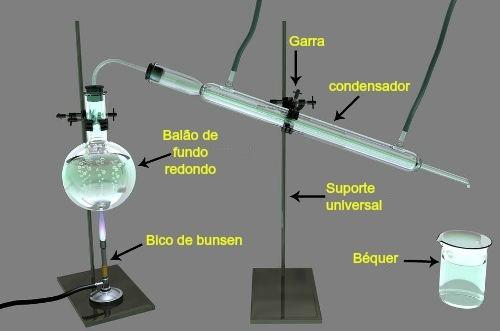
Las reacciones de nitración son reacciones de sustitución que ocurren a través del ácido nítrico (HNO3). Este tipo de reacción ocurre especialmente con alcanos y con benceno y sus derivados, donde uno de los átomos de hidrógeno unidos a la cadena o al núcleo aromático es reemplazado por el grupo NO.2, dando lugar a un compuesto nitro y agua.
Vea algunos ejemplos:
1. Nitración de un alcano:
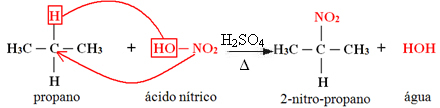
Cuando el alcano tiene más de dos carbonos, se forma una mezcla de diferentes compuestos sustituidos. La cantidad de cada compuesto obtenido será proporcional al siguiente orden de facilidad con que se libera el hidrógeno a la molécula:

En el caso anterior, no hay carbono terciario, solo hay uno secundario y dos primarios; por tanto, la mayor cantidad de compuesto formado como producto será 2-nitro-propano.
Si hay suficiente ácido nítrico, otro hidrógeno puede ser reemplazado por el grupo nitro, dando lugar al 2-dinitropropano. (estructura a continuación), un compuesto ampliamente utilizado como aditivo para el gasóleo, aumentando su índice de octanaje y disminuyendo la emisión de Hollín.
No pares ahora... Hay más después de la publicidad;)
EN EL2
│
H3C─C─CH3
│
EN EL2
2. Nitración de benceno:
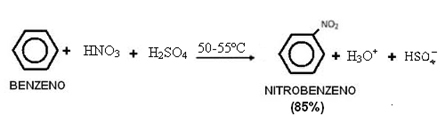
Nótese que esta reacción ocurre en presencia de calor, ya que el benceno se calienta con una mezcla sulfonhídrica, es decir, ácido nítrico concentrado con ácido sulfúrico concentrado. El ácido sulfúrico es un catalizador, lo que hace que la velocidad de reacción aumente a medida que el benceno reacciona lentamente con el ácido nítrico.
3. Nitración de derivados de benceno:
En tales casos, el lugar de sustitución dependerá del grupo sustituyente o grupo funcional unido al núcleo aromático. Los textos "Radicales de dirección en el anillo de benceno" y "Efectos electrónicos de radicales meta y orto-directores”Explique más sobre cómo sucede esto.
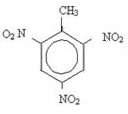
Los anillos aromáticos pueden sufrir nitración y dar lugar a explosivos. Un ejemplo es el trinitrotolueno (2-metil-1,3,5-trinitrobenceno), más conocido como TNT y existen varios pigmentos utilizados principalmente en tejidos.
Por Jennifer Fogaça
Licenciada en Química
¿Le gustaría hacer referencia a este texto en una escuela o trabajo académico? Vea:
FOGAÇA, Jennifer Rocha Vargas. "Reacciones de nitración orgánica"; Escuela Brasil. Disponible: https://brasilescola.uol.com.br/quimica/reacoes-organicas-nitracao.htm. Consultado el 28 de junio de 2021.