A reacciones de hidratación en alcadienos ellos son reacciones de adición, es decir, los componentes (hidronio e hidróxido) de la molécula de agua se añaden a un alcadieno.
Tú alcadienos son hidrocarburos que tienen una cadena abierta y dos dobles enlaces (formados por un sigma y un pi) entre los carbonos, como podemos ver en la siguiente estructura:

Fórmula estructural de un alcadieno
Para el reacción de hidratación en alcadienos se lleva a cabo, es fundamental que el enlace pi, presente en el doble enlace, se rompa por la influencia del calor y del ácido sulfúrico (H2SOLO4). Con la ruptura del enlace pi, aparecen dos sitios de enlace, cada uno en uno de los carbonos involucrados en el doble enlace.

Aparición de sitios de unión con interrupción de la unión de pi
La aparición de sitios de unión en la molécula de alcadieno es necesaria para los iones (H+ y oh-) del agua se añaden al alcadieno, formando, por ejemplo, un dialcohol (alcohol con dos hidroxilos).
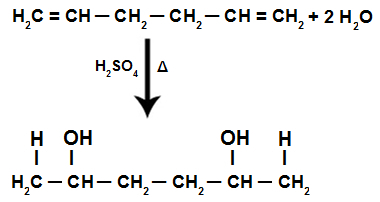
Adición de H+ y oh- en la estructura de un alcadieno
NOTA: La adición de la H+ y oh- en la estructura de alcadieno sigue el La regla de Markovnikov, es decir, la H+ se une al carbono más hidrogenado, y el OH- se une al carbono menos hidrogenado.

Ejemplo de la aplicación de la regla de Markovnikov en la hidratación de alcadienos
Como existen diferentes tipos de alcadienos con respecto a la posición de los dobles enlaces, puede ser que la hidratación de un alcadieno forme diferentes compuestos. Vea los siguientes casos:
→ Alcadieno acumulado o condensado
Es un alcadieno que tiene dos dobles enlaces que involucran simultáneamente tres átomos de carbono, es decir, no existe un enlace sencillo que separe los carbonos implicados en los enlaces dobles.

Fórmula estructural de un alcadieno acumulado.
Durante la reacción de hidratación de un alcadieno alterno, los enlaces pi se rompen, siendo el H+ añadido a los carbonos más hidrogenados y el OH- añadido a carbonos menos hidrogenados:
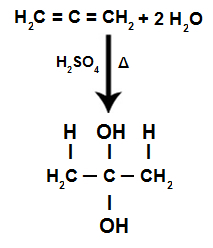
Ecuación de reacción de hidratación de alcadieno acumulado
Tenemos que en la hidratación de un alcadieno acumulado, el mismo átomo de carbono recibe los dos hidroxilos, formando un alcohol gemelo, que es una estructura inestable.

Estructura del alcohol formado por gemelos
Como el alcohol gemelo es inestable, tenemos la formación de una molécula de agua con los componentes de los dos hidroxilos y la creación de un enlace pi entre el carbono y el oxígeno.
No pares ahora... Hay más después de la publicidad;)

Formación de una cetona a partir de un alcohol gemelo
Por lo tanto, la reacción de hidratación de los alcadienos acumulados resultará en la formación de una cetona.
→ Alcadieno conjugado o alternativo
Es un alcadieno que tiene dos dobles enlaces que involucran simultáneamente cuatro átomos de carbono, es decir, hay un enlace sencillo que separa los carbonos implicados en los enlaces dobles.
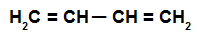
Fórmula estructural de un alcadieno alterno
En los alcadienos alternos, se produce la resonancia de sus dobles enlaces. Por lo tanto, los electrones del enlace pi cambian de posición (flechas rojas), como en el siguiente diagrama:
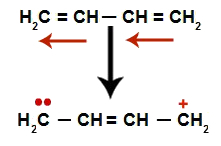
Esquema que representa la resonancia en un alcadieno alterno
Tenemos, en general, la aparición de un doble enlace exactamente entre los carbonos donde los dos dobles estaban previamente y la creación de dos sitios de enlace, uno en cada carbono que ya no forma el doble enlace (en el ejemplo, los carbonos 1 y 4). Los carbonos 1 y 4 de la cadena reciben la H+ y el oh- del agua.

Hidratación parcial en alcadieno alterno
Después de la resonancia, el enlace pi del nuevo doble enlace se rompe y un H+ y un oh- se añaden a la molécula de alcadieno. El OH se agrega al carbono más cercano al primer grupo OH agregado porque sufre la atracción electrónica del grupo, que es más electronegativo.

Terminación de la hidratación en un alcadieno alterno
Debido a la resonancia, decimos que el alcadieno alterno experimentó una hidratación de 1.4, formando un dialcohol.
→ Aislamiento de alcadieno
Es un alcadieno que tiene dos dobles enlaces que involucran al menos cinco átomos simultáneamente. de carbono, es decir, hay al menos dos enlaces simples que separan los carbonos implicados en los enlaces. dobles.

Fórmula estructural de un alcadieno aislado
Durante la reacción de hidratación de un alcadieno aislado, los enlaces pi se rompen, siendo el H+ añadido a los carbonos más hidrogenados y el OH- añadido a los carbonos menos hidrogenados.

Ecuación de la reacción de hidratación de alcadieno aislado
Por lo tanto, en la adición de un alcadieno aislado, solo tenemos la formación de un diaalcohol.
Por mí. Diogo Lopes Dias
¿Le gustaría hacer referencia a este texto en una escuela o trabajo académico? Vea:
DÍAS, Diogo Lopes. "Reacciones de hidratación en alcadienos"; Escuela Brasil. Disponible: https://brasilescola.uol.com.br/quimica/reacoes-hidratacao-alcadienos.htm. Consultado el 28 de junio de 2021.

