Cada celda es un dispositivo en el que se produce una reacción espontánea de oxidación-reducción que genera una corriente eléctrica que, a su vez, se utiliza para hacer funcionar algunos equipos.
Estos dispositivos obtuvieron su nombre porque la primera batería que se creó fue inventada por Alessandro Allá por el año 1800, estaba formado por discos de zinc y cobre separados por algodón empapado en salmuera. Este conjunto se colocó intercalado, uno encima del otro, amontonando los discos y formando una gran columna. Como fue un batería de discos, comenzó a ser llamado por ese nombre.

Las baterías siempre están compuestas por dos electrodos y un electrolito. El electrodo positivo se llama cátodo y aquí es donde la reacción de reducción. El electrodo negativo es el ánodo y aquí es donde la reacción de oxidación. El electrolito también se llama puente de sal y es la solución conductora de iones.
Para que comprenda cómo esto genera corriente eléctrica, vea el caso de una de las primeras baterías, la
Pila de Daniell, en el cual había un recipiente con una solución de sulfato de cobre (CuSO4 (aq)) y, sumergido en esa solución, era una placa de cobre. En otro recipiente separado, había una solución de sulfato de zinc (ZnSO4 (aq)) y una placa de zinc sumergida. Las dos soluciones estaban conectadas por un puente salino, que era un tubo de vidrio con una solución de sulfato de potasio (K2SOLO4 (aq)) con lana de vidrio en los extremos. Finalmente, las dos placas estaban interconectadas por un circuito externo, con una lámpara, cuya iluminación indicaría el paso de la corriente eléctrica: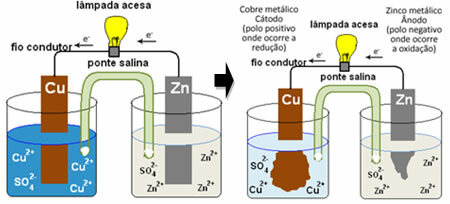
Lo que pasa es que el zinc tiene una mayor tendencia a oxidarse, es decir, a perder electrones, por lo que el zinc metálico de la pala funciona como electrodo negativo, el ánodo, donde se produce la oxidación: Zn( s) ↔ Zn2+(aquí) + 2 y-. Los electrones perdidos por el zinc son transportados por el circuito externo al cobre, generando la corriente eléctrica que enciende la lámpara. Los iones de cobre en la solución reciben electrones (se reducen) y se transforman en cobre metálico que se deposita sobre la hoja de cobre. Esto significa que este es el electrodo positivo, cátodo, donde ocurre la reducción: Culo2+(aquí) + 2 y- ↔ culo( s).
No pares ahora... Hay más después de la publicidad;)
Las baterías de hoy tienen este mismo principio de funcionamiento, en el que un metal dona electrones a otro, a través de una solución conductora, y se produce una corriente eléctrica. La diferencia es que las baterías que se usan hoy en día son secas, porque no usan una solución líquida como electrolito, como ocurre en la batería de Daniell.
Hoy en día existe una variedad muy amplia de baterías que se venden comercialmente. Entre ellos los más comunes son los células ácidas (de Leclanché) y laspilas alcalinas.
Ambos tienen zinc como electrodo negativo; por otro lado, como polo positivo, hay una barra de grafito instalada en el medio del pilote rodeada de dióxido de manganeso (MnO2), carbón vegetal en polvo (C) y una pasta húmeda. La diferencia es que, en la pila de ácido, se usa cloruro de amonio (NH) en la pasta húmeda.4Cl) y cloruro de zinc (ZnCl2) - sales ácidas - además del agua (H2O). En la batería alcalina, se utiliza hidróxido de potasio (KOH), que es una base.

Las baterías Leclanché son las más adecuadas para equipos que requieren una descarga ligera y continua, como control remoto, reloj de pared, radio portátil y juguetes. Las pilas alcalinas, por otro lado, tienen entre un 50 y un 100% más de energía que una pila común del mismo tamaño, siendo recomendada para equipos que requieren descargas más rápidas e intensas, como radios, reproductores de CD / DVD, MP3 portátiles, linternas, cámaras fotográficas digitales etc.

Obtenga más información sobre qué electrolitos y electrodos se utilizan en estos y otros tipos de baterías. en cuanto a qué tipos de equipos son los más recomendados, leyendo los artículos relacionados más bramido.
Por Jennifer Fogaça
Licenciada en Química


