El texto Primera ley de radiactividad o primera ley de Soddy mostró la primera ley general que corresponde a lo que sucede cuando un átomo de un elemento radiactivo sufre desintegración alfa.
LA segunda ley de radiactividad o La segunda ley de Soddy se refiere a la desintegración beta. Vea lo que dice esta ley:
“Cuando un átomo emite una partícula beta, su número atómico (Z) aumenta en una unidad y su número de masa (A) permanece igual ".
Genéricamente, podemos representar esta ley mediante la siguiente ecuación:
ZLAX →-10β + Z + 1LAY
El número atómico (Z) es el número de protones en el núcleo atómico. El número de masa (A) corresponde a la suma de los protones y neutrones existentes en el núcleo (A = p + n). Esto significa que el átomo obtenido es una isobare del átomo original, es decir, tienen el mismo número de masa.
Aquí hay un ejemplo: el torio-231 emite una partícula beta y forma protactina-231:
23190Th → -10β + 23191Sartén
Tenga en cuenta que hay conservación del número de masa y el número atómico en los dos miembros de la ecuación:
A: 231 = 0 + 231;
Z: 90 = -1 + 91.
Entonces, puede usar esta regla para averiguar qué partícula se emitió o qué átomo se formó.
Como se explica en el texto Problema beta (β), esta emisión es como un electrón porque tiene una carga de -1 y no tiene masa. Pero entonces, ¿por qué aumenta el número atómico y el número másico permanece constante?
Este hecho fue explicado por una hipótesis lanzada por el físico italiano Enrico Fermi (1901-1954).

Un sello postal impreso alrededor de 2001 en los EE.UU. muestra una imagen del ganador del Premio Nobel de Física Enrico Fermi
No pares ahora... Hay más después de la publicidad;)
Enrico Fermi propuso lo siguiente:
“La emisión de partículas beta ocurre cuando un neutrón inestable dentro del núcleo atómico se desintegra, formando un protón que permanece en el núcleo. Al mismo tiempo, esta desintegración forma la partícula beta (-10β), que es similar al electrón y es emitido por el núcleo junto con el radiación gamma (γ - es solo radiación electromagnética, sin carga eléctrica ni masa) y un neutrino (00ν, partícula de carga y masa nula).”
O sea:
01n → 11p + -10β + 00 γ + 00ν
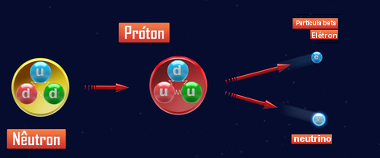
Desintegración de neutrones para la emisión de partículas beta
El protón y el neutrón tienen prácticamente la misma masa, por lo que cuando un átomo emite una partícula beta, su número de La masa (A) permanece igual, es decir, mientras el neutrón se desintegra, se forma el protón, reemplazándolo en el núcleo, por lo que decir. Dado que se forma el protón, el número atómico aumenta en uno.
Consulte la siguiente ilustración para ver otro ejemplo de cómo esta ley se aplica realmente en casos de desintegraciones beta. En él, el isótopo 14 del elemento carbono emite una partícula beta, transformándose en nitrógeno-14:

Desintegración beta del carbono 14 que genera nitrógeno 14
__________________
* Imagen con derechos de autor: pasarela / Shutterstock.com.
Por Jennifer Fogaça
Licenciada en Química
¿Le gustaría hacer referencia a este texto en una escuela o trabajo académico? Vea:
FOGAÇA, Jennifer Rocha Vargas. "Segunda ley de radiactividad o segunda ley de Soddy"; Escuela Brasil. Disponible: https://brasilescola.uol.com.br/quimica/segunda-lei-radioatividade-ou-segunda-lei-soddy.htm. Consultado el 27 de junio de 2021.