- Descubrimiento:
Como se indica en el texto "Emisión alfa (α)”, El químico neozelandés Ernest Rutherford realizó un experimento en el que colocó una muestra de un material radiactivo en un bloque de plomo, con un orificio para dirigir las emisiones radiactivas; y sometió estas radiaciones a un campo electromagnético.
Entre los resultados obtenidos, Rutherford notó que un haz de radiación era atraído por la placa positiva, lo que le llevó a concluir que estas emisiones eran de carga negativa. Esta radiación se llamó rayoso emisiones betaβ).
Dado que los rayos sufrieron desviación cuando se sometieron a un campo electromagnético, esto también lo llevó a concluir que en realidad estaban compuestos de partículas que tienen masa. La masa de estas partículas, sin embargo, fue menor que la de las partículas que constituían las emisiones alfa, porque las partículas beta sufrieron una mayor desviación.
- Constitución:
En 1900, el físico francés Antoine-Henri Bequerel (1852-1908) comparó estas desviaciones sufridas por el partículas beta con los cambios que realizan los electrones cuando también están sujetos a un campo electromagnético. El resultado fue que eran iguales; con eso, se vio que
las partículas beta eran en realidad electrones.Como resultado, la representación de esta partícula viene dada por 0-1β o β-. Tenga en cuenta que la emisión beta tiene un número de masa (A) igual a cero, ya que los electrones no son parte del núcleo del átomo.
- Consecuencias de la emisión de partículas beta para la estructura del átomo:
La emisión de una partícula beta (0-1β) es el resultado de la reordenación del núcleo inestable del átomo radiactivo para adquirir estabilidad. Por tanto, se produce un fenómeno en el núcleo, en el que se descompone un neutrón, originando tres nuevas partículas: un protón, un electrón (partícula β) y un neutrino. Se emiten antineutrinos y electrones; el protón, sin embargo, permanece en el núcleo.
10No →11p + 0-1y + 00ν
neutrón neutrino de electrones de protones
No pares ahora... Hay más después de la publicidad;)
De esa forma, cuando un átomo emite una partícula beta, cambia a un nuevo elemento con el mismo número de masa (porque el neutrón que existía antes ha sido "reemplazado" por el protón), pero su número atómico (Z = protones en el núcleo) aumenta en un unidad.
Vea a continuación cómo sucede esto en general:
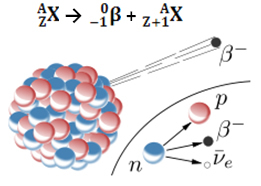
Aquí hay un ejemplo de desintegración beta que ocurre con el isótopo 14 del elemento carbono:

La radiación beta consta de electrones emitidos a alta velocidad por los núcleos de átomos radiactivos, esta velocidad inicial es de 100 000 km / s hasta 290 000 km / sy alcanza el 95% de la velocidad del luz.
La masa de la radiación β es la misma que la de un electrón, que es 1840 veces más pequeña que la de un protón o neutrón. La radiación alfa (α) emite dos protones y dos neutrones, por lo que la masa de las partículas α es 7360 veces la de las partículas β. Esto explica el hecho de que las partículas α sufren una desviación menor que las partículas β, como había verificado Rutherford en su experimento.
- Poder de penetración:
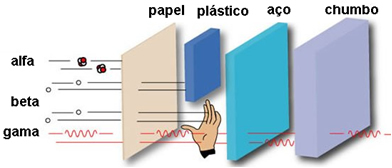
Su poder de penetración es medio, siendo de 50 a 100 veces más penetrante que las partículas alfa. Estos pueden atravesar una hoja de papel, pero están sujetos por una hoja de solo 2 mm de plomo o 2 cm de aluminio. Cuando afectan al cuerpo humano, pueden penetrar hasta 2 cm.
- Daño a humanos:
Dado que su poder de penetración sobre el cuerpo humano es de solo 2 cm, las partículas β pueden penetrar la piel, provocando quemaduras, pero se detienen antes de llegar a la mayoría de órganos internos del cuerpo.
Por Jennifer Fogaça
Licenciada en Química
¿Le gustaría hacer referencia a este texto en una escuela o trabajo académico? Vea:
FOGAÇA, Jennifer Rocha Vargas. "Problema beta"; Escuela Brasil. Disponible: https://brasilescola.uol.com.br/quimica/emissao-beta.htm. Consultado el 27 de junio de 2021.


