Στο αμίδια είναι οργανικές ενώσεις που χαρακτηρίζονται από παρουσία α άζωτο (N) άμεσα συνδεδεμένο με ένα καρβονύλιο (C = O). Αυτές είναι ουσίες διαθέσιμες με φυσικό τρόπο, μία από αυτές είναι στα περιττώματα των θηλαστικών (ουρία), αλλά μπορούν επίσης να ληφθούν με τεχνητή σύνθεση.
Τα αμίδια μπορούν να παραχθούν, για παράδειγμα, από αφυδάτωση αλατιού αμμωνίου, μέθοδος που χρησιμοποιείται για την κατασκευή πολυμερών. Χρησιμοποιούνται επίσης ως λιπάσματα, λόγω της διαθεσιμότητας των αζώτων και πώς φάρμακο, με αντιμικροβιακή δράση.
Διαβάστε περισσότερα:Ακρυλαμίδιο - αμίδιο που μπορεί να προέρχεται από τη θέρμανση ορισμένων τροφίμων
Αμιδική δομή
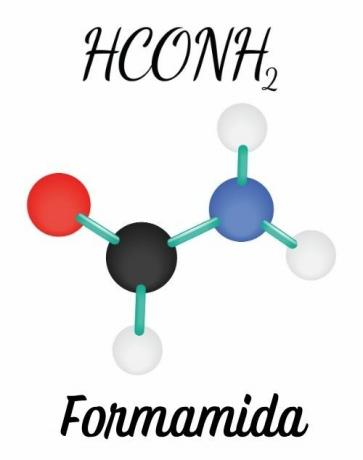
Τα αμίδια σχηματίζονται από ένα άζωτο συνδεδεμένο απευθείας με μια καρβονύλ ή ακύλ ομάδα (R-C = O). Ο διπλός δεσμός μεταξύ του άνθρακας είναι το οξυγόνο και η δυνατότητα μετακίνησης αυτού του ζεύγους σε άζωτο δίνει το μόριο επίπεδη γεωμετρία, σε αντίθεση με τις αμίνες, οι οποίες έχουν πυραμιδική γεωμετρία.
Ταξινόμηση αμιδίων
Ταξινόμηση σύμφωνα με τον αριθμό των οργανικών υποκαταστατών
Καθώς και η αμίνες, τα αμίδια ταξινομούνται σύμφωνα με το αριθμός υποκατάστασης οργανικών ριζών που έχει το άζωτοΩστόσο, για τα αμίδια, πρέπει να λάβουμε υπόψη ότι ένας από τους προσδέτες της ομάδας θα είναι η ακυλομάδα, δηλαδή θα έχουμε μόνο αμίδια του τύπου:
- Μη υποκατεστημένο αμίδιο: έχει άζωτο συνδεδεμένο με δύο υδρογόνα και μια ομάδα καρβονυλίου.
Παράδειγμα:

- Μονοϋποκατεστημένη αμίνη: έχει άζωτο συνδεδεμένο με υδρογόνο, καρβονύλ ομάδα και οργανική ρίζα. Σε αυτήν την περίπτωση, όπου ένα από τα υδρογόνα έχει αντικατασταθεί από μια αλυσίδα άνθρακα, θεωρήστε το R ως οργανική ομάδα.
Παράδειγμα:

- Υποκατεστημένη αμίνη: έχει άζωτο συνδεδεμένο με δύο οργανικές ρίζες και ένα καρβονύλιο. Στην περίπτωση αυτή, τα δύο υδρογόνα αντικαταστάθηκαν από αλυσίδες άνθρακα.
Παράδειγμα:

Δείτε επίσης: Πώς να ταξινομήσετε τα οργανικά αλογονίδια;
Ταξινόμηση σύμφωνα με τον αριθμό των καρβονυλίων που συνδέονται με το άζωτο
Τα αμίδια μπορούν επίσης να ταξινομηθούν σύμφωνα με τον αριθμό των καρβονυλίων που συνδέονται απευθείας στο άζωτο του μορίου.
- Πρωτεύοντα αμίδια: μόνο μία ακυλομάδα συνδεδεμένη με άζωτο (R-CO) NH2 .
- δευτεροταγή αμίδια: δύο καρβονύλια ή ακυλομάδα συνδεδεμένα με άζωτο (R-CO)2ΝΗ.
- τριτοταγή αμίδια: τρεις ακυλομάδες συνδεδεμένες με άζωτο (R-CO)3Οχι.

Ονοματολογία αμιδίων
Ο ονοματολογία για αμίδια θα δοθεί από:
πρόθεμα που υποδεικνύει τον αριθμό των ανθράκων στην αλυσίδα + θέση και το επίθεμα που υποδεικνύει ακόρεστους (εάν υπάρχουν) + τερματισμό αμιδίου |
Δείτε τον παρακάτω πίνακα:
Πρόθεμα (αριθμός ανθράκων) |
Infix (κορεσμός αλυσίδας) |
Επίθημα (λειτουργική ομάδα) |
|||
1 άνθρακας |
Συνάντησε- |
Μόνο μεμονωμένες κλήσεις |
-ένα- |
αμίδια |
-αμίδη |
2 άνθρακες |
Κ.λπ. |
||||
3 άνθρακες |
Στήριγμα- |
1 διπλός δεσμός |
-εν- |
||
4 άνθρακες |
Αλλά- |
||||
5 άνθρακες |
έγκλειστος- |
2 διπλοί δεσμοί |
-αδέν- |
||
6 άνθρακες |
Μαγεύω- |
||||
7 άνθρακες |
Επτά- |
1 τριπλός δεσμός |
-σε- |
||
8 άνθρακες |
Οκτ- |
||||
9 άνθρακες |
Μη- |
2 τριπλοί σύνδεσμοι |
-διενέργεια- |
||
10 άνθρακες |
Δεκ- |
Η μέτρηση του άνθρακα πρέπει να ξεκινά με την πλησιέστερη πλευρά του αζώτου της λειτουργικής ομάδας.
Παραδείγματα:
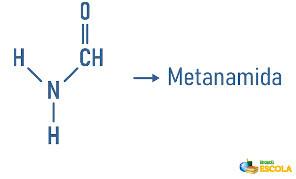



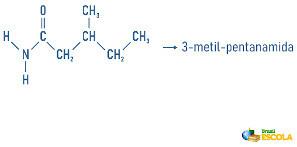
Οι αμίνες μπορούν επίσης να λάβουν στην ονοματολογία τους μια προδιαγραφή για την ταξινόμηση του μορίου:
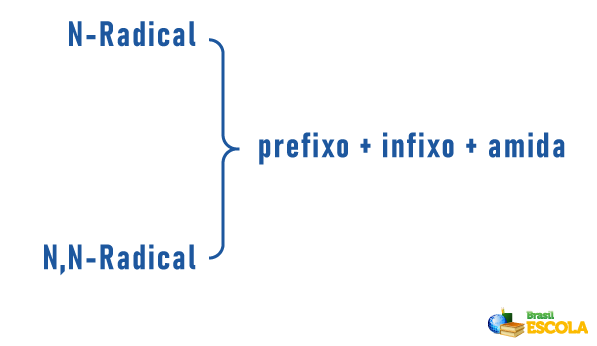
Υπενθυμίζοντας ότι η ονοματολογία για ρίζες σχηματίζεται από: Πrefix που δείχνει τον αριθμό των ανθράκων + τερματισμό "il" ή "ila". Οι ρίζες τοποθετούνται στην ονοματολογία με αλφαβητική σειρά.
Παραδείγματα:


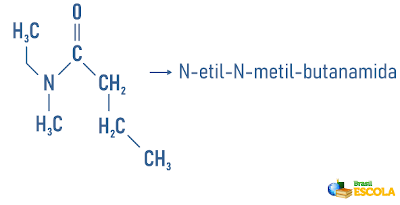
Επίσης πρόσβαση: Ονοματολογία κυκλικών και διακλαδισμένων υδρογονανθράκων
Ιδιότητες αμιδίων
- Υψηλό σημείο τήξεως και βρασμού, το οποίο θα έχει κλίμακα ανάλογα με το μέγεθος και τη χωρική διάταξη της αλυσίδας άνθρακα.
- Πολύ πολικό λόγω της παρουσίας καρβονυλίου και αζώτου.
- Μη υποκατεστημένος και μονοϋποκατεστημένος αμιδικός δεσμός υδρογόνου.
- Μικρότερα και απλούστερα μόρια είναι υδατοδιαλυτά. Το μέγεθος του μορίου επηρεάζει επίσης τη διαλυτότητα των αμιδίων: όσο μεγαλύτερη είναι η αλυσίδα άνθρακα, τόσο λιγότερο διαλυτές θα είναι στο νερό.
- Τα αμίδια είναι βασικά λόγω της τάσης λήψης ιόντων Η+.
Εφαρμογή αμιδίων
- Χρησιμοποιείται ως μεσάζων στην κατασκευή πολυαιθυλενίων όπως το νάιλον.
- Εφαρμόζεται στη σύνθεση φαρμάκων όπως σουλφανιλαμίδη και πενικιλλίνη, δραστικές αρχές βακτηριοκτόνων φαρμάκων για τον έλεγχο των λοιμώξεων.
- Η ουρία, η οποία μπορεί να ληφθεί συνθετικά ή ως προϊόν που εκκρίνεται από θηλαστικά, είναι μια ουσία της αμιδικής ομάδας, ένα διαμίδιο. Χρησιμοποιείται ως συμπλήρωμα διατροφής στη γεωργία και ως λίπασμα.

Λήψη των αμιδίων
Τα αμίδια βρίσκονται εύκολα σε φυσική μορφή, αλλά η συνθετική τους μορφή εξακολουθεί να χρησιμοποιείται ευρέως σε βιομηχανικές διαδικασίες. Ακολουθούν μερικές αντιδράσεις παραγωγής αμιδίων που βασίζονται σε άλλες αζωτούχες ενώσεις.
Αντίδραση αφυδάτωσης άλατος αμμωνίου

Αντίδραση αμινών με όξινο χλωρίδιο
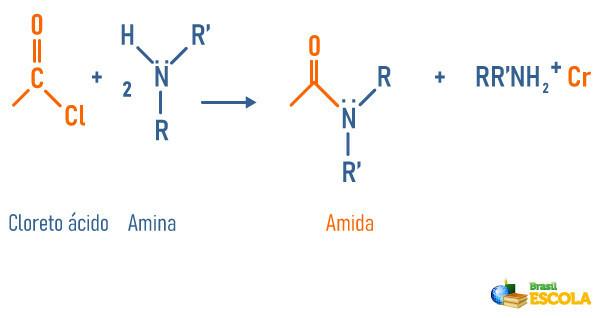
-
Αντίδραση ανυδριτών με αμίνες
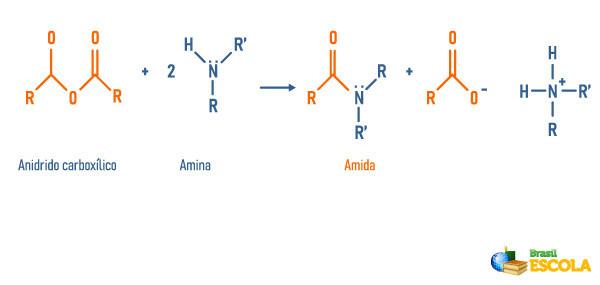
Αντίδραση εστέρων με αμίνες

Δομική αναδιάταξη μιας αλδοξίμης
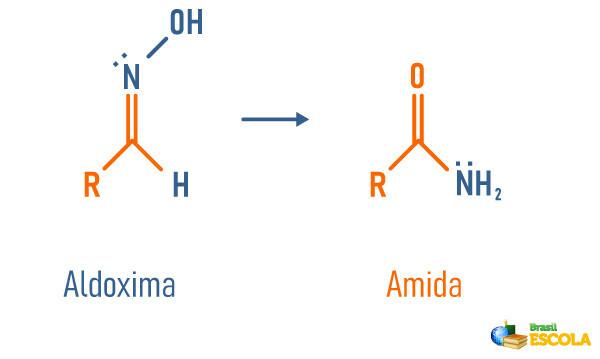
-
Ενυδάτωση νιτριλίου
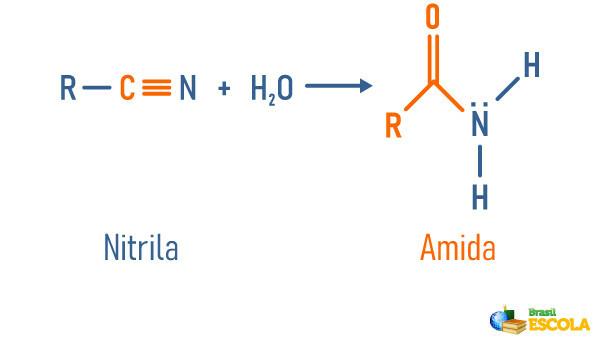
Διαβάστε επίσης: Υδρόλυση αμιδίου - αντίδραση που χρησιμοποιείται για τη λήψη σημαντικών ουσιών
λύσεις ασκήσεις
Ερώτηση 1 - (UFRS) Η ασπαρτάμη, που απεικονίζεται παρακάτω, είναι ένα τεχνητό γλυκαντικό που χρησιμοποιείται σε πολλά αναψυκτικά και τρόφιμα χαμηλών θερμίδων.

Η ομάδα που πλαισιώνεται στο σχήμα είναι χαρακτηριστική της οργανικής λειτουργίας
Α) εστέρας.
Β) αμίδιο.
Γ) αμινοξύ.
Δ) αμίνη.
Ε) υδατάνθρακες.
Ανάλυση
Εναλλακτική Β. Η λειτουργική ομάδα που επιλέγεται στο σχήμα είναι ένα αμίδιο, λόγω της παρουσίας ενός καρβονυλίου (C = O) συνδεδεμένου απευθείας με άζωτο (Ν).
Ερώτηση 2 - (UNESP) Τον Αύγουστο του 2005, αναφέρθηκε η κατάσχεση παρτίδων λιδοκαΐνης που θα είχαν προκαλέσει το θάνατο πολλών ανθρώπων στη Βραζιλία, λόγω κατασκευαστικών προβλημάτων. Αυτό το φάρμακο είναι ένα τοπικό αναισθητικό που χρησιμοποιείται ευρέως σε ενδοσκοπικές εξετάσεις, μειώνοντας την ενόχληση του ασθενούς. Η μοριακή του δομή φαίνεται παρακάτω:
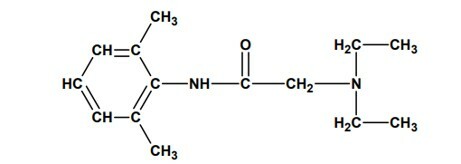
και παρουσιάζει τις λειτουργίες:
Α) δευτεροταγής αμίνη και τριτοταγής αμίνη.
Β) αμίδιο και τριτοταγής αμίνη.
Γ) αμίδιο και εστέρας.
Δ) εστέρας και τριτοταγής αμίνη.
Ε) εστέρας και δευτεροταγής αμίνη.
Ανάλυση
Εναλλακτική Β.
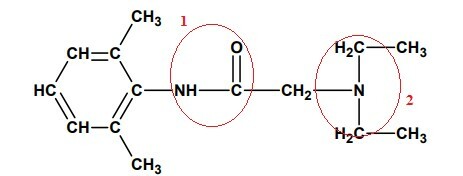
Αφού επιλέξετε και αρίθμηση των χαρακτηριστικών τμημάτων κάθε οργανικής λειτουργίας, ας αναλύσουμε το καθένα:
1- Είναι AMIDA λόγω της παρουσίας της ακυλομάδας, (R-C = O) που συνδέεται άμεσα με άζωτο, μονοϋποκατεστημένο.
2- Δεδομένου ότι δεν έχουμε την παρουσία της ακυλομάδας (R-C = O), αλλά μόνο το άζωτο συνδέεται απευθείας με άλλους άνθρακες αυτής της ομάδας Έχουμε μια ΠΕΡΙΟΡΙΣΤΗ ΑΜΙΝΗ, επειδή και τα τρία υδρογόνα, που προηγουμένως είχαν συνδεθεί με άζωτο, έχουν αντικατασταθεί από ομάδες Οργανικός.
Από τη Laysa Bernardes Marques de Araújo
Καθηγητής Χημείας
