Κατά τη μελέτη της Νευτώνης Μηχανικής (Κλασική Μηχανική), μπορεί να έχετε παρατηρήσει ότι γνωρίζοντας την αρχική θέση και τη στιγμή (μάζα και ταχύτητα) όλων των σωματιδίων που ανήκουν σε ένα σύστημα, μπορούμε να υπολογίσουμε τις αλληλεπιδράσεις τους και να προβλέψουμε πώς θα θα συμπεριφερθεί. Ωστόσο, για την κβαντομηχανική, αυτή η διαδικασία είναι λίγο πιο περίπλοκη.
Στα τέλη της δεκαετίας του 1920, ο Χάισενμπεργκ διατύπωσε τη λεγόμενη αρχή της αβεβαιότητας. Σύμφωνα με αυτήν την αρχή, δεν μπορούμε να προσδιορίσουμε με ακρίβεια και ταυτόχρονα τη θέση και την ορμή ενός σωματιδίου.
Δηλαδή, σε ένα πείραμα δεν μπορείτε ταυτόχρονα να προσδιορίσετε την ακριβή τιμή ενός στοιχείου ροής px ενός σωματιδίου και επίσης την ακριβή τιμή της αντίστοιχης συντεταγμένης, Χ. Αντ 'αυτού, η ακρίβεια της μέτρησης περιορίζεται από την ίδια τη διαδικασία μέτρησης, με τέτοιο τρόπο ώστε px. Δx≥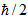 , όπου το px είναι γνωστό ως η αβεβαιότητα του Δpx, και η θέση x την ίδια στιγμή είναι η αβεβαιότητα Δx. Εδώ
, όπου το px είναι γνωστό ως η αβεβαιότητα του Δpx, και η θέση x την ίδια στιγμή είναι η αβεβαιότητα Δx. Εδώ  (Διαβάζει κάθετο h) είναι ένα απλοποιημένο σύμβολο για ω / 2η, Οπου Η είναι η σταθερά του Planck.
(Διαβάζει κάθετο h) είναι ένα απλοποιημένο σύμβολο για ω / 2η, Οπου Η είναι η σταθερά του Planck.
Ο λόγος για αυτήν την αβεβαιότητα δεν είναι πρόβλημα με τη συσκευή που χρησιμοποιείται για τη μέτρηση των φυσικών ποσοτήτων, αλλά για την ίδια τη φύση της ύλης και του φωτός.
Για να μετρήσουμε τη θέση ενός ηλεκτρονίου, για παράδειγμα, πρέπει να το δούμε και, για αυτό, πρέπει να το ανάψουμε (βασική αρχή της γεωμετρικής οπτικής). Επιπλέον, η μέτρηση θα είναι πιο ακριβής όσο μικρότερο είναι το μήκος κύματος του φωτός που χρησιμοποιείται. Στην περίπτωση αυτή, η κβαντική φυσική λέει ότι το φως σχηματίζεται από σωματίδια (φωτόνια), τα οποία έχουν ενέργεια ανάλογη με τη συχνότητα αυτού του φωτός. Επομένως, για να μετρήσουμε τη θέση ενός ηλεκτρονίου πρέπει να εστιάσουμε σε αυτό ένα πολύ ενεργητικό φωτονίο, καθώς όσο υψηλότερη είναι η συχνότητα, τόσο μικρότερο είναι το μήκος κύματος του φωτονίου.
Ωστόσο, για να ανάψει το ηλεκτρόνιο, το φωτόνιο πρέπει να συγκρουστεί με αυτό και αυτή η διαδικασία μεταφέρεται ενέργεια στο ηλεκτρόνιο, το οποίο θα αλλάξει την ταχύτητά του, καθιστώντας αδύνατο τον προσδιορισμό της ορμής του ακρίβεια.
Αυτή η αρχή που πρότεινε ο Heisenberg ισχύει μόνο για τον υποατομικό κόσμο, καθώς η ενέργεια φωτονίων που μεταφέρεται σε ένα μακροσκοπικό σώμα δεν θα μπορούσε να αλλάξει τη θέση της.
Από τον Kléber Cavalcante
Αποφοίτησε στη Φυσική
Πηγή: Σχολείο της Βραζιλίας - https://brasilescola.uol.com.br/fisica/principio-incerteza.htm

