Το ρυθμιστικό διάλυμα είναι συνήθως ένα μείγμα ενός αδύναμου οξέος και του άλατος αυτού του οξέος, ή μιας αδύναμης βάσης και του άλατος αυτής της βάσης. Αυτή η λύση προορίζεται να αποτρέψει την εμφάνιση πολύ μεγάλων μεταβολών στο ρΗ ή ρΟΗ ενός διαλύματος.
Ακολουθούν μερικά παραδείγματα λύσεων buffer:
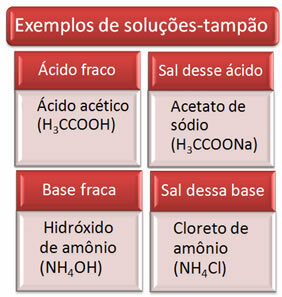
Η αποτελεσματικότητα του ρυθμιστικού διαλύματος μπορεί να φανεί στο αίμα μας, όπου, ακόμη και με την προσθήκη οξέος ή βάσης σε μικρές ποσότητες στο πλάσμα του αίματος, ουσιαστικά δεν υπάρχει αλλαγή στο pH του.
Πώς συμβαίνει αυτό, δεδομένου ότι εάν προσθέσουμε οξέα ή βάσεις στο νερό, το pH του αλλάζει γρήγορα;
Το ανθρώπινο αίμα είναι ένα ελαφρώς βασικό ρυθμιστικό σύστημα, δηλαδή είναι ένα ρυθμιστικό υγρό: το pH του παραμένει σταθερό μεταξύ 7,35 και 7,45. Ένα από τα πιο ενδιαφέροντα και σημαντικά ρυθμιστικά στο αίμα σχηματίζεται από ανθρακικό οξύ (Η2CO3) και από το άλας αυτού του οξέος, όξινο ανθρακικό νάτριο (NaHCO3).
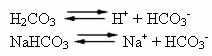
Έτσι, υπάρχουν τα ακόλουθα είδη σε αυτό το ρυθμιστικό διάλυμα:
Η2CO3: υπάρχει σε μεγάλες ποσότητες, καθώς είναι ασθενές οξύ, υποφέρει λίγο ιονισμό.
Η+: από τον ιονισμό του Η2CO3;
HCO3-: επίσης σε μεγάλες ποσότητες, από τον ιονισμό του H2CO3 και διαχωρισμός άλατος (NaHCO3);
Στο+: από τον ιονισμό του NaHCO3;
Εάν προστεθεί μια μικρή συγκέντρωση οξέος σε αυτό το διάλυμα, θα πραγματοποιηθεί ιονισμός του, δημιουργώντας H κατιόντα+, που θα αντιδράσει με ανιόντα HCO3- παρόν στο μέσο, που προέρχεται από μη ιονισμένο ανθρακικό οξύ. Δεν υπάρχει αλλαγή στο pH.
Εάν προστεθεί μια βάση, θα δημιουργηθούν ανιόντα ΟΗ-. Αυτά τα ιόντα συνδυάζονται με τα κατιόντα Η+, από τον ιονισμό του Η2CO3. Έτσι, τα ανιόντα του OH- εξουδετερώνονται, διατηρώντας το ρΗ του μέσου.
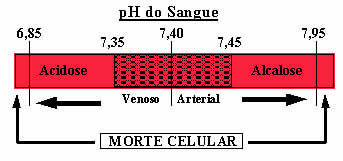
Εκτός από αυτό το ρυθμιστικό διάλυμα που αναφέρεται, υπάρχουν και άλλα δύο στο αίμα, τα οποία είναι: H2ΣΚΟΝΗ4/HPO42- και μερικές πρωτεΐνες. Εάν δεν υπήρχαν τέτοια ρυθμιστικά διαλύματα στο αίμα, το εύρος του pH θα μπορούσε να είναι σοβαρό. Εάν το pH του αίματος αυξηθεί πάνω από 7,8, ονομάζεται αλκάλωση. Εάν το pH πέσει πάρα πολύ, κάτω από 6,8, θα είναι μια κατάσταση οξέωσης. Και οι δύο είναι επικίνδυνες καταστάσεις που μπορούν να οδηγήσουν σε θάνατο.
Από την Jennifer Fogaça
Αποφοίτησε στη Χημεία
Πηγή: Σχολείο της Βραζιλίας - https://brasilescola.uol.com.br/quimica/solucaotampao-no-sangue-humano.htm

